- +1
【重磅综述】骨关节炎中细胞衰老的机制和治疗
以下文章来源于老顽童说 ,作者老顽童说
 老顽童说
老顽童说公众号致力于传播衰老相关的前沿科研进展和趣味科普,帮助大家更深入地了解衰老背后的科学故事~
 关注我们,获取更多相关资讯
关注我们,获取更多相关资讯翻译 By 左越晟、杨宽、马米阳、李豪
俗话说的好,“人老腿先老”。尽管大多数人都有着“老骥伏枥,志在千里”的愿望,却不得不面对无奈的现实:好不容易卸下工作的负担,等待着的不是“最美不过夕阳红”,而是找上门来的关节炎、“老寒腿”。2020年11月18日,来自北卡罗莱纳大学医学院的研究团队在Nature Reviews Rheumatology上发表了一篇标题为“Mechanisms and therapeutic implications of cellular senescence in osteoarthritis”的综述,旨在总结衰老与骨关节炎发生的关系,并概述了两类可用于骨关节炎治疗的新型药物。衰老与关节炎之间存在着怎样说不清道不明的关系?可能成为关节炎患者福音的潜力新药又是何方神圣?下面,请听小编我一一细说!
 通讯作者:Richard F. Loeser教授(图片源于网络)
通讯作者:Richard F. Loeser教授(图片源于网络)摘 要
骨关节炎(Osteoarthritis, OA)的发展与关节组织中衰老细胞数量的增加有关,并且OA和软骨降解也与衰老相关分泌表型(Senescence-associated secretory phenotype, SASP)有关。年龄相关的线粒体功能障碍和相关的氧化应激都可能诱导关节组织细胞衰老。但衰老并不是OA的唯一驱动力,而且衰老细胞诱发疾病的机制目前仍不明确。此外,能够影响OA表型的关节细胞类型及SASP因子也尚待确定。目前该领域的研究着眼于开发能清除或逆转衰老细胞以阻止疾病发病进程的药物疗法(即使用Senolytics和Senomorphics这两类药物)。更好地了解衰老如何导致关节功能障碍,可能会增强这些治疗方法的有效性,缓解OA患者的痛苦。
正 文
骨关节炎(Osteoarthritis,OA)作为最常见的关节炎类型,是一种以软骨退化和骨质增生、软骨下骨增厚为特征的滑膜关节疾病。OA还伴有不同程度的滑膜炎和包括韧带和膝关节半月板在内的其他关节结构的损伤。OA进行性的发展,最终导致衰弱性疼痛和活动能力的丧失,这点在老年人群体中尤为明显。尽管OA与肥胖、关节损伤和遗传等风险因素都脱不开干系,但年龄是最普遍的风险因素。随着婴儿潮一代(即1946年至1964年出生的人)的老龄化,美国患有OA的人数预计将从现有的3,000万上升到2030年的6,700万,而这其中一半以上的病例将会是65岁以上的老年人。除了OA患者要承受疼痛和行动不便的负担外,据2013年发布的数据,这种疾病的治疗和护理每年会给美国医疗系统造成270亿美元的经济负担,造成的生产力损失更是难以估量。因此,衰老和制药领域的研究者对设计新型疗法以缓解OA的症状并延缓其病程产生了极大的兴趣。
在过去的5年内,研究者开始探索一种通过靶向软骨细胞和其他发生衰老的关节组织细胞来治疗OA的新方法。细胞衰老(Senescence)是衰老的标志之一,是细胞命运的一种,其特征是细胞周期永久停滞,并释放有害的促炎分子到周围的微环境中,这一特征被称为衰老相关分泌表型(Senescence-associated secretory phenotype,SASP)。衰老细胞随着机体的衰老而积累,导致细胞增殖减少,组织再生和功能受损。OA作为衰老相关疾病中的一种,其病理过程与衰老相关联的具体机制仍不明确。尽管如此,临床试验正在测试一种通过使用Senolytic(一类选择性诱导衰老细胞死亡的药物)清除衰老细胞以治疗OA的药物疗法。这种方法的早期结果已经显示出极大的应用前景,其能在小鼠模型中改善诸如特发性肺纤维化,动脉粥样硬化和癌症等其他衰老相关疾病。与OA病程进展相关的酶被认为属于SASP因子,Senomorphics(又被称为SASP抑制剂和Senostatics)通过选择性抑制SASP因子为OA的治疗提供了一条可能的途径,有望有朝一日减轻OA患者的痛苦。然而,由于缺乏这些药物对治疗关节疾病的特异性和疗效的研究,目前关于Senomorphics对OA治疗的益处仍有待验证。
本篇综述中,作者探讨了与细胞衰老相关的几种常见表型及其与OA病理学的联系。此外,作者还探讨了几种直接针对衰老细胞的治疗策略,而这些策略也正被验证其预防疾病和改善患者预后的作用。
亮 点
OA的病理学特征与关节组织中细胞衰老和衰老相关分泌表型部分重叠。
许多衰老相关标志物与OA有关,但哪些衰老标志物会引发疾病目前仍不清楚。
年龄增长、DNA损伤和氧化应激可诱导关节组织细胞衰老。
衰老细胞表型的复杂性使得鉴定衰老细胞必须谨慎使用生物标志物。
针对细胞衰老的OA疗法是一种有前途的新方法,值得进一步研究。
细胞衰老与SASP
自Hayflick和Moorhead半个世纪前发现细胞衰老现象以来,细胞衰老通常被定义为因复制压力和衰老而发生不可逆的细胞周期停滞。然而,过去十年的研究已经扩大了细胞衰老这一定义的范围,不仅仅将其定义局限于增殖能力的降低。譬如,在受损的神经元和衰老的骨细胞等终末分化细胞中检测到衰老表型。此外,衰老可以独立于复制应激过程,如通过DNA损伤、致癌信号和氧化应激而诱导。衰老可以被很好地描述为一个涉及细胞对多种细胞压力的新陈代谢、形态学和生理学转变的复杂过程。此外,衰老过程还可以通过改变旁分泌信号通路来影响邻近的细胞,这一发现促使研究人员研究衰老细胞是如何改变其微环境的,而微环境的改变可以对整个机体产生系统性的影响。
关于衰老的许多研究都致力于了解其多效性,因为它既是肿瘤抑制因子又是衰老相关疾病的驱动因素。作为一种肿瘤抑制因子,衰老与细胞周期抑制基因对致癌基因的上调响应相关,而这一上调响应会导致永久性的生长停滞并预防肿瘤的增生。作为相关疾病的驱动因素,衰老阻碍了长期的组织再生和正常的细胞功能,并与肌肉减少症,骨质疏松,黄斑变性,神经退行性疾病和OA等多种疾病相关。此外,衰老还在包括伤口愈合早期和胚胎发生过程中发挥着重要作用。
虽然衰老细胞处于生长停滞的状态,但它们在组织内并不是休眠的。相反,衰老的细胞仍然保持着活跃的新陈代谢,并在生理过程中发生动态变化,其中可能包括旁分泌信号的改变。SASP的特征之一是衰老细胞中诸如趋化因子、细胞因子、蛋白酶和生长因子等的生物活性分子分泌增加。这些分子可以在周围的微环境中诱导包括炎症、生长停滞和肿瘤发生等的一系列病理反应。从机制上讲,mTOR是SASP的关键调节因子,因为它能够差异性调节MAPK激酶激活的蛋白激酶2(MAPKAPK2,也称为MK2)和IL-1α的翻译。MK2被p38磷酸化,并使ZFP36L1失活,ZFP36L1是一种锌指蛋白,可降解许多促炎性SASP因子的mRNA。IL-1α促进NF-κB信号传导,这与许多SASP基因的上调有关。相应地,雷帕霉素对mTOR的抑制降低了SASP因子的表达。
不同的诱导衰老的刺激因素可以产生不同的分泌蛋白,而这些蛋白可以根据受影响组织的不同而产生不同的生物学结果,这进一步增加了SASP表型的复杂性。大部分关于SASP的研究都关注于其在疾病发生发展中的作用,以及如何针对SASP因子进行治疗干预。与SASP因子表达相关的疾病包括动脉粥样硬化、癌症、心脏功能障碍、髓系偏倚、肾功能障碍、OA和总体健康寿命的下降。确定特定的SASP因子如何导致衰老相关疾病中不同的病理结果,可能有助于进一步开发减轻疾病发展的疗法。因此,诸如SASP Atlas(http://www.saspatlas.com/)之类的数据库是很好用的工具,研究人员可以搜索和归类整理新的SASP因子及其对组织表型的影响。
细胞衰老与骨关节炎
尽管软骨细胞在动态平衡期间增殖水平较低,但它们在某些环境中确实保持了增殖的潜力。例如,在OA的早期阶段,软骨细胞以“簇”的形式增殖,这通常被认为是在尝试修复损伤。软骨细胞在组织培养中也会启动细胞分裂。静息(即可逆的细胞周期停滞)和衰老之间的关系是复杂的,有证据表明,对受损的静息细胞进行促分裂刺激,可以在其重新进入细胞周期时被诱导衰老。
像其他器官一样,关节组织也容易随着时间的推移而衰老和衰退,衰老的软骨细胞和滑膜成纤维细胞的数量与年龄密切相关。考虑到骨-软骨串扰的重要作用,衰老过程中骨细胞衰老加剧也可能是OA的原因之一。细胞衰老也是创伤后骨关节炎的一个特征,因为关节损伤会加速软骨细胞衰老,刺激软骨退化。异常的机械性负荷可能是损伤后过早衰老的原因之一,因为抵消剪切应力会驱动年轻软骨移植块的衰老。此外,增加OA易感性的风险因素已被发现与诱导细胞衰老的风险因素相重叠。例如,接受高热量和低营养饮食的小鼠表现出脂肪组织衰老加剧,而运动则缓解了这一结果。另外,OA可以诱导关节细胞中与衰老特征相关的表型改变。例如,细胞表面蛋白尿激酶型纤溶酶原激活剂表面受体(Urokinase plasminogen activator surface receptor, uPAR)在衰老细胞和骨关节炎关节软骨细胞中被广泛诱导。
随着时间的推移,衰老诱导细胞中的代谢模式发生重构,这可能推动OA的病理进程。事实上,将衰老的成纤维细胞移植到小鼠的膝关节中会导致软骨侵蚀、骨赘形成和活动能力丧失,这表明衰老的细胞改变了滑膜微环境,导致了类骨关节炎。衰老的关节细胞表现出共同的特征,如端粒缩短、p53和细胞周期蛋白依赖性激酶(CDK)抑制剂p21和p16INK4a(p16)的表达增加、通过线粒体功能障碍促进活性氧(ROS)的生成,以及衰老相关的异染色质增加。值得注意的是,软骨细胞、骨细胞和滑膜成纤维细胞也会表现出SASP。如上所述,SASP的一个特点是分泌促炎细胞因子,如IL-6、IL-17、IL-1β、抑瘤素M和肿瘤坏死因子,和其他几种SASP因子以诱导OA相关改变,包括炎症、骨生长和细胞外基质(ECM)的降解(图1)。因此,确定关节组织中SASP因子所诱发的表型后果将更好理解的OA发病机制。
OA患者关节液中IL-6等细胞因子水平升高。IL-6-STAT3信号通路可诱导正常人成纤维细胞提前衰老,提示这些细胞可能触发旁观效应,导致周围细胞进一步衰老和出现SASP。这一假说在软骨中进一步被证实,软骨细胞通过产生细胞外囊泡(Extracellular vesicles, EVs)促进细胞间通讯,与健康人相比,OA患者EVs的水平显著升高,并诱导附近细胞处于衰老状态。EVs在细胞衰老和OA中的作用后文将更详细地讨论。
细胞因子可以上调基质金属蛋白酶(MMPs)家族的表达。与细胞因子一样,基质金属蛋白酶,如MMP13(也称为胶原酶-3),以及带有血小板反应蛋白基序的去整合素和金属蛋白酶(ADAMTS),如ADAMTS-5,由细胞分泌到ECM中。MMPs和ADAMTS的分解代谢活性可以降解软骨中的ECM蛋白,包括硫酸化蛋白多糖、胶原和纤维连接蛋白。软骨细胞外基质的丢失是OA的一个关键早期特征,这进一步表明软骨细胞和滑膜关节其他细胞的衰老是OA发病的驱动因素。
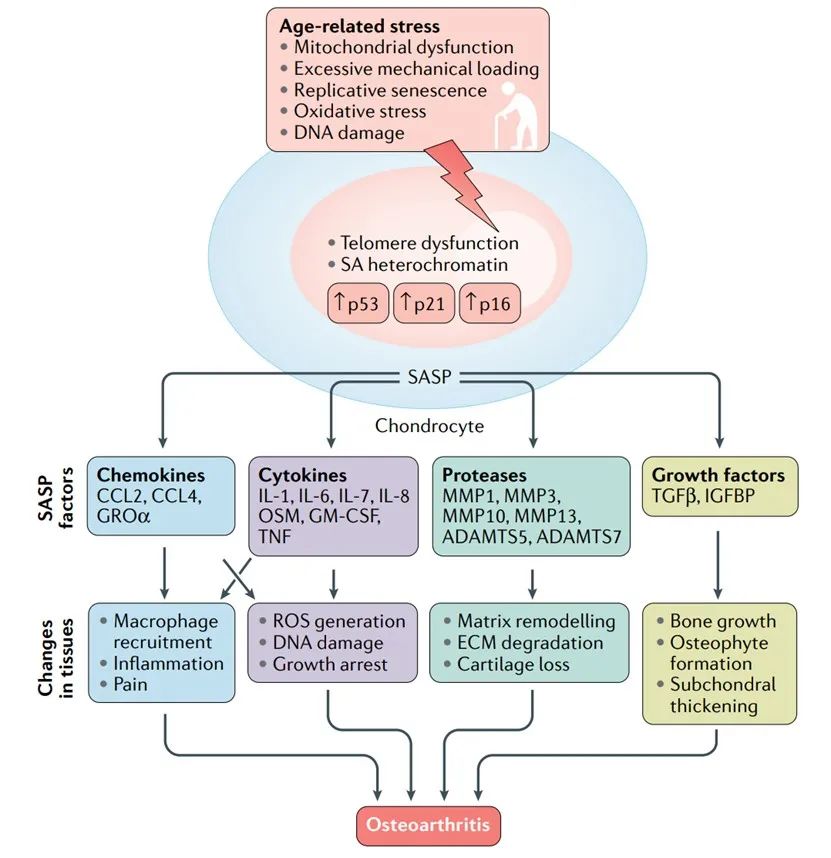 图1:年龄相关应激、衰老与骨质疏松症的关系。多种与年龄相关的压力集中在关节细胞衰老标志的诱导上。这些细胞可以表现出衰老相关的分泌表型(SASP)和分泌SASP因子(包括趋化因子、细胞因子、蛋白酶和生长因子),它们可以单独或共同作用,诱导骨关节炎组织中常见的变化。ADAMTS,一种带有血小板反应蛋白基序的去整合素和金属蛋白酶;CCL,CC-趋化因子配体;ECM,细胞外基质;GM-CSF,粒细胞-巨噬细胞集落刺激因子;GRO,生长调节的α蛋白;IGFBP,胰岛素样生长因子结合蛋白;MMP,基质金属蛋白酶;OA,骨关节炎;OSM,癌蛋白M;ROS,活性氧物种;SA异染色质,衰老相关的异染色质;TGFβ,转化生长因子-β。
图1:年龄相关应激、衰老与骨质疏松症的关系。多种与年龄相关的压力集中在关节细胞衰老标志的诱导上。这些细胞可以表现出衰老相关的分泌表型(SASP)和分泌SASP因子(包括趋化因子、细胞因子、蛋白酶和生长因子),它们可以单独或共同作用,诱导骨关节炎组织中常见的变化。ADAMTS,一种带有血小板反应蛋白基序的去整合素和金属蛋白酶;CCL,CC-趋化因子配体;ECM,细胞外基质;GM-CSF,粒细胞-巨噬细胞集落刺激因子;GRO,生长调节的α蛋白;IGFBP,胰岛素样生长因子结合蛋白;MMP,基质金属蛋白酶;OA,骨关节炎;OSM,癌蛋白M;ROS,活性氧物种;SA异染色质,衰老相关的异染色质;TGFβ,转化生长因子-β。衰老过程与生物标志物
在细胞衰老过程中会发生几种表型转变。在这里,我们讨论其中的3个(衰老相关β-半乳糖苷酶(SA-β-gal)的产生、p16的表达和EV的分泌),以及它们与骨关节炎发病机制的关系(框1)。
衰老相关的β-半乳糖苷酶
检测衰老细胞的β-半乳糖苷酶活性的细胞化学染色,称为SA-β-gal染色,是细胞培养和组织样本中最常用的技术之一。阳性染色是由于溶酶体中β-半乳糖苷酶活性上调所致,在pH 4.0时酶活性最佳,但在pH 6.0时在衰老细胞中可检测到。在关节软骨中,老年小鼠中SA-β-gal阳性的软骨细胞数高于年轻小鼠。然而,要使用SA-β-gal作为关节衰老细胞的标志物必须注意一些事项。首先,溶酶体的酶活性受自噬途径的调节,分离和单层培养原代细胞可以增加基础自噬和衰老表型;因此,在培养的软骨细胞中,SA-β-gal染色可以代表自噬的增加,而不是衰老状态。第二,沉默编码β-半乳糖苷酶的基因GLB1可以消除SA-β-gal染色,但不能抑制衰老,这表明了SA-β-gal阳性染色与衰老的间接联系。第三,在幼年啮齿动物的神经元中观察到与衰老无关的β-半乳糖苷酶染色,这与细胞生长过程中溶酶体的增加有关。最后,一种溶酶体功能失调的疾病,常染色体隐性G(M1)神经节苷脂沉积症,患者成纤维细胞在经历复制衰老后SA-β-gal呈阴性。综上所述,这些研究表明,决定SA-β-gal染色的结果的是自噬和细胞溶酶体活性的变化,而不是衰老。
因此,在进行SA-β-gal染色时,应考虑随年龄和OA而发生的自噬变化。OA患者的自噬和溶酶体功能降低,而自噬的刺激(例如,用雷帕霉素)可以赋予正常人软骨保护性的稳态效应。自噬也可以由多种与衰老无关的细胞应激刺激,包括营养剥夺、缺氧、活性氧、DNA损伤、蛋白质聚集体、受损细胞器或细胞内病原体。低氧诱导的自噬尤其令人担忧,因为软骨细胞由于软骨中缺乏血管而处于低氧条件下。这种环境中的新陈代谢和动态平衡是通过自噬来维持的,自噬可以回收细胞内的氨基酸并清除功能失调的线粒体。因此,软骨细胞在正常生理条件下表达自噬标记ULK1、Beclin1和LC3,这表明自噬在这些细胞中具有结构性活性。
由于这些原因,在使用细胞衰老作为OA进展指标的研究中,理想的SA-β-gal实验应该在关节组织上开展,而不是在培养的细胞上进行,这些研究应该包括一个或多个额外的衰老生物标志物。此外,当诱导或治疗OA样表型时,应仔细考虑正在应用的治疗对自噬有何影响。
p16
p16通过结合CDK4和CDK6,阻止细胞周期抑制蛋白视网膜母细胞瘤相关蛋白(Rb)的下游抑制,诱导细胞衰老。p16在细胞应激中表达上调,如辐射或端粒缩短造成的DNA损伤、ROS或致癌应激。作为一种肿瘤抑制因子,p16突变与几种癌症的风险增加有关,包括皮肤恶性黑色素瘤和胰腺癌。除了作为生物标记物的作用外,选择性去除p16高表达细胞还可以延长小鼠的寿命和健康寿命,表明p16高表达细胞影响衰老相关病理的发生。
重要的是,在小鼠和人关节软骨细胞中,p16的高表达与年龄相关。高表达p16的软骨细胞也降低了软骨相关ECM蛋白表达,如聚集蛋白聚糖,但增加了ECM降解SASP因子的表达,如MMP13和MMP1。这些初步结果表明,软骨细胞衰老不仅与年龄密切相关,而且还会导致新陈代谢转化,从而使软骨进一步破坏。鉴于p16和SASP可能是衰老表型的独立分支,研究人员还评估了p16本身是否与OA病理有关,结果发现并非如此。事实上,成年小鼠软骨细胞中p16的体细胞失活并没有抑制SASP,也没有改变OA对生理老化或诱导的关节损伤的反应速度。综上所述,这些结果表明p16可以作为软骨细胞衰老的生物标志物,但软骨细胞p16的表达似乎与OA无因果关系。
胞外囊泡
了解衰老如何诱导组织结构改变是衰老研究的一个主要焦点,但研究衰老如何影响维持组织动态平衡和功能的循环因子也很重要。在一项具有里程碑意义的研究中,老年小鼠通过异体共生模型暴露于年轻小鼠体内存在的因子,表现出骨骼肌祖细胞再生能力的恢复。此外,一项研究发现,将年轻小鼠暴露在老龄鼠血液中将导致年轻小鼠组织功能和修复受损。异体共生尚未被广泛用于研究软骨功能,但今年发表的一项实验表明,长达4个月的异体共生实验中,与年轻小鼠共用血液循环发生OA的程度比与年老小鼠共用循环系统的要轻。这项研究进一步表明,每天全身注射再生因子-生长/分化因子11可以促进软骨细胞的增殖,并保护小鼠免受关节组织退化的影响。鉴于这些结果,确定有助于促进或恶化关节组织健康的特定循环系统因素对于理解OA和其他与年龄相关性疾病的机制可能很重要。
EV,如外泌体,是微小脂膜结合颗粒,通过运输蛋白质和RNA促进细胞间的通讯。与SASP因子一样,EV分泌在衰老细胞中上调,这可以诱导邻近细胞提前衰老,例如,通过转移激活衰老途径的microRNA。有趣的是,一项横向和纵向研究发现,EV在血浆中的浓度随着年龄的增长而降低。然而,这种下降伴随着B细胞和单核细胞囊泡内化和激活的增加,提示EVs可能随着年龄的增长而增强促炎免疫反应。总而言之,这些研究强调了EVs在细胞和组织衰老中的新作用。
在另一项研究中,相对于健康人的软骨,OA患者的软骨中衰老的软骨细胞和EV浓度都较高。此外,将非衰老软骨细胞暴露于来自OA患者的EV可增加衰老表型并减少蛋白多糖的产生。荧光标记和EVs追踪证实,这些囊泡在暴露后6 h内被软骨细胞内化。在衰老相关的EVs和不与衰老相关的EVs中,microRNAs也有不同的表达;前者表现为较低水平的miR-140-3p,而miR-140-3p的缺失与软骨功能障碍有关,miR-34a-5p的增加与衰老相关蛋白的上调有关。使用促进衰老的化合物UBX0101(见下文)选择性去除衰老细胞,减少了培养的OA患者软骨细胞中EV的数量,从UBX0101治疗的小鼠的关节滑液中分离出的EV含有与软骨生长相关的特征,如凝集素增加和蛋白酶减少。总之,这项工作表明,EV分泌和内化的增加,以及囊泡RNA和蛋白质含量的变化,都应作为软骨细胞衰老和OA的潜在生物标志物进行研究。重要的是,这项研究的作者还发现,在老年健康供体和临床OA供体之间,滑液中的EV中microRNAs的表达存在差异。检查EV microRNA图谱可以帮助区分除衰老外,由OA和其他关节疾病造成的软骨丢失。
框1
细胞衰老中常见的变化
β-半乳糖苷酶的产量提高
p16INK4a表达量增高
不可逆转的生长停滞
细胞外囊泡(EVs)分泌增加
EV的microRNA含量改变
基因组不稳定
异染色质水平增加
端粒磨损
蛋白平衡丧失
营养感知失调
线粒体功能障碍
活性氧和活性氮产生增加
衰老相关分泌表型因子分泌增加
尿激酶型纤溶酶原激活剂表面受体(uPAR)上调
氧化应激驱动OA和衰老
衰老的另一个标志是线粒体功能障碍,它通过提高胞内ROS水平引起氧化应激。ROS诱导的DNA损伤与许多衰老相关疾病的发病机理有关,包括心血管,肺,肾和神经退行性疾病。此外,氧化应激的升高和线粒体抗氧化能力的降低会破坏细胞生理信号转导,这可能会通过逐渐引起细胞完整性和组织稳态的丧失而促进衰老。
关于OA,有人提出氧化应激是导致软骨分解代谢和合成代谢信号失衡的驱动因素,导致基质逐渐降解(图2)。 例如,氧化应激的存活和耐受性由MAPK通路的成员调节,如c-Jun N-末端激酶(c-Jun N-terminal kinases,JNKs)和p38。已有研究表明细胞因子介导的JNK信号激活会通过激活关节组织细胞中的促炎和ECM降解通路而使OA相关表型恶化。然而,在培养的人软骨细胞中,氧化应激使JNK失活,而p38仍保持活性。与野生型小鼠相比,小鼠中JNK1和JNK2的缺失导致更为严重的衰老相关OA,以及软骨尤其是滑膜中的衰老加重,这表明JNK是关节衰老的负调节剂。
除年龄增长外,衰老本身已被证实能够诱发线粒体功能障碍和刺激ROS产生。在人类和猴子的老年软骨和OA软骨中均检测到过氧化氢和活性氮自由基(包括一氧化氮(Nitric oxide, NO))的过量产生。体外培养的人软骨外植体细胞在过氧化氢刺激下表现出明显的细胞衰老特征,包括端粒缩短、复制能力降低和糖胺聚糖产量降低。已知抗氧化酶(如超氧化物歧化酶(Superoxide dismutase,SOD))的缺失与早衰和加速的衰老表型有关。全部三个SOD家族成员(SOD1、SOD2和SOD3)在人关节软骨中均大量表达,但其活性在OA患者的软骨中显著降低。
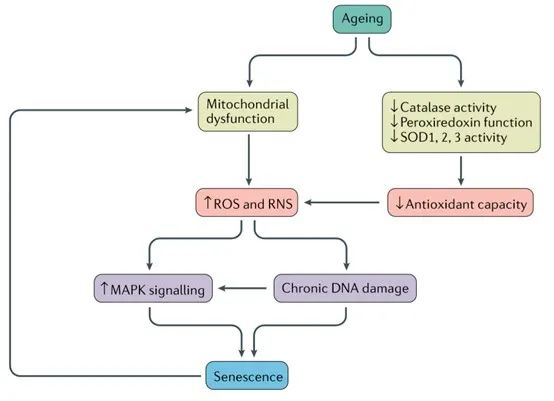 图2:氧化应激诱导的关节细胞衰老模型。衰老的软骨细胞和滑膜细胞通过降低过氧化氢酶和超氧化物歧化酶(SOD)的活性以及降低过氧化物酶的功能,表现出线粒体功能障碍以及抗氧化能力的降低。这些表型提高了活性氧自由基(ROS)和活性氮自由基(RNS)的生成,从而诱导了慢性DNA损伤并增强了MAPK应激信号传导,二者均可独立或共同发挥作用来诱导衰老。衰老本身可引起线粒体进一步损伤,引起正反馈。
图2:氧化应激诱导的关节细胞衰老模型。衰老的软骨细胞和滑膜细胞通过降低过氧化氢酶和超氧化物歧化酶(SOD)的活性以及降低过氧化物酶的功能,表现出线粒体功能障碍以及抗氧化能力的降低。这些表型提高了活性氧自由基(ROS)和活性氮自由基(RNS)的生成,从而诱导了慢性DNA损伤并增强了MAPK应激信号传导,二者均可独立或共同发挥作用来诱导衰老。衰老本身可引起线粒体进一步损伤,引起正反馈。与之类似,过氧化物酶和过氧化氢酶是抗氧化剂,在调节氧化还原信号和通过控制H2O2的含量来保护氧化应激中发挥重要作用。有研究注意到,从老年人中分离出的软骨细胞具有过氧化的(因此失活的)过氧化物酶,而针对线粒体的过氧化氢酶的过表达降低了24月龄小鼠OA的严重程度。总之,这些结果表明氧化应激的增加和软骨衰老的诱导之间的相关性,这可能驱动OA。这些结果还支持使用抗氧化剂防止ROS诱导衰老,这可能是治疗OA的有效方法。
用于治疗OA的Senolytics和 Senomorphics
Senolytics和Senomorphics是两类治疗药物,据报道它们可减轻小鼠模型中的衰老相关病理表型,目前正在人类试验中进行研究。Senolytics优先诱导衰老细胞凋亡,而Senomorphics抑制与促炎旁分泌信号传导和组织损伤相关的SASP因子(图3)。考虑到细胞衰老、SASP和OA之间的相关性,这些药物是靶向OA发病机制并减慢其进展的有力候选者。
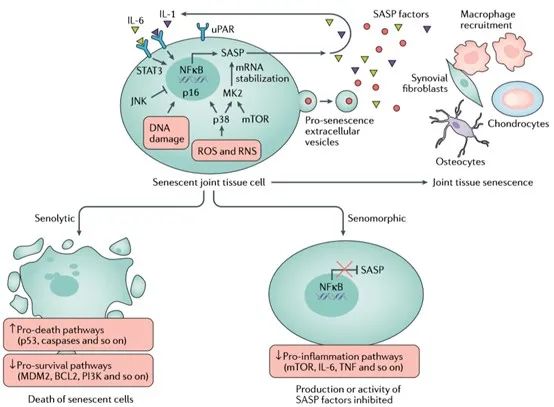 图3:关节组织中细胞衰老的模型和潜在的治疗方法。细胞因子(例如IL-6)通过转录因子STAT3促进衰老,而IL-1可以诱导NF-κB驱动的编码衰老相关分泌表型(SASP)因子的基因表达。衰老的关节细胞的特征是氧化应激增加(由于产生活性氧自由基(ROS)和活性氮自由基(RNS)),DNA损伤,尿激酶型纤溶酶原激活物表面受体(uPAR)的表达增加以及应激蛋白的上调,例如p38,c-JunN末端激酶(JNK)和mTOR。p38诱导衰老和p16的表达,而JNK负调控关节组织细胞的衰老。mTOR和p38通过上调(mTOR)的翻译和磷酸化(p38)MK2(也称为MAPKAPK2)来促进SASP,MK2稳定了编码SASP因子的mRNA转录物。这些细胞将SASP因子(包括IL-1和IL-6)和诱导衰老的细胞外囊泡分泌到细胞外基质中,从而促进周围关节组织中巨噬细胞的募集和进一步衰老。Senolytic药物旨在通过上调死亡相关通路中的p53,胱天蛋白酶和其他蛋白质来诱导特别是衰老细胞的凋亡,从而预防衰老相关疾病,同时抑制与细胞存活相关的通路(如涉及MDM2,BCL2和PI3K的通路)。Senomorphic药物不会杀死衰老细胞,而是通过抑制与炎症相关的蛋白质(如mTOR)的活性或直接抑制SASP因子(如IL-6和TNF)的活性或产生来抑制SASP。
图3:关节组织中细胞衰老的模型和潜在的治疗方法。细胞因子(例如IL-6)通过转录因子STAT3促进衰老,而IL-1可以诱导NF-κB驱动的编码衰老相关分泌表型(SASP)因子的基因表达。衰老的关节细胞的特征是氧化应激增加(由于产生活性氧自由基(ROS)和活性氮自由基(RNS)),DNA损伤,尿激酶型纤溶酶原激活物表面受体(uPAR)的表达增加以及应激蛋白的上调,例如p38,c-JunN末端激酶(JNK)和mTOR。p38诱导衰老和p16的表达,而JNK负调控关节组织细胞的衰老。mTOR和p38通过上调(mTOR)的翻译和磷酸化(p38)MK2(也称为MAPKAPK2)来促进SASP,MK2稳定了编码SASP因子的mRNA转录物。这些细胞将SASP因子(包括IL-1和IL-6)和诱导衰老的细胞外囊泡分泌到细胞外基质中,从而促进周围关节组织中巨噬细胞的募集和进一步衰老。Senolytic药物旨在通过上调死亡相关通路中的p53,胱天蛋白酶和其他蛋白质来诱导特别是衰老细胞的凋亡,从而预防衰老相关疾病,同时抑制与细胞存活相关的通路(如涉及MDM2,BCL2和PI3K的通路)。Senomorphic药物不会杀死衰老细胞,而是通过抑制与炎症相关的蛋白质(如mTOR)的活性或直接抑制SASP因子(如IL-6和TNF)的活性或产生来抑制SASP。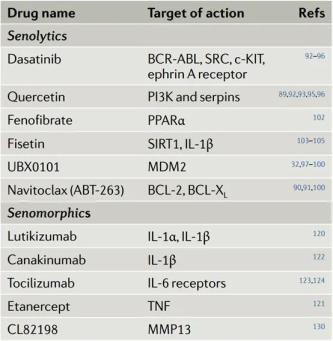 表1:Senolytics和Senomorphics有可能作为OA的疗法。MDM2, 小鼠双微体-2同源物;MMP13, 基质金属蛋白酶13;PPARα, 过氧化物酶体增殖物激活受体α;SIRT1, NAD依赖性去乙酰化酶Sirtuin-1。
表1:Senolytics和Senomorphics有可能作为OA的疗法。MDM2, 小鼠双微体-2同源物;MMP13, 基质金属蛋白酶13;PPARα, 过氧化物酶体增殖物激活受体α;SIRT1, NAD依赖性去乙酰化酶Sirtuin-1。Senolytics
基于OA的Senolytics研制。在开创性的临床前研究中,开发了一种可诱导的转基因手段,它可以靶向杀死和清除高水平表达p16的衰老细胞。与野生型小鼠相比,表达这种转基因的小鼠表现出更高的平均寿命和衰老相关病理的延缓。当使用类似的转基因技术清除小鼠关节软骨局部衰老细胞时,创伤后骨性关节炎的发展显著减弱。
尽管这些实验利用转基因小鼠在衰老细胞中诱导凋亡,但其他研究已经测试了Senolytics是否可以在治疗上模仿这种作用。在一项比较衰老细胞和增殖细胞基因表达谱的研究中,发现衰老可以上调编码抗凋亡信号网络中蛋白的基因,例如BCL-2家族成员和PI3K–AKT通路中的蛋白。许多Senolytics通过抑制衰老而非健康细胞中激活的促活途径,选择性地诱导衰老细胞凋亡。例如,通过BCL-2和BCL-XL双重抑制剂Navitoclax(ABT-263)处理受辐射或正常衰老的小鼠,来消除骨髓中衰老的造血干细胞,和衰老的肌肉干细胞并促进细胞再生。此外,在小鼠软骨外植体中,Navitoclax通过清除在细胞凋亡中表达高水平p16的软骨细胞来减轻衰老负担。另一个例子是达沙替尼和槲皮素的Senolytic复合药物,它可以有效清除衰老细胞,其用于治疗特发性肺纤维化(一种与衰老相关的致命性疾病)的疗效正在临床试验中。达沙替尼抑制多种酪氨酸激酶,包括BCR-ABL、SRC、c-KIT、ephrin A受体和血小板衍生生长因子β受体激酶,而槲皮素是一种植物黄酮醇,可抑制PI3K和的丝氨酸蛋白酶抑制剂(称作Serpins)。在另一项研究中,衰老细胞被移植到年轻和年老小鼠体内,导致身体机能障碍和寿命缩短。然而,用达沙替尼和槲皮素治疗这些小鼠可减轻衰老的有害影响,并延长健康期和寿命。同样,用达沙替尼和槲皮素治疗老年小鼠减少了骨骼中衰老骨细胞的数量,减少了破骨细胞形成和骨质流失,改善了矿物质的重吸收和厚度,并显著改善了小梁和皮质骨微结构。
尽管这些用于治疗关节组织疾病的药物尚未在人体中测试过,但目前正在OA的临床试验中研究其他几种Senolytics,包括UBX0101,该药物可抑制p53和小鼠双微体2同源物(MDM2)间的相互作用,MDM2是一种靶向p53降解的E3泛素蛋白连接酶。对患有创伤性OA的小鼠进行局部关节内注射UBX0101可以选择性清除衰老细胞,减少蛋白聚糖的损失,并减轻OA相关的疼痛和关节软骨退化的症状。在另一项研究中,软骨细胞中的促炎性应激诱导了组织蛋白酶B介导的NAD依赖性去乙酰化酶Sirtuin-1(SIRT1)的切割,该酶被发现在软骨细胞存活和ECM稳态中发挥关键作用。SIRT1的切割导致其缺少去乙酰化酶活性的N末端片段,而血清中N末端和C末端SIRT1片段的比例升高与早期OA和软骨衰老相关。研究人员证实,前交叉韧带横断可增加血清中N末端与C末端SIRT1的比例,而全身应用Navitoclax和关节内应用UBX0101联合清除衰老细胞降低了该比例。
高通量药物筛选可用于发现对软骨细胞和滑膜细胞起作用的新Senolytics,发现有助于OA病理研究的新机制。例如,在一项研究中,筛选了超过1,000种化合物在人软骨细胞系中的Senolytic活性。非诺贝特是一种黄酮类化合物,是过氧化物酶体增殖物激活受体-α(Peroxisome proliferator activated receptor-α, PPARα)的激动剂,用于治疗血脂异常,可诱导SA-β-gal-阳性软骨细胞凋亡。 这一发现促使作者研究了OA情况下的PPARα表达,他们发现OA患者的血液和膝关节软骨中的PPARα表达降低了。激活sirtuins的类黄酮(如非瑟酮),与长寿相关并抑制骨关节炎软骨细胞中IL-1β所诱导的炎症。非瑟酮目前正处于评估其减轻软骨衰老,减轻OA症状的功效的临床试验阶段。
Senolytics治疗在OA中相关的应用问题
尽管用药理学方法治疗老年相关疾病看起来很有前途,但潜在的副作用和药物效力的差异仍然令人担忧。关于关节疾病的治疗,目前尚不清楚用Senolytics促进细胞死亡是否会损害骨性关节炎患者的组织完整性,加剧软骨和骨丢失。有趣的是,用表达蛋白多糖4(也称为浅表区蛋白多糖)的细胞产生的白喉毒素杀死小鼠关节软骨浅表区软骨细胞,并没有引起进一步的软骨损伤。事实上,浅表区软骨细胞的死亡似乎改善了手术破坏内侧半月板后的损伤结果。作者提出,在关节损伤后,来自完整软骨细胞的分解代谢,而不是软骨细胞死亡,进一步导致软骨丢失。鉴于衰老是外伤性骨关节炎的一个特征,这一证据表明,用Senolytics杀死衰老软骨细胞可能有助于防止由衰老软骨细胞分泌的SASP因子引起的损伤性的软骨丢失。因此在年龄相关性骨关节炎患者中开展类似的研究,对于确定诱导细胞死亡后软骨维持长期稳态的能力至关重要。
在OA策略中使用Senolytics的另一个考虑是,尽管有大量证据表明细胞衰老是衰老和疾病病理的驱动因素,但一些研究表明衰老在各种生理过程中有有益作用,包括组织重构和伤口愈合。例如,发现在蝾螈的肢体再生的中间阶段衰老被诱导。截肢后,衰老细胞在发育中肢体的软骨和肌肉中积累,但随后在完全再生前被巨噬细胞自然清除。另一项研究发现,清除巨噬细胞会阻碍衰老细胞的清除,并阻碍再生。重要的是,截肢后衰老的细胞比例不受年龄的影响,表明衰老在组织修复中起着不依赖年龄的作用。虽然还需要对这一概念进行更多研究,但本研究的作者假设,对衰老细胞进行有效的免疫监测可能允许巨噬细胞被招募到受损组织区域,这对再生是必要的。在小鼠的一项研究中,衰老的成纤维细胞和内皮细胞被发现聚集在皮肤伤口附近,并通过分泌血小板来源的生长因子AA (PDGF-AA; 即PDGF由两个A亚基组成),诱导成肌成纤维细胞分化。本研究提示,SASP分泌的生长因子和重构酶可能有助于促进细胞生长,从而促进组织再生和伤口愈合。因此,还需要更多的研究来确定,大规模消除关节中的衰老细胞是否会导致进一步导致骨性关节炎组织损失。
Senomorphics
Senomorphic候选药物概述。以炎症和疾病相关的通路和分子为治疗靶点并不是一个新策略,大量的Senomorphic候选物已经被证明可以抑制与SASP相关的途径,而不会诱导细胞凋亡。这些Senomorphic候选包括IκB激酶抑制剂和NFκB(比如NEMO-binding domain peptides)、酪氨酸蛋白激酶抑制剂JAK(如ruxolitinib)、ATM抑制剂(如KU- 60019)、Rogerin-lamin A/C蛋白封闭化合物(如JH4),活化剂PDGF和纤维母细胞生长因子信号(例如胚胎干细胞条件培养基), TGFβ受体2型抑制剂和p21(如Mmu-mir-291-A-3-p)等等。考虑到SASP因子的表达与OA样病理的相关性,抑制这些因子是一种有吸引力的治疗方法。然而,选择正确的靶点是保证治疗疗效和特异性的必要条件。
细胞因子抑制。在软骨中,TNF与其他SASP因子(如IL-1β)结合,刺激了损伤性MMPs的产生并抑制组织修复。TNF或IL-1抑制OA的临床试验并未取得理想的结果。例如,在临床II期试验中对患有膝盖OA和滑膜炎的患者使用Lutikizumab(il-1α和il-1β的双重抑制剂)治疗,对疼痛的缓解非常有限并且也没有改善滑膜炎。对炎性手部OA患者服用依那西普(TNF抑制剂)治疗未能缓解疼痛并对关节变形只有有限的影响。然而,最近对一项试验数据的探索性分析发现,该试验旨在检查抗IL-1β抗体Canakinumab对高危人群(即先前有心肌梗塞和C反应蛋白升高的患者)的心脏疾病病发事件的疗效。发现Canakinumab治疗组的膝关节和髋关节置换发生率低于安慰剂对照组。
IL-6与类风湿关节炎(RA)的发病机制有关,IL-6受体抑制剂Tocilizumab在RA的临床治疗中是有效的,目前正处于手OA的III期试验中。虽然RA是一种自身免疫性疾病,但它与OA有共同的特征,包括释放促炎细胞因子和软骨基质降解。然而,令人惊讶的是,IL-6敲除小鼠在生理衰老反应中比野生型小鼠表现出更严重的OA,这表明OA发病机制复杂,需要多方面的治疗方法。
靶向MMPs(基质金属蛋白酶)。 MMPs是另一类SASP因子,由于其已知的对软骨的分解代谢作用,而被视为药物干预的靶点。具体而言,MMP13是结缔组织中表达量最高的MMP,也是关节软骨中用于降解II型胶原的最特异的酶。研究发现,来自OA患者的人软骨细胞表达的MMP13水平高于来自健康软骨捐赠者的软骨细胞。此外,MMP13在转基因小鼠出生后过表达诱导了OA样关节炎,暗示MMP13是OA发病的主要驱动因素。在另一项研究中,软骨细胞特异性的MMP13缺失减轻了半月板韧带损伤(MLI)引起的OA的严重程度。为了测试Senomorphics对OA进展的影响,研究人员还在MLI后用CL82198治疗野生型小鼠,CL82198是MMP13选择性抑制剂。CL82198治疗降低了OA严重程度,增加了II型胶原水平,并且抑制了软骨细胞死亡。
综上所述,这些数据表明,通过Senomorphics抑制SASP因子可能是一种有前途的治疗OA的方法。然而,需要更多的研究来准确确定哪些SASP因子促进了OA病理,以及它们的抑制是否减缓或阻止了疾病的进展。
结 论
有证据表明关节组织中的细胞衰老是OA发病和进展的主要驱动因素,但需要进一步的研究来确定衰老导致特定疾病表型的确切机制。最可能的是,随着时间的推移衰老细胞的积累将机体衰老、细胞衰老和OA病理联系在了一起,加上细胞代谢、形态和功能的逐渐改变,所有这些都导致关节组织稳态和完整性的丧失。有效的OA治疗策略需要首先建立驱动细胞生理变化的潜在机制,然后针对这些机制设计治疗方案。
此外,常用的用于识别衰老的生物标志物不足以诊断OA。SA-β-gal染色不一定是软骨细胞衰老的指标,可以受到自噬和溶酶体功能改变的影响,这两种功能在OA中都降低了。此外,软骨细胞中p16的表达在SASP或OA发病机制中不是必需的。因此,针对参与OA的细胞进行靶向治疗时,应考虑使用其他的生物标志物来确保特异性,防止意外的影响。最近的证据表明,软骨细胞衰老和OA与EVs及其分泌的变化有关。因此,EVs以及uPAR表达(衰老软骨细胞表达)应进一步研究,以确定它们是否是关节疾病的准确临床标志物。
关节组织衰老是由一些与压力相关的通路引起的,因此抑制炎性细胞因子或选择性地消除衰老细胞并保证健康细胞安然无恙的技术是一种非常吸引人的抗衰老策略。然而,尽管使用Senolytics的临床证据和Senomorphics治疗OA表型看起来前途无量,但这些方法尚未显示出消除或预防这种疾病的有效性。此外,尽管SASP抑制剂,如CL82198,已被证明能有效减轻小鼠创伤后OA的严重程度,但同样的效果尚未在老年或患病的软骨细胞和其他人类滑膜关节细胞得到证明。
此外,这些疗法从实验室到临床的进展受到无法证明是否存在某种特定的细胞类型作为OA的主要驱动因素的阻碍。软骨细胞、滑膜成纤维细胞、骨细胞,可能还有其他尚未被研究的关节组织细胞,都能衰老并向关节环境分泌SASP因子。如果不知道哪些细胞负责哪种OA表型,疾病治疗的药物特异性将很难评估。
最后,还需要进一步研究杀死或改变器官中衰老细胞的潜在有害影响。最近的研究表明,衰老细胞通过招募巨噬细胞促进早期伤口愈合和组织再生。即使衰老细胞导致骨关节炎损伤后的进展,过早消除这些细胞或阻止旁分泌信号可能会阻止受损软骨和其他组织的初始愈合,这可能会对整个关节造成毁灭性的后果。因此,使用Senolytics和Senomorphics的研究必须包括对不同治疗时间的疾病结果的比较,以确保可以正确地预测药物疗效。
 来源:老顽童说
来源:老顽童说原标题:《【重磅综述】骨关节炎中细胞衰老的机制和治疗》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




