- +1
【科技前沿】周钢桥/贺福初合作揭示新的肝癌癌基因RRS1
我国是肝癌(Hepatocellular cancer, HCC)高发国家,每年新发病例约50万,约占全球肝癌新发病例的半数以上。近年来生物医学和技术的发展显著促进了肝癌的防诊治水平,但肝癌患者的总体生存率和预后仍不理想。机体生命周期内基因组变异的持续累积是肝癌发生发展的重要原因。其中,体细胞的拷贝数变异(Copy number alteration, CNA)是基因组变异的一种重要类型。迄今已发现数十个肝癌相关的CNA;然而,这些CNA(例如染色体1q和8q的拷贝数扩增、8p和17p的拷贝数缺失等)常常跨越较大的基因组区域,可影响数十甚至数百个基因的表达变化,因而给鉴定其中的肝癌致病基因(包括癌基因或抑癌基因)带来了极大的挑战【1】。
20210年8月26日,军事科学院军事医学研究院辐射医学研究所周钢桥研究员与该院生命组学研究所贺福初院士团队合作在Science Advances杂志上发表了题为 Genomic gain of RRS1 promotes hepatocellular carcinoma through reducing the RPL11-MDM2-p53 signaling 的研究论文,在发生拷贝数扩增的染色体8q区域发现了一个新的肝癌癌基因——核糖体生物合成调节因子RRS1(Ribosome biogenesis regulator 1 homolog),并揭示该基因通过抑制RPL11-MDM2-p53信号转导通路促进肝癌的发生发展【2】。

研究人员首先通过370例肝癌患者癌组织的拷贝数变异图谱和转录组数据的整合分析,揭示了拷贝数变异在全基因组水平存在广泛的顺式和反式调控作用。其中,发现染色体8q区域的拷贝数扩增呈现最强的反式调控效应,并且与“核糖体生物合成”功能显著相关。在染色体8q区域存在多个与核糖体生物合成相关的基因;然而,其中的RRS1基因尤为引人注意,它的基因组拷贝数扩增不但与核糖体生物合成的活性显著正相关,而且与p53通路的活性呈显著的负相关性。通过随后的细胞学实验发现,RRS1可显著促进肝癌细胞的细胞周期进程、抑制细胞凋亡,进而促进细胞的生长和克隆形成能力;裸鼠成瘤实验也证实,RRS1可显著促进肝癌细胞的在体成瘤能力。进一步的临床相关性分析发现,RRS1在肝癌组织中显著上调表达,且其高表达与肝癌患者更高的谷丙氨酸转氨酶(Alanine transaminase, ALT)水平以及不良预后显著相关,特别是在p53基因野生型的肝癌患者中。
以往研究已发现,若核糖体的生物合成过程发生紊乱,细胞将会产生应激反应,导致某些核糖体蛋白(Ribosome protein, RP)从核仁穿梭到核质,结合E3泛素连接酶MDM2,从而竞争性抑制MDM2对p53的泛素化降解,最终激活p53信号转导通路【3】。2018年,周钢桥/贺福初团队合作曾在Gastroenterology杂志发表论文(周钢桥/贺福初团队发现新的非编码RNA是肝癌易感基因并揭示相关调控机制),报道了一个发挥肝癌癌基因作用的小核仁RNA(Small nucleolar RNAs, snoRNA)——SNORA18L5(snoRNA H/ACA box 18-like 5),它可显著促进核糖体RNA(rRNA)的成熟和核糖体的生物合成进程,缓解核糖体应激压力,阻滞核糖体蛋白RPL5和RPL11的核仁-核质易位,从而促进MDM2介导的p53蛋白泛素化降解【4】。
在本研究中,研究人员同样发现在肝癌细胞中RRS1的高表达可显著促进rRNA的成熟和核糖体亚基的组装,从而缓解核糖体应激反应的压力。进一步的机制研究发现,RRS1(与RPF2一起)可与RPL11相互作用并将其锚定在核仁中,从而解除RPL11对MDM2-p53相互作用的竞争性抑制作用,促进MDM2介导的p53蛋白泛素化降解,最终下调p53通路的活性。这些科学发现揭示了核糖体生物合成调节蛋白RRS1的新功能,再次将癌细胞中核糖体生物合成的稳态调节与RPs-MDM2-p53信号转导通路耦联在一起。
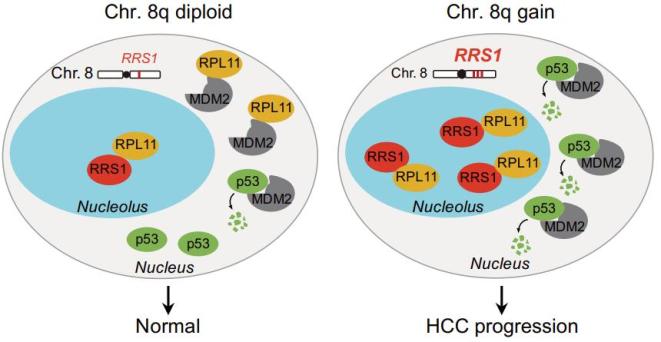
RRS1的作用机制示意图
总之,该研究通过肝癌组织的基因组拷贝数变异图谱和转录组的整合分析,以及系统的功能和分子机制研究,在染色体8q区域发现和揭示了一个受基因组拷贝数扩增驱动的新的肝癌癌基因RRS1,它可通过影响核糖体生物合成的稳态而下调RPs-MDM2-p53信号转导通路活性,从而促进肝癌的发生发展。这些科学发现不但有助于我们深入了解肝癌的致病机制,也为肝癌的诊治和预后预测等潜在的临床应用提供了新的候选靶标。
军事科学院军事医学研究院辐射医学研究所周钢桥研究员和生命组学研究所贺福初院士为论文的共同通讯作者;辐射医学研究所曹鹏博副研究员、杨爱清助理研究员和李佩尧博士研究生为论文的共同第一作者。
原文链接:
http://doi.org/10.1126/sciadv.abf4304
参考文献
1. Cancer Genome Atlas Research Network. Comprehensive and integrative genomic characterization of hepatocellular carcinoma. Cell. 2017;169(7):1327-1341.
2. Cao P, Yang A, Li P, et al. Genomic gain of RRS1 promotes hepatocellular carcinoma through reducing the RPL11-MDM2-p53 signaling. Science Advances. 2021;7(eabf4304).
3. Zhang Y, Lu H. Signaling to p53: ribosomal proteins find their way. Cancer Cell. 2009;16(5):369-377.
4. Cao P, Yang A, Wang R, et al. Germline duplication of SNORA18L5 increases risk for HBV-related hepatocellular carcinoma by altering localization of ribosomal proteins and decreasing levels of p53. Gastroenterology. 2018;155(2):542-556.
本文转载自公众号“BioArt”(BioGossip)
中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】周钢桥/贺福初合作揭示新的肝癌癌基因RRS1》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




