- +1
新冠特效药争相上市,能否为疫情带来新的转机
原创 核真录 核真录
第一百九十九期
文稿 | 南大新传未来编辑部·核真录 学生
高雅儿 王竞翊 王亦千 袁佳琪
编辑 | 史书晓 林歆瑶
制图 | 史书晓
排版 | 邬思存
前言
奥密克戎(Ormicron)变异株的扩散使世界新冠疫情防控形势再一次紧张起来。自2021年11月上旬南非发现首例奥密克戎确诊病例以来,这种变异毒株在各个国家攻城略地,成为南非、博茨瓦纳以及英美部分城市的主要流行株,已蔓延到至少121个国家和地区。据新华社2021年12月29日电,在当天世界卫生组织召开的新闻发布会上,总干事谭德塞称,奥密克戎与德尔塔同时流行将导致病例“海啸”般激增,并将继续给疲惫不堪的卫生工作者和濒临崩溃的卫生系统带来巨大压力,再次扰乱人们的生活和生计。
面对又趋严峻的疫情,几款新冠特效药的上市和研发进展受人关注。
2021年12月8日晚,国家药监局官网消息显示,我国首个自主知识产权新冠病毒中和抗体联合治疗药物获批。这也是我国第一个全自主研发并经过严格随机、双盲、安慰剂对照研究证明有效的抗新冠病毒特效药。

我国首个新冠治疗特效药出现
(图片来源:国家药监局官网)
而早在2021年11月份,默沙东公司(MSD)[1]与Ridgeback Biotherapeutics公司合作开发的口服抗病毒小分子药物莫努匹韦(Molnupiravir)就已在英国上市,成为全球首个获批上市的新冠口服药物,引发了全球关注。
与注射类药物等治疗手段相比,口服药物在许多人眼中意味着轻便、快捷与家常。那么,默沙东口服新冠特效药到底是什么?它的疗效如何?两个多月过去了,它的疗效是否真如当初官方披露的那么神奇?近期全球范围内还有哪些受人瞩目的新冠特效药?
本期核真录将为您梳理第一个新冠口服药莫努匹韦的疗效和上市情况,以及其他“知名”新冠特效药的研发成果。
莫努匹韦是什么?真有“特效”吗?
莫努匹韦是什么?据默沙东官网公布的资料显示,莫努匹韦是一种核糖核苷类似物,可抑制新冠肺炎病原体SARS-CoV-2的复制。它可以与新冠病毒的RNA聚合酶结合,在新合成的RNA分子中引入错误的核苷酸,使病毒的RNA出现错误,从而丧失毒性或被杀死。
简单来说,莫努匹拉韦的作用原理是将自己“伪装”起来,将“错误”传播到病毒的整个基因组中。

(图源:默沙东官网)
那么,莫努匹韦对新冠病毒的疗效如何呢?
我们先来看看默沙东官方发布的莫努匹韦的实验数据。
药品的临床试验往往要经过I、II、III、Ⅳ期(上市后)临床试验,其中III期阶段是药品上市前最重要的阶段。而莫努匹韦的III期实验中期数据显示该药物的疗效良好,这也是默沙东向美国食品药品监督管理局申请紧急授权的契机。
默沙东官网2021年11月4日公布的III期临床试验中期数据显示,莫努匹韦可将患者的住院或死亡风险降低约 50%。该实验在全球范围内23个国家进行,拉丁美洲、欧洲和非洲的被试者分别占研究人群的 56%、23% 和 15%。
实验又是如何实施的呢?临床试验将被试者分为两组,其中实验组投用莫努匹韦,对照组投用安慰剂。实验计划招募1550名轻症至中症的高危、非住院、未接种疫苗的成年患者,此次公布的中期报告分析了其中775名患者的数据。
在随机分组后的第 29 天,口服安慰剂治疗的患者中有14.1%住院或死亡,而口服莫努匹韦治疗的患者中这一比例仅有7.3%;其中,口服安慰剂的患者中有 8 人死亡,而口服莫诺匹韦治疗的患者没有死亡报告。另外,约40%的被试者具有病毒测序数据,他们的实验结果显示,莫努匹韦对于新冠病毒的Gamma、Delta 和 Mu变体都表现出一致的疗效。

莫努匹韦III期临床试验部分中期数据一览
对于莫努匹韦III期临床试验中期数据,默克公司首席执行官兼总裁Robert M. Davis曾表示:“凭借这些令人信服的结果,我们乐观地认为,莫努匹拉韦可以成为一种重要的药物,作为全球抗击新冠病毒大流行努力的一部分,并将增加默克公司的独特遗产,在最需要的时候在传染病方面取得突破。”
与此同时,Ridgeback Biotherapeutics首席执行官Wendy Holman表示:“我们对中期分析的结果感到非常鼓舞,并希望莫努匹韦如果被授权使用,可以在控制新冠疫情方面产生深远的影响。”

默克公司首席执行官兼总裁对莫努匹韦III期临床试验中期数据表示满意并给予厚望
(截图来源:默沙东官网)
然而,最新试验数据显示,默沙东新冠特效药并不像III期临床试验中期数据中所表现得那么“令人鼓舞”。美国东部时间2021年11月26日上午6:45,默沙东官网更新了有关莫努匹韦的研究数据。更新数据显示,在参与试验的1400多名患者中,莫努匹韦将住院或死亡风险从安慰剂组的 9.7% (68/699) 降低至莫努匹韦组的 6.8% (48/709),绝对风险降低了 3.0%,相对风险了降低30%。安慰剂组报告了9例死亡,莫努匹韦组报告了1例死亡。与莫努匹韦的III期研究中期分析相比,它的药效显著下降了。
莫努匹韦被哪些国家引进?定价如何?
尽管时间证明,莫努匹韦的药效前后有所差距,但基于2021年11月4日的III期临床试验中期数据,再加上11月前后各国媒体的造势,莫努匹韦早就已经向被疫情困扰的各个国家递出了橄榄枝,试图成为“全球抗击新冠病毒大流行努力的一部分”。
那么,至今为止,有哪些国家已经引进了莫努匹韦?
首先,莫努匹韦需要经过各国药品管理部门的审查,获得正式授权之后才能够在该国上市。
截至目前,该药物已获得英国药品和保健产品监管局(MHRA)正式授权,在英国上市,在美国通过了紧急申请使用授权(EUA)[2]申请,在日本仍处于审查阶段。
2021年11月4日,默沙东(MSD)与Ridgeback Biotherapeutics公司宣布,英国药品和医疗产品监管署 (MHRA)已经授权在英国使用该公司的口服抗病毒小分子药物——莫努匹韦,治疗轻度至中度且至少有一个指标指向重症风险的COVID-19成人患者,成为全球首款新冠口服药。据默沙东官网透露,英国政府已购入48万疗程的药品。

(英国已经购入48万疗程药品 图源:默沙东官网)
与此同时,这两家公司已经向美国食品和药物管理局(FDA)、日本医药品医疗机器综合机构(PMDA)提交紧急使用授权申请(EUA),审查通过后将执行先前的订购协议。美国政府先后宣布共购买310万疗程药品,日本政府购买大约160万疗程药品。
其中,FDA在2021年12月22日通过了莫努匹韦的紧急使用授权申请(仅在疫情爆发期间有效),用于治疗SARS-CoV-2病毒检测阳性且进展为严重COVID-19的高风险的成年人,以及不适合或用不了FDA授权的其他的COVID-19治疗方案的人。
此外,据默沙东集团官网显示,默沙东已与30多个国家的政府签订了莫努匹拉韦的预购和供应协议。但经过核查发现,各国政府购入的合同报价并不相同。据BBC新闻2021年11月4日报道,英国政府尚未披露其48万疗程的莫努匹韦初始合同报价。但据美国政府预购170万个疗程花费大约12亿美元可以推算,单个病人一疗程(5天,一天服药2次)约为700美元,约相当于人民币4482元。
默沙东集团宣称,莫努匹韦的定价将依照世界银行国家收入标准采取分级定价方法,各国政府购入莫努匹韦的实际价格必然存在差异。
中国能买到莫努匹韦吗?
如此看来,默沙东正在努力向各个国家推广莫努匹韦的使用,那么中国也在它的名单之中吗?在中国能买到这款新冠口服药吗?经核真录核查,答案是否定的。
2021年10月27日,默沙东公司将新冠口服特效药莫努匹韦的专利授权给药品专利池(MPP)。这意味着,其他仿制药企可以通过药品专利池申请获得莫努匹韦的专利实施许可,生产并向中低收入国家销售莫努匹韦。
根据协议公布的可销售莫努匹韦的国家的名单,此次共有105个中低收入国家被纳入其中,包括阿富汗、老挝、越南等国。但中国并不在名单之列,这表明中国生产商虽然可以向MPP申请莫努匹韦的专利实施许可,但生产的莫努匹韦只能销售给协议中的105个中低收入国家,而并不能在国内销售。也就是说,目前中国不能买到莫努匹韦。

(被授权的105个国家列表 图源:MPP官网)
此外,在与MPP达成协议之前,默沙东已经与五家印度制药商达成双边许可协议,授权这五家印度制药商生产并向104个国家销售莫努匹韦。
除了莫努匹韦,还有哪些新冠特效药?
在全球范围内,除了莫努匹韦,还有不少新冠治疗药物已上市或在研发中。核真录整理了目前广受关注的三种新冠药物的具体情况,其中有两种是中国研发的。
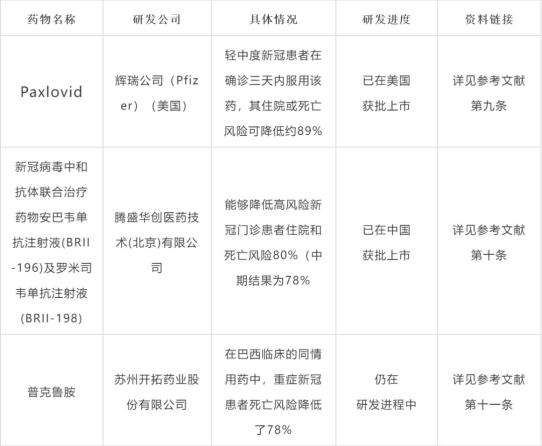
Paxlovid
2021年11月5日,辉瑞公司(Pfizer)公布了其研发的新冠口服药物Paxlovid的三期临床研究结果,显示轻中度新冠患者在确诊三天内服用该药,其住院或死亡风险可降低约89%。
中期分析显示,与安慰剂相比,在症状出现3天内接受治疗的患者中,住院或因任何原因死亡的风险降低了 89%。
Paxlovid的表现可以媲美新冠中和抗体的治疗效果,也显著优于前几日在英国获批上市的默沙东公司研发的广谱抗病毒药物莫努匹韦(Molnupiravir)。这一消息引起了人们的广泛关注,有媒体称Paxlovid为对付新冠感染的“银色子弹”(silver/magic bullet)。
据美国食品和药物管理局(FDA)当地时间2021年12月22日消息,辉瑞公司的口服新冠药“Paxlovid”已获批上市,成为了美国首个获得正式授权的口服抗新冠病毒药物。

Paxlovid已在美国获批上市(截图来源:FDA官网)
然而,面对新冠病毒最新的变异株——奥密克戎的快速传播,德国华裔病毒学家、埃森大学教授陆蒙吉在接受《中国新闻周刊》采访时认为,这两款小分子抗新冠药物(Paxlovid和莫努匹韦)不能随意使用,因为新冠病毒突变和进化能力非常强,如果这两种药物广泛投入使用,又不能完全地阻止病毒复制,在很短的时间内就可能会出现耐药的毒株,从而导致治疗效果下降,甚至完全失效。
新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)
2021年12月8日,由清华大学医学院教授、清华大学全球健康与传染病研究中心与艾滋病综合研究中心主任张林琦领衔研发的新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法(此前称BRII-196/BRII-198联合疗法)获得中国药品监督管理局(NMPA)的应急批准上市,用于治疗新型冠状病毒(SARS-CoV-2)检测结果为阳性,同时伴有进展为重型COVID-19危险因素的成人和青少年(≥12岁,体重≥40 kg)患者。
此次获批是基于美国国立卫生研究院(NIH)支持的ACTIV-2的3期临床试验,包括847例入组患者的积极中期及最终结果。最终结果显示,与安慰剂相比,安巴韦单抗/罗米司韦单抗联合疗法能够降低高风险新冠门诊患者住院和死亡风险80%(中期结果为78%),具有统计学显著性。
仅不到20个月的时间,清华大学与深圳市第三人民医院及腾盛博药合作,将安巴韦单抗/罗米司韦单抗联合疗法从最初的中和抗体分离与筛选迅速推进到完成国际3期临床试验,并最终获得中国的上市批准。这一成就是中国与全球一流的科学家和临床研究人员共同努力的成果,包括支持ACTIV-2国际临床研究的美国国立卫生研究院(NIH)下属的美国国家过敏和传染病研究所(NIAID)、以及领导ACTIV-2临床研究的艾滋病临床试验组(ACTG)。
普克鲁胺
在全球已获批或研发进展较快的四款新冠药物中,有两个由国内医药公司开发。除了已获批的安巴韦单抗注射液(BRII-196)及罗米司韦单抗注射液(BRII-198)外,还有一家中国创新药企——苏州开拓药业的普克鲁胺也占据一席之地。该药前期在巴西开展的三项临床试验初步表明,普克鲁胺对新冠肺炎轻中症非住院和住院患者具有较好疗效,将重症患者死亡风险降低78%。目前,普克鲁胺正在中国、美国、巴西开展国际多中心III期临床试验。
对于与辉瑞和默沙东药物对比,苏州开拓药业创始人、董事长兼CEO童友之认为,“普克鲁胺的优势不仅仅在防止轻症转为重症上,更重要的是对重症患者的保护率。在巴西临床的同情用药[3]中,重症新冠患者死亡风险降低了78%,这个数据是令人振奋的。”
结 语
新冠特效药的出现,是否能使对新冠病毒的治疗“日常化”“流感化”?就目前核真录核查到的情况看来,距离让新冠特效药“飞入寻常百姓家”的目标依旧有很长的路要走。新冠药物的实际药效、药物分配、生产成本、最终定价等等,还有很多不确定因素。
据美国有线电视新闻网(CNN)报道,抗病毒口服药可能是“游戏规则改变者”。但至少在药物供应初期,新冠疫苗的作用仍不可取代。英国政府网站在公布莫努匹韦获批消息时特意指出,它不能作为新冠疫苗的“替代品”使用。
中国科学院广州生物医药与健康研究院特聘研究员陈凌在接受新华社采访时指出,疫苗和药物是互补的“组合拳”关系:疫苗不是所有人都可接种,其保护效果和持久性尚不十分清楚;一部分先天免疫较差的人接种疫苗效果不好,药物可保护这些人;有了疫苗保护,最终需要用药的人会少很多,即便药物有一定副作用,从百分比来看,绝对数也不会很大;如能研发出更有效、保护更持久的疫苗,药物的使用会更加减少。
不过,毫无疑问,在抗击疫情的漫漫长征路上,新冠特效药的种种可能,已经让我们看到了新的希望。
注释:
[1] 默克公司(Merck)在美国和加拿大以外的地区被称为默沙东(MSD)。根据官网信息显示,此次参与莫努匹韦的研发为默沙东公司,因此核真录采用“默沙东”的说法。
[2]医药产品紧急使用授权(Emergency Use Authorization,EUA)指由美国食品药品管理局(FDA)在实际的或潜在的紧急状态下,对未获批准的医药产品的使用及已获批准产品的未获批准用途的授权。
[3]同情用药指对于患有严重或危及生命疾病的患者,在不能通过现有药品或入选临床试验来得到有效治疗时,可以申请在临床试验之外使用未经上市许可的试验用药物。
参考资料
1. 口服新冠特效药来了!我们能打败新冠病毒吗?:https://xw.qq.com/partner/vivoscreen/20211111A09LUR/20211111A09LUR00?isNews=1
2. 英国成为首个批准默沙东新冠特效药的国家:https://t.ynet.cn/baijia/31684693.html
3. Merck and Ridgeback’s Molnupiravir, an Oral COVID-19 Antiviral Medicine, Receives First Authorization in the World:https://www.merck.com/news/merck-and-ridgebacks-molnupiravir-an-oral-covid-19-antiviral-medicine-receives-first-authorization-in-the-world/
4. Merck and Ridgeback’s Investigational Oral Antiviral Molnupiravir Reduced the Risk of Hospitalization or Death by Approximately 50 Percent Compared to Placebo for Patients with Mild or Moderate COVID-19 in Positive Interim Analysis of Phase 3 Study:https://www.merck.com/news/merck-and-ridgebacks-investigational-oral-antiviral-molnupiravir-reduced-the-risk-of-hospitalization-or-death-by-approximately-50-percent-compared-to-placebo-for-patients-with-mild-or-moderat/
5. 默沙东集团官网关于莫努匹韦的搜索结果:https://www.merck.com/?s=Molnupiravir
6. https://www.bbc.com/news/health-59163899
7.《关于 FDA 咨询委员会投票支持口服抗病毒药物 Molnupiravir 用于高危成人轻度至中度2019冠状病毒疾病的研究》:https://interpreter.caiyunai.com/html/61ac2b8fc5fbe2c40066f3a8
8. MPP官网:https://medicinespatentpool.org/licence-post/molnupiravir-mol
9. 辉瑞官网:https://www.pfizer.com/news/press-release/press-release-detail/pfizers-novel-covid-19-oral-antiviral-treatment-candidate
10. 11. 央广网《中国新冠口服药提上日程表 普克鲁胺有望率先完成三期临床试验 重症死亡风险降低78%》:https://apicnrapp.cnr.cn/html/share.html?id=27737051
12. 新华网:《新冠口服药问世,就不用再接种疫苗?专家明确回应》http://www.news.cn/2021-11/14/c_1128062990.htm
13. 解放日报:首个新冠疫苗临床试验结果发表,来了解临床试验为何要分3期做?https://tech.sina.com.cn/roll/2020-05-23/doc-iircuyvi4655296.shtml
14. FDA官网《冠状病毒(COVID-19)更新:FDA授权第一种口服抗病毒药物治疗》https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-authorizes-first-oral-antiviral-treatment-covid-19
15. Countries in Asia are placing orders for a new drug to treat coronavirus. Poorer nations could miss out again. CNN
16. 新华社特稿:多款新冠口服药获进展 抗疫仍需“组合拳” :https://baijiahao.baidu.com/s?id=1716390270189718646&wfr=spider&for=pc
17. First oral antiviral for COVID-19, Lagevrio (molnupiravir), approved by MHRA
18. https://www.gov.uk/government/news/first-oral-antiviral-for-covid-19-lagevrio-molnupiravir-approved-by-mhra
19. 20. 世卫组织:奥密克戎和德尔塔毒株可能导致全球新冠病例“海啸”:http://www.news.cn/world/2021-12/30/c_1128216536.htm)
本文内容首发于《核真录》
原标题:《新冠特效药争相上市,能否为疫情带来新的转机》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




