- +1
【科技前沿】闫道广/钟文彬课题组揭示造血干细胞恶性转化的机制及髓性白血病治疗的新靶点
白血病(Leukemia)在儿科恶性肿瘤的发病率中居第一位,它的致死率在导致儿童及35岁以下成年人死亡的恶性肿瘤中排首位【1】。Leukemia是一类起源于造血干细胞的克隆性恶性疾病,但造血干细胞恶化机制多有未知【2】。
2022年1月26日,暨南大学生命科学技术学院闫道广/钟文彬课题组在Science Translational Medicine在线发表了题为 Loss of miR-31-5p drives hematopoietic stem cell malignant transformation and restoration eliminates leukemia stem cells in mice 的研究论文,揭示造血干细胞恶性转化的机制及髓性白血病治疗的新靶点。

该研究发现,相比于正常造血干细胞 (HSCs),miR-31-5p的表达在人类白血病干细胞(LSCs)中显著被抑制或无法检测到。在HSPC中抑制miR-31-5p可促进其靶基因FIH (factor inhibitor hypoxia inducing factor 1α,HIF-1α) 的表达,从而抑制HIF-1α信号通路;增加的FIH表达可导致HSCs的能量代谢模式由糖酵解转化为氧化磷酸化 (OXPHOS),进而增加了三羧酸循环中间代谢产物延胡索酸的丰度。延胡索酸的增加促进组蛋白的甲基化进而促进HSCs向LSCs的恶性转化,并B-NDG重度免疫缺陷小鼠中引发髓系白血病样疾病的发生。在白血病患者来源的异种移植小鼠模型中,联合化疗药物阿糖胞苷(Ara-C),使用G7聚 (胺) 纳米级树突状复合体包封的miR-31-5p,可消除LSCs并阻断急性髓系白血病 (AML) 的进程。这些结果显示HSCs通过改变能量代谢的模式恶化的机制,并为AML患者提供了一种潜在的治疗策略。
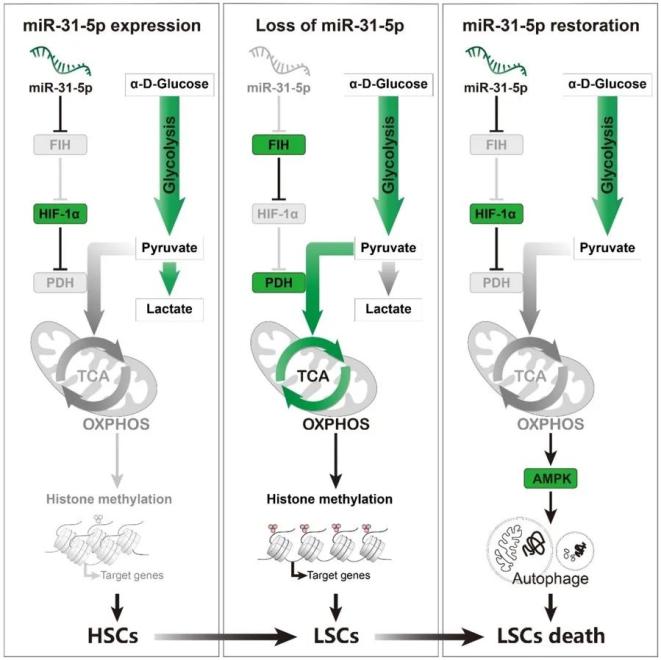
图1. miR-31-5p丢失导致HSCs恶化其恢复导致LSCs死亡
MicroRNA-31 (miR-31) 是位于染色体9p21.3区域的miRNAs,这一染色体区域在人类多种癌症中十分容易发生丢失【3】。为探究miR-31-5p在白血病中的功能,作者首先分析了miR-31-5p在HSCs和LSCs的表达,发现LSCs中miR-31-5p表达被显著抑制或无法检测到,并且其低表达与人类AML病人的生存期呈负相关性。
通过慢病毒介导的方式抑制miR-31-5p在HSCs中的表达,体外研究发现在这种HSCs中FIH的表达被上调,HIF信号通路和糖酵解途径关键酶的基因被抑制,这促使HSCs的能量供应模式由糖酵解途径转为氧化磷酸化途径。进一步分析发现miR-31-5p的抑制促进HSCs自我更新能力以及恶性转化能力。研究团队接下来将miR-31-5p被抑制的HSCs移植到B-NDG重度免疫缺陷小鼠体内,经过3个月左右的饲养,这种小鼠出现包括外周血白细胞增高、脾脏肿大、造血衰竭等严重的髓系白血病症状,证明miR-31-5p的抑制确实能诱导白血病的发生。通过荧光示踪技术,研究人员发现在小鼠体内miR-31-5p被抑制的HSCs表达多种LSCs的表面标记物,证明HSCs被直接转导为恶性LSCs。
为了拓展该发现在临床白血病治疗中的意义,作者构建了G7聚 (胺) 纳米级树突状复合体包封的纳米材料,在PDX动物中模型中,联合化疗药物Ara-C,该纳米药物能有效清除白血病干细胞并治愈部分疾病小鼠,显示出有效的抗白血病功能。
总的来说,应用动物模型、代谢组学、转录组学等技术手段,结合临床病例分析,这项研究从重构正常细胞的能量代谢出发,在实验层面阐明了HSCs恶变的驱动因素。LSCs被认为是白血病患者复发的主要原因。这项研究开发的纳米材料将为白血病尤其是复发性白血病患者带来新的治疗靶点和概念。
暨南大学博士后朱碧莹和副教授钟文彬等为该研究论文的共同第一作者,通讯作者为暨南大学闫道广教授。本研究在南方医科大学南方医院小儿血液肿瘤专科冯晓琴主任、广东省人民医院血液科杜欣主任鼎力协作下完成。
原文链接:
http://doi.org/10.1126/scitranslmed.abh2548
参考文献
1. H. Sung, J. Ferlay, R. L. Siegel, M. Laversanne, I. Soerjomataram, A. Jemal, F. Bray, Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 71, 209-249 (2021).
2. M. Yamashita, P. V. Dellorusso, O. C. Olson, E. Passegue, Dysregulated haematopoietic stem cell behaviour in myeloid leukaemogenesis. Nat Rev Cancer 20, 365-382 (2020).
3. M. Yamagishi, K. Nakano, A. Miyake, T. Yamochi, Y. Kagami, A. Tsutsumi, Y. Matsuda, A. Sato-Otsubo, S. Muto, A. Utsunomiya, K. Yamaguchi, K. Uchimaru, S. Ogawa, T. Watanabe, Polycomb-mediated loss of miR-31 activates NIK-dependent NF-kappaB pathway in adult T cell leukemia and other cancers. Cancer Cell 21, 121-135 (2012).
本文转载自公众号“BioArt”(BioGossip)
中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】闫道广/钟文彬课题组揭示造血干细胞恶性转化的机制及髓性白血病治疗的新靶点》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




