- +1
肺癌哪里跑!陈崇教授团队发现小细胞肺癌转移的表观遗传学重编程分子调控机制
原创 果壳硬科技 我是科学家iScientist
小细胞肺癌(SCLC)是一类恶性程度极高的神经内分泌肿瘤,发病率约占肺癌总数的15-20%,其5年生存率不到10%。SCLC的一个显著特征是具备极强的远端转移能力。SCLC作为人类肿瘤中转移能力最强的癌种之一,表观遗传学重编程在其转移和耐药中的功能研究甚少。
4月21日,Nature Cancer在线报道了四川大学华西医院生物治疗国家重点实验室陈崇教授团队的研究论文KMT2C deficiency promotes small cell lung cancer metastasis through DNMT3A-mediated epigenetic reprogramming,阐明了组蛋白甲基转移酶KMT2C缺失通过组蛋白-DNA协同低甲基化促进SCLC远端转移的表观遗传学机制,对SCLC治疗具有一定的理论意义。
 论文截图
论文截图表观遗传学重编程在肿瘤发生以及恶性进展过程中具有十分关键的调控作用。限制SCLC分子机制研究和新型药物研发的重要原因之一在于SCLC具有极强的远端转移能力。在诊断时,超过70%的SCLC患者都已经发生了转移,因而不能进行手术治疗,这也导致缺乏研究材料。
为此,陈崇教授团队创建了一类新型的“精准肿瘤模型”。团队利用最新的肺类器官培养、基因编辑和原位移植等技术,构建了原发、原位,并且驱动基因明确的SCLC小鼠模型。该模型与临床患者的病理特征、基因表达等高度相似,同时表现出广泛的侵袭转移能力。
基于SCLC模型,研究团队通过单细胞测序以及临床大数据协同分析,构建了SCLC转移的分子路径,发现KMT2C是一个关键的SCLC转移基因。
KMT2C,又叫MLL3,是组蛋白H3的4位赖氨酸1-、2-甲基转移酶,在多种人类肿瘤中高频突变。前期陈崇教授首次证明KMT2C在白血病中是一个单倍剂量不足的肿瘤抑制基因(2)。研究过程中,团队发现KMT2C的表达沿着SCLC的转移路径逐渐下调,并在有远端转移的SCLC患者中有更高频率的突变。研究团队利用体外类器官和小鼠体内功能学实验证明KMT2C的敲除显著地促进SCLC的进展和远端转移。
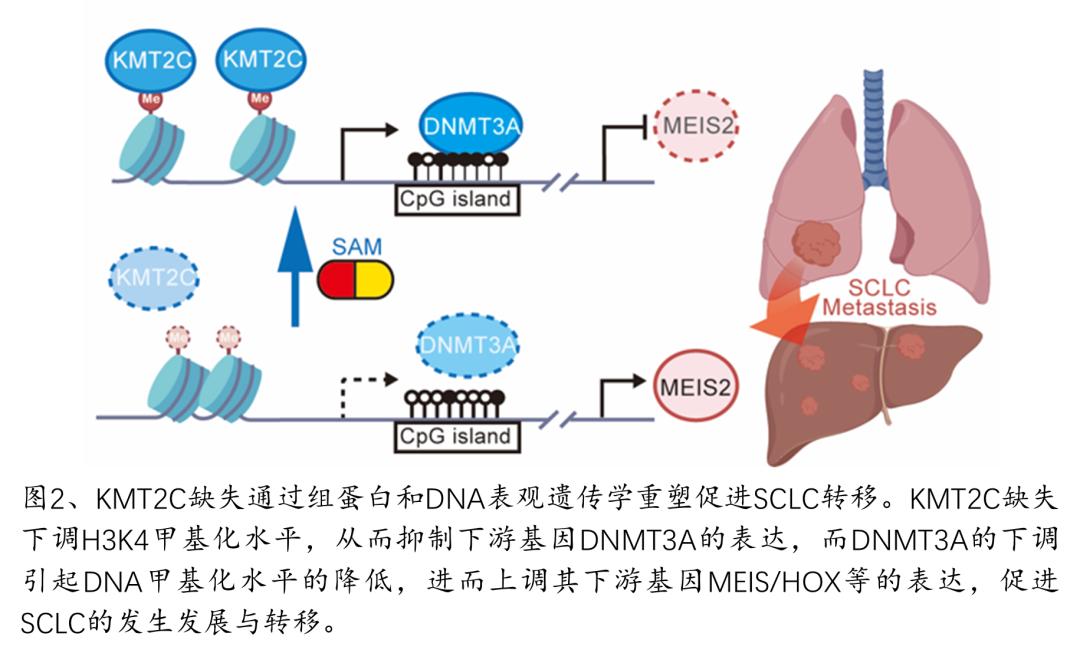
进而,团队利用表观遗传学相关的多组学联合分析和生物学功能研究,阐明了KMT2C通过直接调控DNMT3A表达对SCLC细胞表观遗传学重编程的分子机制。KMT2C缺失引起是组蛋白H3的4位赖氨酸1-、2-甲基化水平的显著下调,从而影响下游基因的表达。DNA甲基转移酶DNMT3A是KMT2C直接调控的下游基因之一。因而,KMT2C缺失的SCLC也呈现出显著的DNA低甲基化。而回补DNMT3A可以抑制KMT2C缺失SCLC的转移。值得注意的是,DNA和组蛋白甲基转移酶的共同底物S-腺苷甲硫氨酸(SAM)可以提高KMT2C缺失的SCLC中的DNA和组蛋白甲基化水平,从而显著抑制肿瘤的进展与转移。
 该工作的科学意义和创新性在于:
该工作的科学意义和创新性在于:1)研究团队利用肺类器官培养、基因编辑和原位移植等技术,构建了原发、原位、驱动基因明确的SCLC小鼠模型。
2)研究团队通过单细胞多组学技术、多种表观遗传学协同分析平台、临床大数据分析以及体内/体外的功能学实验,发现KMT2C是一个SCLC转移相关的关键基因。
3)阐明KMT2C缺失直接下调了DNMT3A造成了组蛋白-DNA协同低甲基化,对SCLC细胞的表观遗传学进行了重编程,从而促进SCLC远端转移发生的分子机制。
4)阐明SAM可以作为KMT2C突变SCLC患者的新型治疗方案,用于抑制肿瘤转移的发生和恶性进展。
研究团队期待KMT2C可以作为新的分子标记物为SCLC患者的临床诊断提供重要参考;也期望SAM可以作为一种新治疗方式以提高KMT2C突变患者的生存时间和生存质量。此外,团队自主构建的新型SCLC小鼠模型也将广泛地应用于SCLC的基础与转化研究。
参考文献
[1] Na F, Pan X, Chen J, Chen X, Wang M, Chi P, et al. KMT2C Loss Promotes Small Cell Lung Cancer Metastasis through DNMT3A-mediated Epigenetic Reprogramming. Nature Cancer. 2022:DOI : 10.1038/s43018-022-00361-6.
[2] Chen C, Liu Y, Rappaport AR, Kitzing T, Schultz N, Zhao Z, et al. MLL3 is a haploinsufficient 7q tumor suppressor in acute myeloid leukemia. Cancer Cell. 2014;25(5):652-65.
[3] Chen M, Chen X, Li S, Pan X, Gong Y, Zheng J, et al. An Epigenetic Mechanism Underlying Chromosome 17p Deletion-Driven Tumorigenesis. Cancer Discov. 2021;11(1):194-207.
[4] Liu Y, Chen C, Xu Z, Scuoppo C, Rillahan CD, Gao J, et al. Deletions linked to TP53 loss drive cancer through p53-independent mechanisms. Nature. 2016;531(7595):471-5.
[5] Zhang Q, Zhao L, Yang Y, Li S, Liu Y, Chen C. Mosaic loss of chromosome Y promotes leukemogenesis and clonal hematopoiesis. JCI Insight. 2022;7(3).
[6] Pan X, Wang J, Guo L, Na F, Du J, Chen X, et al. Identifying a confused cell identity for esophageal squamous cell carcinoma. Signal Transduct Target Ther. 2022;7(1):122.
作者:陈崇教授团队
编辑:酥鱼
排版:尹宁流
研究团队
通讯作者 陈崇:四川大学华西医院生物治疗国家重点实验室教授,博士生导师。1999年毕业于北京大学生命科学学院获学士学位,2009 年毕业于(美国)密歇根大学细胞与发育生物学系获博士学位。先后师从肿瘤免疫学家刘洋/郑盼教授(博士)和肿瘤学家、美国科学院院士Scott Lowe教授(博士后)。2014年起在四川大学华西医院生物治疗国家重点实验室与刘玉教授共同建立肿瘤研究实验室。主要研究方向包括:肺癌、食管癌、胃癌、膀胱癌等发生发展机制;类器官及精准肿瘤模型;肿瘤治疗靶标及新药研发;肿瘤转移及耐药机制等。作为(共同)第一或(共同)通讯作者已在国际学术期刊Nature、Nature Cancer、Cancer Cell、Cancer Discovery等发表研究论文40余篇,他引4,000余次。主持国家自然科学基金面上、优秀青年基金项目及国家重点研发计划重点专项子课题。
课题组主页
http://faculty.scu.edu.cn/chenchong/zh_CN/index/11459/list/index.htm
论文信息
发布期刊 《自然·癌症》 Nature Cancer
发布时间 2022年4月21日
论文标题
KMT2C deficiency promotes small cell lung cancer metastasis through DNMT3A-mediated epigenetic reprogramming
(DOI:https://doi.org/10.1038/s43018-022-00361-6)
原标题:《肺癌哪里跑!陈崇教授团队发现小细胞肺癌转移的表观遗传学重编程分子调控机制》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




