- +1
PCSK9抑制剂:降脂治疗应答不良的机制(一)
以下文章来源于脂在线 ,作者脂在线
脂在线.
聚焦脂代谢与动脉粥样硬化,追踪前沿科学动态,传递最新指南共识,陪您一“脂”学习。
PCSK9抑制剂:降脂治疗应答不良的机制
动脉粥样硬化性心血管疾病 (ASCVD) 是造成全球病死率升高的主要原因 [1]。动脉粥样硬化疾病的发生涉及多个风险因素,其中血脂异常是关键的独立的可改变的风险因素 [2]。血脂异常表现为胆固醇和甘油三酯(尤其是LDL-C)水平升高以及高密度脂蛋白胆固醇 (HDL-C) 降低 [3]。LDL-C水平升高被认为是动脉粥样硬化发生和发展的主要原因。因此,将ASCVD高危人群中的 LDL-C 设定为一个管理目标。2019年ESC/EAS血脂异常管理指南指出:对于极高危人群的一级预防和二级预防,LDL-C较基线降低≥50%并且<1.4 mmol/L(< 55 mg/dL) 。这种严格的降脂目标需要更精细的降脂策略,因为一些患者对高强度他汀类药物的耐受性较差,常因不良反应停药。近年来,前蛋白转化酶枯草溶菌素9(PCSK9) 抑制剂已成为一种有前景的治疗药物。依洛尤单抗(evolocumab)和阿利西尤单抗( alirocumab )这两种单克隆抗体 (mAb) 在被发现后不久被批准用于临床,不仅广泛应用于家族性高胆固醇血症 (FH) 的治疗,也广泛应用于 ASCVD 的二级预防。多项试验表明,PCSK9 mAb可使 LDL-C 平均降低约60%,各人口统计学亚组均得到临床获益 [4]。其他抑制 PCSK9 功能的治疗药物也在研发中,Inclisiran是一种小干扰RNA(siRNA),它可阻止 PCSK9mRNA 的翻译,使 ASCVD 或 ASCVD 同等风险患者的 LDL-C 降低49.2–53.8%[5]。然而,广泛的应用引起了人们对PCSK9抑制剂(PCSK9i)应答不良的临床关注,因为PCSK9 抑制剂在现实世界应用中报告的应答不良发生率相对高于大型随机临床试验 [6,7]。在此,主要基于文献和临床实践,我们回顾了 PCSK9 的生物学特性,并总结了 PCSK9 i应答不良的潜在机制。我们还提出了对策来识别和区分PCSK9i应答不良的患者,以改善需要降脂治疗的患者的预后。
一
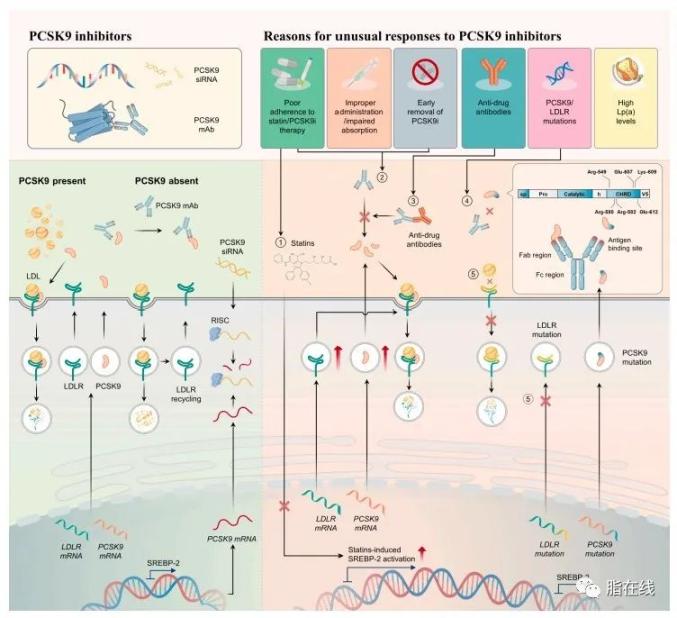
PCSK9抑制剂的作用机制
PCSK9介导的LDLR降解
LDL是极低密度脂蛋白 (VLDL) 的代谢副产物,LDL-C的血浆浓度是由富含甘油三酯的 VLDL 的肝脏分泌、VLDL向LDL 的外周转化和 LDL 清除之间平衡所致 [8]。肝脏 LDL 受体 (LDLR) 主要负责 LDL 清除 [9],通过受体介导的内吞作用清除血浆LDL。简言之,在中性 pH 值下,细胞外与 LDLR 结合的 LDL 在肝细胞中内化,然后释放到内体中,导致其随后的溶酶体降解 [9,10]。在酸性环境中,受体发生构象变化,形成闭合构象,促进 LDL 释放,并发出 LDLR 再循环到细胞表面的信号 [10]。LDLR在其 20 h 寿命内往返于细胞表面几百次 [9]。
人PCSK9 基因位于1号染色体的短臂上(条带p32.3)[11]。该基因编码一种非活性糖蛋白,该糖蛋白被激活并通过自身裂解过程从内质网释放到细胞外空间 [12]。PCSK9对脂质代谢的影响主要是通过影响肝脏 LDLR 的水平,从而增加血浆 LDL-C 浓度 [13]。在机制上,循环 PCSK9 与 LDLR 的表皮生长因子-A(EGF-A) 结构域结合 [12],PCSK9在胞内体 pH 值下以更高的亲和力与受体结合,这种结合导致 LDLR 从内体转运到溶酶体进行降解,而不是再循环到细胞表面 [14]。
PCSK9 的转录主要受固醇调节元件结合蛋白2(SREBP2;细胞胆固醇稳态的主要调节因子)调控。SREBP2还调节脂质代谢相关基因的表达,如 LDLR 和3-羟基-3-甲基葡糖-芳基辅酶 a 还原酶 (HMGCR)。内质网中低胆固醇含量促进 SREBP2 向高尔基体的转运,导致 SREBP2 的加工和随后靶基因的转录。相反,高胆固醇含量可阻断转运并抑制基因表达 [15]。他汀类药物抑制3-羟基-3-甲基-戊二酰辅酶 A 还原酶活性并限制胆固醇生物合成,从而激活 SREBP 并增加 PCSK9 转录 [16]。
在PCSK9 结构域中发现了至少250种突变 [17]。PCSK9序列变异体分为功能获得 (GOF) 和功能丧失 (LOF)。GOF突变患者的 LDL-C 水平高于无突变的患者,且风险增加 [18]。相比之下,LOF突变或基因缺失携带者的肝脏 LDLR 密度更高,LDL-C水平更低 [19,20]。LOF突变患者的 ASCVD 终生风险降低50-86%[20,21]。这一现象促进了PCSK9抑制剂的发展,用于那些追求更低的LDL-C靶目标时安全性问题更少的患者。
PCSK9抑制剂:一种降低LDL-C的新型药物
目前,两种全人源化mAb evolocumab和aliocumab,获批用于遗传性高胆固醇血症的患者或高危ASCVD患者,尤其是对他汀类药物不耐受或对高强度他汀类药物反应不佳的患者 [22-25]。这些 mAb 与 PCSK9 竞争性结合,并干扰 PCSK9-LDLR 复合物的形成,该过程可阻断 LDLR 降解,增加 LDLR 的再循环,并增强循环 LDL-C 清除率,从而降低血浆LDL-C [26]。
PCSK9mAbs 在很多具有相似 LDL-C 水平的患者中有效。mAbs单药治疗可使 LDL-C 水平降低50-55%[27-29],在他汀类药物不耐受的患者中报告了相似的降低 [30]。此外,mAbs在大多数 FH 患者中显示出令人满意的结果,尤其是在杂合子 FH(HeFH) 患者中 [31,32]。mAbs与其他降脂治疗(如他汀类药物或依折麦布)联用可进一步适度降低 LDL-C 水平 [26,33]。如上所述,他汀类药物可诱导 SREBP2 活化并增加循环 PCSK9 水平,该现象至少部分解释了 PCSK9i 降低 LDL-C 水平的“叠加”效应 [34]。
Evolocumab 和 alirocumab 在降低心血管疾病风险方面均可提供持久可靠的疗效。在 FOURIER 试验中,27,564例患者在他汀类药物治疗背景下随机接受 evolocumab 或安慰剂皮下给药 [35]。与安慰剂相比,Evolocumab治疗使 LDL-C 降低平均百分比为59%[35]。在中位随访2.2年,主要心血管事件 (MACE) 的相对风险降低了15%,这也显著降低了确诊 ASCVD 患者的心血管事件复发风险 [35]。关键次要终点(包括心血管死亡、心肌梗死或卒中)的风险降低了20%[35],该疗效在不同人口统计学亚组中一致[35,36]。ODYSSEY研究中阿利西尤单抗治疗急性冠脉综合征病史的患者得出了类似的结果[37]。治疗48个月后,LDL-C水平降低54.7%[37]。主要终点由冠状动脉性死亡、心肌梗死、缺血性卒中和需要住院的不稳定型心绞痛组成,中位随访2.8年后 MACE 的相对风险降低了15% [37],该治疗还使死亡风险降低16.2%[37],表明了使用更长时间的PCSK9 抑制剂在降低急性冠脉综合征后死亡率方面的潜在疗效[38]。
除注射部位反应外,两种 mAbs 具有相似的安全性特征。进一步分析显示,接受阿利西尤单抗和安慰剂治疗的患者之间神经认知障碍的发生率相似 [1,39]。
其他 PCSK9 抑制方法也在开发中, Inclisiran是一种化学合成的siRNA,与含有3个 N-乙酰半乳糖胺残基的配体共价连接。这些残基导致肝细胞特异性摄取siRNA,其中 inclisiran 与 RNA 诱导的沉默复合物 (RISC) 结合,并使 PCSK9mRNA分裂,从而抑制 PCSK9 合成。siRNA的持久作用允许每6个月给药一次,这种延长的给药间隔引起了人们的兴趣。在几个inclisiran 用于高胆固醇血症患者的临床试验中,LDL-C降低的中位水平也达到了50%[5]。在接受最大耐受剂量他汀类药物联合或不联合依折麦布治疗的 HeFH 患者中,与安慰剂相比,inclisiran使 LDL-C 水平进一步降低39.7%,并且除注射部位反应外,具有相似的安全性特征 [40]。
 二
二PCSK9抑制剂治疗的应答不良
应答不良的定义
随着PCSK9i在现实世界中的广泛应用,文献中报告的应答不良即低反应性(甚至无应答)病例越来越多 [6,41-44]。对降脂药物的低反应性定义为 LDL-C 降低 < 15%[6],这主要是基于药物批准所需的一般最低LDL-C降低。
LDL-C降低<15%的定义也应用于ODYSSEY阿利西尤单抗早期分析PCSK9i低反应性的研究中,3120例患者中的33例报告了低反应性 [6]。在这些试验中,使用 Friedewald 公式计算LDL-C,除非甘油三酯水平大于400mg/dL,在这种情况下,通过超速离心和沉淀的方法来定义LDL-C。PCSK9抑制剂的特殊获益和LDL-C降低的临床预期挑战了该定义。基于对 evolocumab 治疗后 LDL-C 降低个体间变异的深入分析,LDL-C水平相对于基线的中位降低百分比为66%。在他汀类药物治疗基础上加用 evolocumab 可使90%以上患者的 LDL-C 水平降低≥50%,99%以上患者的LDL-C水平降低≥30%[45]。定义低反应性为LDL-C降低<30%更合适,并且超过预期LDL-C降低平均值的两个标准差[45]。基于该更新定义,Warden等人[7] 根据直接测定的治疗中 LDL-C 水平,将对 PCSK9i 治疗的应答不良分为4类[7]:(1)无应答—所有时间点LDL-C均无明显降低;(2)应答延迟—第3次给药(PCSK9i开始后1个月)时未达到≥30%的 LDL-C 降低,但之后达到了该阈值。(3) 应答降低—所有时间点 LDL-C 降低 < 30%;(4)应答消失—第3次给药(PCSK9i启动后1个月)时 LDL-C 降低≥30%,但随后降低 < 30%。该更新显示应答不良患者的发生率增加,应答不良的发生率往往比临床试验中报告的至少高3倍[7]。尽管如此,延迟应答是异常反应人群中最常见的[7],这意味着在长期暴露于 PCSK9 抑制剂期间,大多数受试者的 LDL-C 降低超过30%,并且该组中经常发生相对较低的降低 (30-50%)[7],导致对 LDL-C 降低和 ASCVD 风险的作用减弱。
在评估对 PCSK9i 的治疗反应时,还需要考虑测量时间。药效学数据显示,在 mAb 单次给药后约14天观察到 LDL-C 降低峰值[46,47],并在2-3次给药后达到稳定降低 [48],这意味着假设每两周一次规律给药,4周后可达到 LDL-C 降低的稳态。在大多数临床试验中,在过夜禁食 10 h 后的早晨和研究药物给药前采集血样 [33,49]。在评价阿利西尤单抗每两周一次疗效的几项试验中,当在研究药物给药前测量 LDL-C 水平时,在第4周观察到显著的 LDL-C 降低[49]。Warden还使用在基线和 PCSK9i 治疗开始后1、6和12个月注射后5天内采集的血浆样本描述了结构化方案[7]。延长持续时间对于识别应答延迟或丧失的组至关重要。因此,评估 PCSK9i 疗效的第一个时间点应设定为治疗开始后约1个月,并应在第三次给药前或给药后采集样本[7]。建议进行长期随访,以区分延迟应答者和丧失应答者。然而,PCSK9i疗效评价的具体时间仍不清楚,需要进一步的临床验证。
参考文献:Mechanisms of unusual response to lipid-lowering therapy: PCSK9 inhibition. Clin Chim Acta. 2022 Nov 17;538:113-123.
“脂在线”平台由著名脑血管病专家王拥军教授发起,国家神经系统疾病临床研究中心-脂代谢与动脉粥样硬化中心承办,旨在建立以脂代谢与动脉粥样硬化性疾病为核心的临床科研学术交流平台。平台将聚焦脂代谢最新热点,分享国内外前沿资讯,解读血脂异常管理指南,通过整合多媒体视听资源,致力于更加便捷的知识共享。
致谢:赛诺菲医学部
排版:程爱春
原标题:《PCSK9抑制剂:降脂治疗应答不良的机制(一)》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




