- +1
Cell:冯越/Bondy-Denomy揭示噬菌体抑制和逃逸细菌CBASS免疫系统的分子机制
 生命科学
生命科学Life science
2023年2月6日,美国加州大学旧金山分校Joseph Bondy-Denomy教授课题组与北京化工大学冯越教授课题组合作在Cell Press细胞出版社旗下期刊Cell在线发表了题为“Bacteriophages inhibit and evade cGAS-like immune function in bacteria”的研究论文,报道了噬菌体抑制和逃逸细菌CBASS免疫系统的机制。
环状GMP-AMP合成酶cGAS是一种属于DNA传感器家族的酶,可以识别来自病原体等外来入侵者以及自身的DNA。在哺乳动物细胞中,环状寡核苷酸2’, 3’-cGAMP在干扰素基因刺激通路中起着至关重要的作用,cGAS产生的2’, 3’-cGAMP作为信号分子与STING(IFN基因的刺激因子)结合,随后诱导TBK1-IRF3依赖性地产生IFN-β,导致DNA驱动的免疫反应,根据信号强度的不同,STING也会进一步激活其他细胞过程,如细胞凋亡或坏死等[1]。近期,在细菌中也鉴定出了数千种名为CD NTase的cGAS样酶,这些酶在噬菌体感染期间通过未知机制被激活,并产生环状寡核苷酸以激活下游的效应蛋白,这种细菌免疫策略被定义为基于环状寡核苷酸的抗噬菌体信号系统(cyclic-oligonucleotide-based antiphage signaling system),简称为CBASS系统[2]。
CBASS系统是一种广泛存在于细菌和古细菌中的抗噬菌体免疫防御系统,由环状GMP-AMP合成酶 CD NTase和下游效应蛋白组成,这些效应蛋白可以通过细胞膜降解、噬菌体和宿主DNA的裂解、跨膜孔洞的形成及多种未知的作用方式杀死被噬菌体感染的细菌或抑制细菌生长,从而成功阻止噬菌体增殖。细菌通过CBASS系统介导的抗噬菌体感染的免疫防御又称“流产感染(或顿挫感染)”,这一过程涉及细菌从感应噬菌体到启动个体自杀,最终使细菌群体产生对噬菌体的免疫防御的分子机制。通俗而言,其本质是通过牺牲被噬菌体感染的部分细菌,从而保护其他细菌不被更多子代噬菌体感染。CBASS系统根据结构域的组成可分为四类,I型CBASS由一个紧凑的双基因系统组成,仅包含CD-NTase和效应器等核心基因,而在II型、III型和IV型 CBASS中还包含多种可调节CD-NTase活性的特性基因[3]。
噬菌体感染细菌后将遭遇细菌免疫系统的抵抗,但噬菌体同时也采用多种策略对抗细菌的免疫系统,目前研究最清楚的是噬菌体可编码多种蛋白质以抑制宿主免疫系统如CRISPR-Cas以及限制性修饰系统,但目前尚不清楚噬菌体是否有抑制或逃避CBASS免疫系统的机制。近期美国哈佛大学Philip J. Kranzusch课题组发现了一个由噬菌体编码的抗CBASS系统的磷酸二酯酶(命名为Acb1),Acb1与真核病毒编码的poxin酶相似,具有切割环状寡核苷酸的功能[4]。
CBASS系统的发现和研究标志着原核和真核生物免疫系统之间的联系,但在这一新兴领域中,关于噬菌体-宿主进化以及CBASS调控和激活机制的许多问题尚未解决,而内源性CBASS模型系统可有效地帮助这些问题的阐明。在本文中,Joseph Bondy-Denomy课题组通过生物信息学分析,共计筛选出252株不同的含有CBASS系统的P. aeruginosa菌株,使用CRISPR-Cas技术将其CBASS基因座敲除,最终筛选出一种具有天然功能性的CBASS免疫系统的菌株P. aeruginosa BWHPSA011 (Pa011)。该菌株含有cGAS样环状GMP-AMP合成酶CdnA,其可产生3’, 3’-cGAMP用以响应PaMx41噬菌体感染,从而激活磷脂酶(CapV)效应蛋白,发挥CBASS系统的免疫功能。而PaMx41噬菌体的逃逸突变体可产生一种抗CBASS系统的蛋白Acb2,那么Acb2如何发挥其抗性功能呢?冯越教授课题组结合生物化学、结构生物学等多种手段,阐明了Acb2抑制CBASS系统的功能机制。首先,他们通过体外生化实验发现Acb2可高效结合3’, 3’-cGAMP分子,但不具有酶活。冯越课题组解析了Acb2蛋白及其结合3’, 3’-cGAMP的复合物的结构,结构显示Acb2蛋白自身为一个紧凑的六聚体结构,其可结合3个3’, 3’-cGAMP分子,每个3’, 3’-cGAMP分子位于两个Acb2单体N端形成的“结合口袋”中(图1)。由于Acb2可以吸附并隔离3’, 3’-cGAMP,导致无法激活CBASS系统下游的效应蛋白,因此Acb2有效地破坏了CBASS系统的免疫作用。
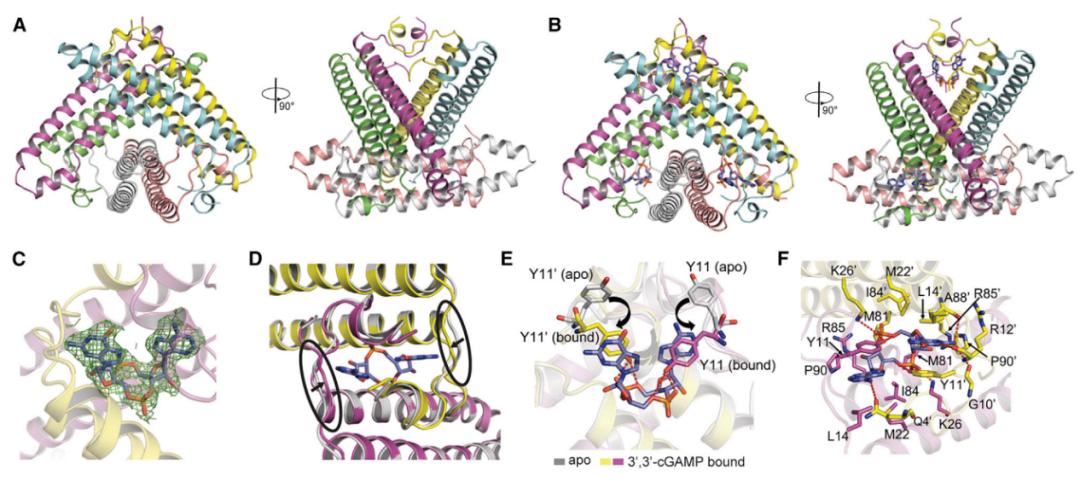 图1 Acb2及其结合3’, 3’-cGAMP的结构
图1 Acb2及其结合3’, 3’-cGAMP的结构后续通过体外生化实验,他们又进一步证实了Acb2还可以结合c-di-AMP/2’, 3’-cGAMP/3’, 3’-cUA/UG/UU等多种寡核苷酸信号分子,覆盖I型和II型两种CBASS系统,显示出Acb2是一种基于cGAS酶的免疫系统的广谱抑制蛋白。此外他们还发现,Acb2的缺失会造成CBASS系统阻断噬菌体的复制及溶原诱导,但少数噬菌体会通过主要的衣壳基因的突变来逃避CBASS系统的免疫作用(图2)。
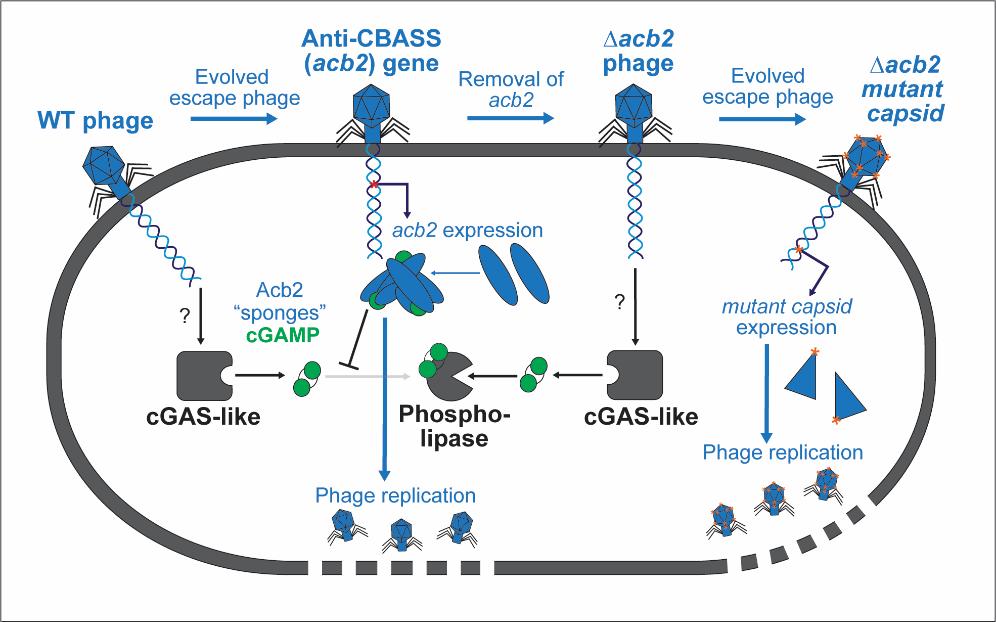 图2 Acb2蛋白抗CBASS系统的作用机制
图2 Acb2蛋白抗CBASS系统的作用机制综上,本文发现了内源性CBASS系统的抗噬菌体免疫作用,并提出了噬菌体抑制和逃避CBASS系统免疫的有效策略。Acb2蛋白作为广谱抑制蛋白,其可以通过结合多种环状寡核苷酸来抑制多种类型的CBASS系统。美国加州大学旧金山分校博士研究生Erin Huiting与北京化工大学博士研究生曹雪利为本论文的共同第一作者,北京化工大学冯越教授与加州大学旧金山分校Joseph Bondy-Denomy教授为本文的共同通讯作者。
作者专访
Cell Press细胞出版社公众号特别邀请冯越教授代表研究团队接受了专访,请他为大家进一步详细解读。
CellPress:
您的团队为何选择开展此项关于噬菌体拮抗细菌CBASS免疫系统的研究?
冯越教授:
我们团队长期从事噬菌体与细菌免疫系统互作的分子机制研究,已经在细菌CRISPR-Cas系统及噬菌体Anti-CRISPR(Acr)蛋白领域做出了一系列系统性的工作。我们先后阐明了七种噬菌体Acr蛋白以及一种新型CRISPR-Cas系统的工作机制,目前还有多项围绕Acr的工作正在有序推进中。值得一提的是,越来越多的证据表明,细菌的CRISPR-Cas系统和CBASS系统可共用关键的效应蛋白组分,二者在进化上甚至可能有共同的祖先。然而,CRISPR-Cas系统至今已经发现了多达101种Acr蛋白,但在我们的研究开始前,CBASS系统还没有任何”Acb”(Anti-CBASS)蛋白被发现。我们非常高兴鉴定到了Acb2这个蛋白,并通过生化和结构生物学研究揭示了它拮抗细菌CBASS免疫系统的精妙的工作机制。
CellPress:
您认为此项研究主要的亮点是什么?
冯越教授:
在我们针对Acb2的机制进行研究过程中,有其他课题组发现了Acb1,并证明其为磷酸二酯酶,可切割CBASS系统感应噬菌体后产生的信号分子。但我们发现的Acb2则是作为一种“海绵蛋白”吸附CBASS系统的信号分子,这是一种全新的噬菌体抑制CBASS系统免疫功能的机制。“海绵”一词巧妙且直白地描述了我们所研究的Acb2蛋白的功能,其吸附的信号分子被“强制”释放后仍然具有正常的活性。综上,我们的工作揭示了一种新颖的噬菌体抑制细菌CBASS免疫系统的策略。
CellPress:
您的团队未来在该领域有哪些进一步的研究计划?
冯越教授:
就Acb2蛋白本身而言,它是一个非常广谱的CBASS系统的抑制蛋白,可吸附多种CBASS系统的信号分子。然而我们最近的研究发现,Acb2的功能还不止于此,还有其他非常有趣的现象,我们正在继续探索。同时,我们还将继续在噬菌体与细菌免疫系统互作的领域中探索,希望在揭示细菌与噬菌体间“军备竞赛”背后更多的基础生物学机制的同时,帮助开发安全有效的噬菌体疗法以及新型的分子生物学工具。
 通讯作者简介
通讯作者简介 冯越
冯越教授
冯越,北京化工大学生命学院教授,博士生导师。长期聚焦于微生物与宿主免疫系统互作的分子机制这一研究领域,共发表通讯作者论文23篇,系统性的创新成果分别发表在Nature、Cell、Mol Cell(2篇)、Nat Chem Biol、PNAS、Nat Plants、Nat Commun(2篇)、Nucleic Acids Res、J Biol Chem(3篇)等期刊。基于在Acr研究领域的工作,受邀为J Mol Biol、RNA Biol等杂志撰写综述。曾获得全国青年岗位能手(2020)、北京市优秀青年人才(2020)、北京市科学技术进步奖二等奖(2018)、中国十大新锐科技人物(2018)、北京市科技新星(2019)等荣誉。
相关论文信息
论文原文刊载于Cell Press细胞出版社旗下期刊Cell上
▌论文标题:
Bacteriophages inhibit and evade cGAS-like immune function in bacteria
▌论文网址:
https://www.cell.com/cell/fulltext/S0092-8674(22)01584-7
▌DOI:
https://doi.org/10.1016/j.cell.2022.12.041
▲长按图片识别二维码阅读原文
1974年,我们出版了首本旗舰期刊《细胞》。如今,CellPress已发展为拥有50多本期刊的全科学领域国际前沿学术出版社。我们坚信,科学的力量将永远造福人类。
CellPress细胞出版社
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




