- +1
Nature子刊:双管齐下激活STING通路,增强抗肿瘤活性
原创 生物世界 生物世界 收录于合集 #表观遗传 14个
 撰文丨王聪
撰文丨王聪编辑丨王多鱼
排版丨水成文
癌症免疫疗法,包括肿瘤浸润淋巴细胞的过继细胞疗法和免疫检查点抑制剂抗体,极大地改变了当前的癌症治疗格局,但是,仍有相当一部分癌症患者对免疫治疗反应不佳。肿瘤细胞可以通过多种机制逃脱宿主的免疫识别,这包括肿瘤细胞的内在和外在因素。
因此,还需要深入了解肿瘤免疫逃逸机制,以克服对癌症免疫疗法的耐药性。
用一种组合策略靶向STING通路可提高抗肿瘤活性。
近日,美国莫菲特癌症中心的研究人员在 Nature Communications 期刊发表了题为:Epigenetic state determines the in vivo efficacy of STING agonist therapy 的研究论文。
这项研究表明,使用临床可用的DNA甲基化抑制剂(地西他宾)逆转小鼠黑色素瘤细胞系中STING的甲基化,可以改善STING激动剂诱导的STING激活和I型干扰素(IFN-I)诱导,在黑色素瘤小鼠模型中,可以通过CD8+T细胞依赖的免疫应答促进肿瘤消退。
这些发现揭示了肿瘤细胞中STING信号功能障碍导致STING激动剂治疗反应受损的机制,还表明通过表观遗传重编程恢复STING信号,可能提高STING激动剂的癌症治疗效果。
 STING通路是对病毒和细菌免疫反应的关键调节因子,并有助于抗肿瘤免疫。在几种癌细胞系中都观察到了STING信号的抑制,并且STING蛋白的表达随着某些癌症类型的进展而降低,例如黑色素瘤。这些发现表明,STING激动剂,或在肿瘤环境中激活STING通路的药物,可能具有抗肿瘤作用。
STING通路是对病毒和细菌免疫反应的关键调节因子,并有助于抗肿瘤免疫。在几种癌细胞系中都观察到了STING信号的抑制,并且STING蛋白的表达随着某些癌症类型的进展而降低,例如黑色素瘤。这些发现表明,STING激动剂,或在肿瘤环境中激活STING通路的药物,可能具有抗肿瘤作用。激活STING通路用于癌症治疗的想法在许多临床前研究中得到了证实,然而,STING激动剂在人体临床试验中的结果令人失望,无论是作为单一治疗,还是与免疫检查点抑制剂联合使用,都没有显示出令人满意的临床疗效。这表明有未知机制导致了这些不良反应。
在这项研究中,研究团队希望进一步了解STING通路,从而找到提高STING激动剂的抗肿瘤活性。他们此前已经证明,控制STING蛋白表达的DNA区域是通过甲基化过程进行修饰的。这种甲基化修饰降低了STING蛋白水平,从而减少了STING蛋白抑制肿瘤的发展。
研究团队推测,在肿瘤细胞中阻断甲基化并增加STING表达水平的药物,与STING激动剂联合使用,可能发挥更好的抗肿瘤效果。
研究团队在肿瘤细胞或周围免疫细胞中STING信号有缺陷的黑色素瘤小鼠模型上进行了实验。与人类STING基因相似,他们发现小鼠STING基因也受到甲基化调控。
当研究团队用阻断DNA甲基化的药物(地西他宾)处理细胞时,STING蛋白表达水平和信号传递增加,进而导致产生更强的抗肿瘤免疫反应。他们还证明,用甲基化抑制剂和STING激动剂联合治疗肿瘤小鼠模型,可改善抗肿瘤活性,这种活性依赖于CD8 T细胞的存在和活性。
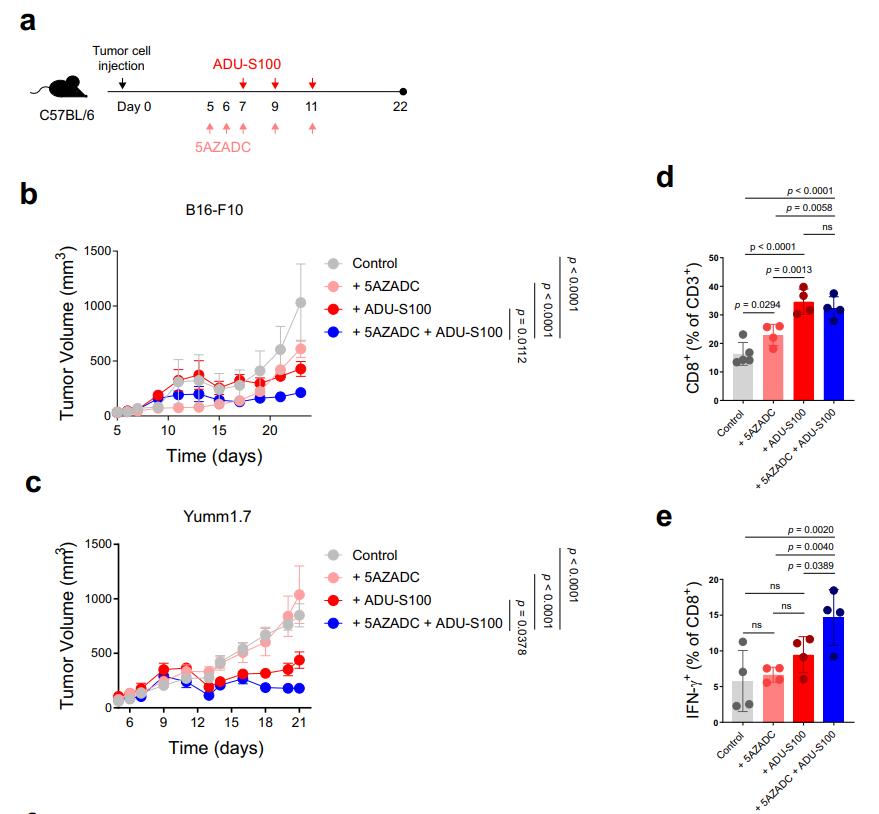 这些研究结果表明,用甲基化抑制剂重新激活肿瘤细胞中的STING通路可以进一步增强STING激动剂的抗肿瘤效果。这项临床前研究有望为临床癌症患者带来更好的治疗方法。
这些研究结果表明,用甲基化抑制剂重新激活肿瘤细胞中的STING通路可以进一步增强STING激动剂的抗肿瘤效果。这项临床前研究有望为临床癌症患者带来更好的治疗方法。论文通讯作者 James J. Mulé 表示,还需要进一步研究来确定甲基化抑制剂和STING激动剂的最佳剂量组合,这项研究为开发基于STING通路的癌症治疗方法提供了新思路。
论文链接:
https://www.nature.com/articles/s41467-023-37217-1
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




