- +1
中科院化学所范青华团队:新型C1对称的手性氮杂环卡宾配体及其参与的铜催化不对称硼化/环化串联反应—…
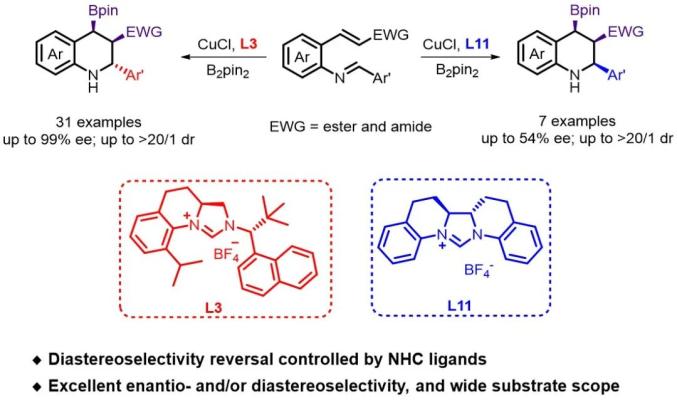
近日,中国科学院化学研究所范青华课题组发展了一类结构可调的新型C1对称的手性氮杂环卡宾(NHC)配体,并成功应用于铜催化的不对称硼化/曼尼希环化串联反应中,以良好的收率和优异的对映选择性及非对映选择性,实现了结构多样的含硼基团的手性2,3-trans-3,4-cis-三取代四氢喹啉衍生物的合成。此外,通过使用位阻较小的手性NHC配体,首次实现了全顺式2,3,4-三取代手性四氢喹啉衍生物的不对称催化合成。
 背景介绍:
背景介绍:新型手性配体的设计与合成一直是不对称催化领域的研究前沿与热点之一。作为一类稳定的强σ给电子配体,手性氮杂环卡宾(NHC)已被广泛应用于多种不对称催化反应研究,并已取得了引人注目的发展。其中,C2对称的手性NHC配体占据主导地位。虽然C1对称的手性NHC配体具有更加精细的电子分布和空间结构,在不对称催化反应中表现出与C2对称的手性NHC配体相当或更优的手性诱导能力,但是,由于该类配体一般需要从手性原料出发,并经历多步反应进行合成,且结构修饰比较困难,所以,发展结构可调的C1对称手性NHC配体的高效不对称合成新方法仍面临挑战。
铜催化的不对称硼化偶联反应是构建结构复杂的含硼基团的手性有机分子的高效方法之一,近年来受到科学家们的广泛关注。其中,铜催化的不对称硼化/环化串联反应已被成功应用于手性含硼基团的碳环或杂环化合物的合成。最近,Lautens小组使用手性双膦配体,首次通过不对称硼化/环化串联反应实现了含硼基团的手性2,3-cis-3,4-trans-三取代四氢喹啉衍生物的不对称催化合成,但产物的立体选择性以及底物的广谱性还有待进一步提升,且全顺式手性2,3,4-三取代四氢喹啉化合物的不对称催化合成尚未实现。
本文亮点:
基于以上研究背景,作者采用他们自己发展的还原胺化/不对称氢化串联反应构建手性邻二胺的新方法,设计并合成了一类同时含有手性四氢喹啉并环结构和手性大位阻N-取代基两种优势结构单元的新型C1对称NHC配体(图1)。该类配体可以由简单易得的喹啉醛和手性胺原料出发,高效、高对映选择性地进行克级规模的合成。该方法易于配体结构的拓展和配体库的构建,而且其高度模块化的结构特点有利于通过调整取代基的种类、位置以及手性中心的构象来实现催化剂手性口袋的调节与优化。此外,通过铜(I)-卡宾配合物单晶结构分析,表明该类配体具有较大的包埋体积和独特的四象限立体结构分布,可以在铜金属中心周围形成拥挤的手性口袋,提升其在不对称催化反应中的手性诱导能力。
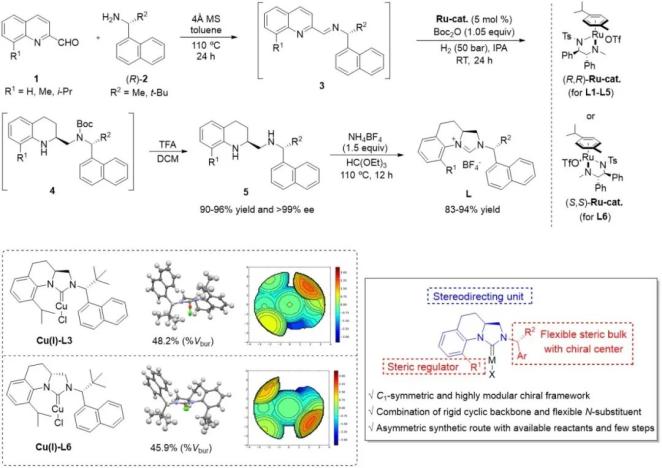 图1. 新型C1对称手性NHC配体的合成及其Cu(I)配合物的四象限结构分析
图1. 新型C1对称手性NHC配体的合成及其Cu(I)配合物的四象限结构分析随后,作者将该类手性NHC配体应用到铜(I)催化的不对称硼化/环化串联反应中,发现该类配体可以获得比许多优势C2对称手性NHC配体更好的反应效果。通过对反应条件的系统筛选,最终以良好的分离产率、优异的对映选择性和非对映选择性得到一系列结构多样的2,3-trans-3,4-cis-三取代手性四氢喹啉衍生物。与双膦配体催化体系相比,部分含特殊官能团(如酰胺、噻吩等)产物的立体选择性得到了大幅提升。此外,酮亚胺底物被首次应用于该串联反应,且以优异的非对映选择性(14:1 dr)和对映体选择性(96% ee)得到含有季碳中心的手性三取代四氢喹啉衍生物(10t),为四氢喹啉骨架上手性季碳中心的构筑提供了一种新的策略。
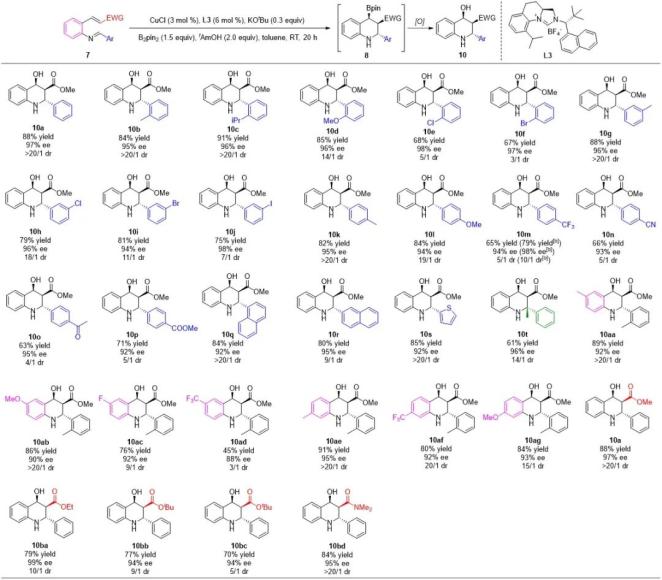 图2. 铜(I)催化的不对称硼化/环化串联反应的底物范围
图2. 铜(I)催化的不对称硼化/环化串联反应的底物范围同时,采用小位阻的C2对称手性NHC配体L11,实现了产物非对映选择性的反转,以优异的非对映选择性和中等的对映选择性获得了全顺式2,3,4-三取代手性四氢喹啉衍生物(图3),从而为结构多样的手性三取代四氢喹啉衍生物的合成提供了新途径。
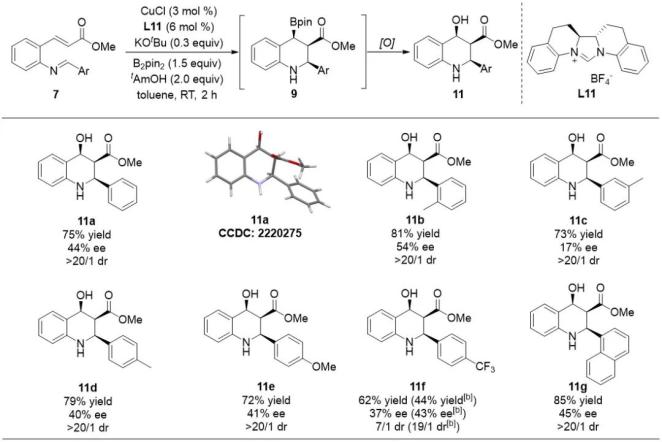 图3. 全顺式2,3,4-三取代手性四氢喹啉衍生物的不对称合成
图3. 全顺式2,3,4-三取代手性四氢喹啉衍生物的不对称合成最终,作者提出了不同的手性NHC配体-铜配合物催化该不对称硼化/环化串联反应的可能催化循环和反应过渡态(图4)。认为这一反应均经过了底物的1,2-顺式硼铜化加成步骤,而最终环化产物的非对映选择性取决于是否生成烯醇中间体C1’,为这一配体控制的非对映选择性反转现象给出了合理的解释。并通过对过渡态的模拟四象限分析、反应中间体理论ee值的推算,同时结合一系列控制实验,初步揭示了手性NHC配体在该反应中的手性诱导机制,证明底物的1,2-顺式硼铜化加成反应的立体选择性最终决定了产物的对映选择性高低。
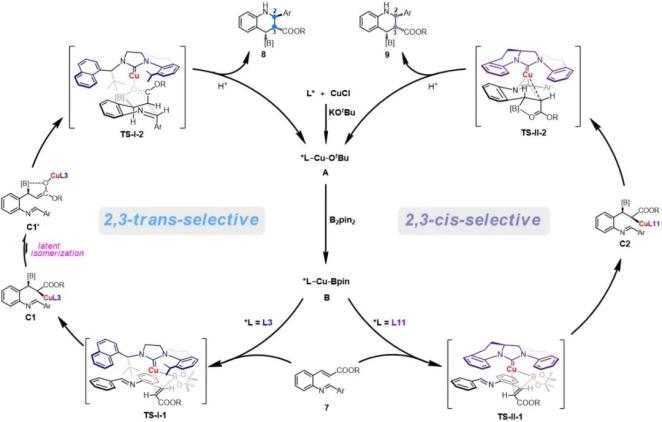 图4. 可能的催化循环与立体选择性控制模型
图4. 可能的催化循环与立体选择性控制模型总结与展望:
综上所述,该研究工作采用不对称催化合成策略,设计合成了一类结构可调的新型C1对称手性NHC配体,它们具有较大的包埋体积和独特的四象限立体结构分布,可在铜金属中心周围形成拥挤的手性口袋。在铜催化的不对称硼化/曼尼希环化串联反应中,该类C1对称的NHC配体显示出优异的对映选择性和非对映选择性,以及广谱的底物适用性。此外,采用小位阻的C2对称手性NHC配体,实现了产物非对映选择性的反转,从而为含硼基团的手性三取代四氢喹啉衍生物的合成提供了高效的新方法。同时,作者提出了该不对称硼化/环化串联反应可能的催化循环和反应过渡态,为这一配体决定的非对映选择性反转现象给出了合理的解释。本研究工作为发展新型C1对称的手性NHC配体提供了全新的思路。
文章详情:
Tunable Unsymmetrical Chiral N-Heterocyclic Carbene Ligands for Highly Diastereo and Enantioselective Copper-Catalyzed Tandem Borylative Cyclization: Ligand Controlled Diastereoselectivity Reversal
Jiahong Han, Yan-Mei He, Yixiao Pan, Faju Li, Dongyu Li, Wei Hao and Qing-Hua Fan*
Cite this by DOI:10.31635/ccschem.023.202302781
文章链接:https://doi.org/10.31635/ccschem.023.202302781
扫码在线阅读
扫描或长按左侧二维码,
在线阅读全文
 中国化学会
中国化学会Chemsoc
原标题:《中科院化学所范青华团队:新型C1对称的手性氮杂环卡宾配体及其参与的铜催化不对称硼化/环化串联反应——配体控制的非对映选择性反转》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




