- +1
植物所鲁丽敏述评:一个高度复杂的内共生系统——包含七个基因组的隐藻细胞
原创 Cell Press CellPress细胞科学
 生命科学
生命科学Life science
作为世界领先的全科学领域学术出版社,细胞出版社特与“中国科学院青年创新促进会”合作开设“青促会述评”专栏,以期增进学术互动,促进国际交流。
2023年第十五期(总第143期)专栏文章,由中国科学院植物研究所研究员、中国科学院青年创新促进会会员 鲁丽敏,就 Current Biology中的论文发表述评。
 长按图片扫描二维码阅读论文
长按图片扫描二维码阅读论文不同物种的共生是自然界中普遍存在的生命现象。共生所引起的复杂相互作用,往往导致各种不同的适应结果,对生物进化有着深远的影响。共生可以分为内共生和外共生。其中,内共生是指一种生物生长在另一生物体内(如细胞或组织中),两种生物间常具有互利共生关系。
原核生物(如细菌)和原生生物(一些结构简单的真核生物的泛称,多为单细胞,如变形虫、草履虫、某些藻类)的共生,是内共生现象的重要表现形式。现在,学术界已经普遍接受,我们熟悉的细胞器——线粒体和质体,就是由内共生于原始真核生物体内的原核生物(如细菌和蓝藻)经历漫长的岁月演变而来的。但是,稳定的内共生关系并不是那么容易建立的,有研究显示,大多数内共生体难逃在宿主体内消亡的命运——即便能侥幸存活,共存时间也不会太长。
上面说的,都是由原核生物与真核生物两方组成的内共生系统。我们知道,噬菌体还可以入侵以细菌为代表的原核生物,那么,自然界中是否存在由真核生物、原核生物和噬菌体三方构成的稳定内共生系统呢?答案是肯定的。一个著名的例子就是“节肢动物-沃尔巴克氏体-WO噬菌体”共生系统,内共生体及其内部的噬菌体可以通过编码蛋白质的形式为其终极宿主提供保护。但是,这样的情况很少见,而且大部分发生在动物中。
那么,在原生生物中,是否也存在类似的三方内共生系统呢?答案也是肯定的。隐藻就是一个涉及原生生物宿主的有趣案例。隐藻的质体是通过红藻的次级内共生获得的,它也作为研究细胞器进化的模式生物而受到广泛关注,有着悠久而完整的培养记录。早在1988年,一份来自著名的哥廷根大学藻种保藏库(SAG)的隐藻属品系SAG 25.80就吸引了科学家的注意,他们用电子显微镜在其细胞中观察到了一些内共生体和病毒样颗粒。但是,受技术条件限制,他们并没有鉴定出这些内共生体的准确身份;宿主、内共生体、病毒样颗粒之间的关系,也有待进一步研究。
直到最近,来自不列颠哥伦比亚大学的研究人员利用基因组数据,终于证实了这个由原生生物、原核生物和噬菌体三方共同构成的共生系统。更加令人惊讶的是,这个高度复杂的共生系统竟然在实验室里稳定存活了50余年!这一研究于2023年4月27日以“A single cryptomonad cell harbors a complex community of organelles, bacteria, a phage, and selfish elements”为题在线发表于Cell Press细胞出版社旗下期刊Current Biology。
为了准确鉴定这一共生系统内各个成员的身份,研究人员首先组装了该品系(Cryptomonas sp. SAG 25.80)的基因组。通过与已发表序列比对,他们证实该宿主细胞为此前曾经报道过的隐藻属物种Cryptomonas gyropyrenoidosa。同时,他们还鉴定出两种内共生立克次氏体(分别为Megaira polyxenophila和Grellia numerosa)和一种噬菌体(作者将其命名为MAnkyphage)(图1)。
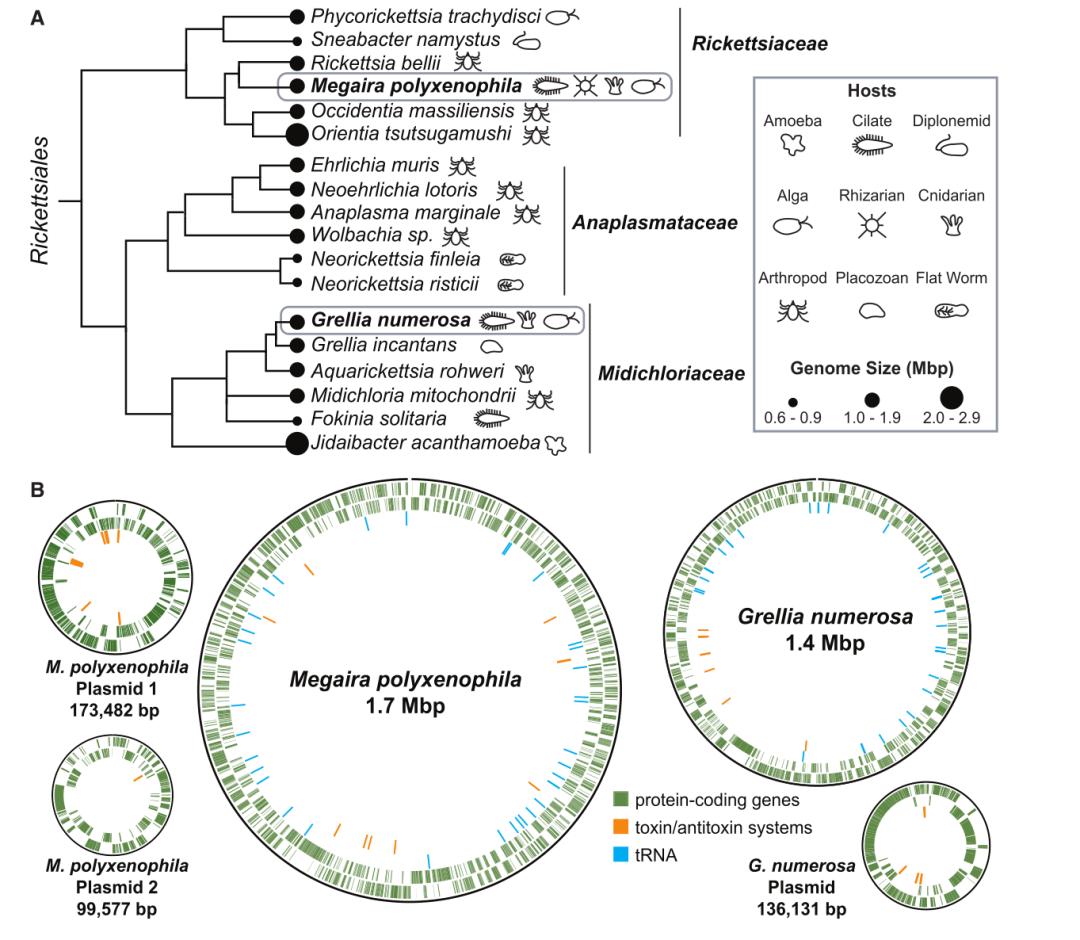 ▲图1 Cryptomonas gyropyrenoidosa品系SAG 25.80中内共生体的基因组概况
▲图1 Cryptomonas gyropyrenoidosa品系SAG 25.80中内共生体的基因组概况对两种内共生体的基因组分析发现,M. polyxenophila基因组由一条1.7 Mbp的染色体和两个质粒组成,G. numerosa基因组由一条1.4 Mbp的染色体和一个质粒组成;前者比后者拥有更多的蛋白质编码基因(1915 vs. 1403),同时也拥有更为丰富的转座子(16% vs. 4%);两者都含有多个毒素-抗毒素系统,这些系统可能是转录和翻译的调控因子。而对噬菌体和内共生体基因组的分析表明,内共生体M. polyxenophila是噬菌体MAnkyphage的宿主。
然后,他们通过荧光原位杂交技术(FISH)和透射电镜(TEM)进一步确认了内共生体和噬菌体的存在(图2C-E)。在每个宿主细胞中,M. polyxenophila的丰度始终高于G. numerosa,约有17% ± 8%的内共生体存在病毒样颗粒(图2F-H)。
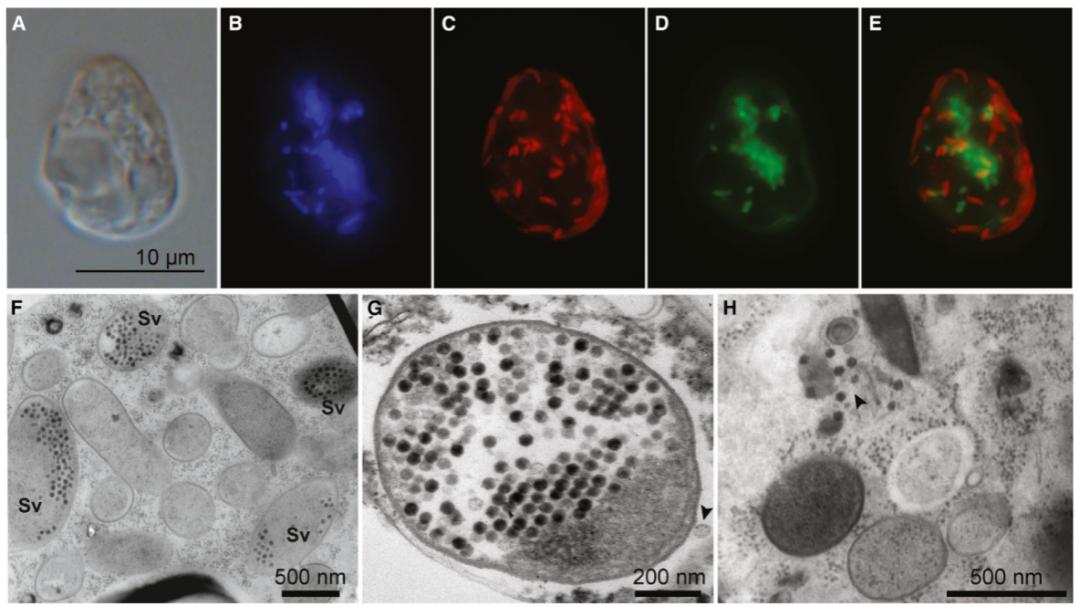 ▲图2 C. gyropyrenoidosa SAG 25.80的显微图像
▲图2 C. gyropyrenoidosa SAG 25.80的显微图像代谢途径分析发现,两种内共生体的代谢相关基因与其他已报道的菌株类似,其中G. numerosa展现出比M. polyxenophila更强的生物合成能力。而M. polyxenophila无法独立产生辫苷,可能对G. numerosa存在代谢依赖。另外,它们的基因组编码了大量可能参与和宿主互作的蛋白,其中多个具有ANK或LRR结构域。部分蛋白的ANK结构域与外膜蛋白的融合表明,内共生体和隐藻细胞之间存在直接的蛋白相互作用。通过比较所有已知的Megaira属和Grellia属立克次氏体基因组发现,尽管宿主各异,但内共生体的功能多样性高度相似,这可能提示了宿主-内共生体相互作用的一般机制。
最后,作者对噬菌体MAnkyphage基因组的研究发现,它可以编码51个基因,包括核心基因和辅助基因两大类。其中有些可以表达与真核细胞中类似的蛋白,这些蛋白功能各异,例如有的可能有结构功能,有的可能有调控宿主毒素-抗毒素系统的功能,有的甚至可能操控宿主繁殖、帮助内共生体逃避宿主免疫等。但是,仍有许多蛋白质的功能尚不清楚。对环境样本的检测表明,噬菌体MAnkyphage所在的支系在自然界中广泛存在,可以侵染来自从淡水到海洋等不同环境的Megaira属立克次氏体。
这项研究首次从分子水平上揭示了隐藻中经由多次内共生形成的、包含七个基因组的复杂系统(图3)。这个系统的复杂性和各组分之间的潜在冲突,似乎暗示着这个系统经历了复杂的选择过程,甚至终将在进化中崩溃。但事实是,它已经维持了4000多代,显示出极高的稳定性。这一长期维系的复杂系统不仅展现了裂解周期和溶源周期之间的微妙平衡,也提示我们对内共生系统的选择压,特别是系统内各组分之间相互作用受到的不同选择压的关注。
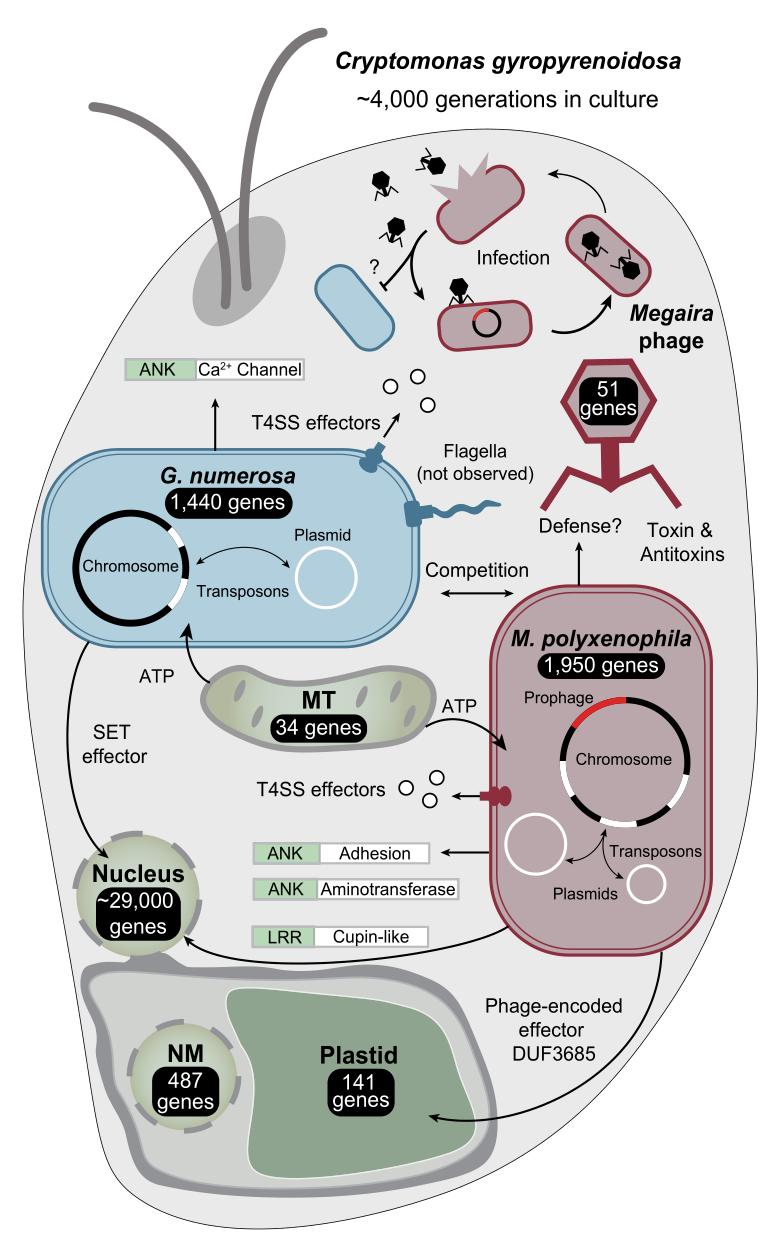 ▲图3 MAnkyphage、两种内共生体(M. polyxenophila和G. numerosa)及隐藻宿主之间可能的互作关系
▲图3 MAnkyphage、两种内共生体(M. polyxenophila和G. numerosa)及隐藻宿主之间可能的互作关系论文摘要
原核生物和原生生物的共生对进化生物学和生态学有着深远影响。内共生导致了线粒体和质体的出现,随后后者又通过几轮内共生在真核生物中广泛存在。现在,原生生物中的内共生体普遍且多样,尽管我们通常并不了解它们的功能。在这项研究中,我们描述了一个存在于隐藻细胞中、由内共生体和噬菌体构成的高度复杂的群落。隐藻类因其次级质体中保留了内共生体残留的细胞核而被作为细胞器进化的模式生物,但目前仅发现一个此前未鉴定的隐藻属(Cryptomonas)品系(SAG 25.80)包含细菌内共生体。我们通过电镜观察、FISH成像技术和基因组测序对隐藻属品系SAG 25.80进行研究,发现了一个在50多年的连续培养后仍保持稳定的复杂共生群落。我们确定宿主物种为Cryptomonas gyropyrenoidosa,并对其线粒体、质体、类核体(以及部分细胞核),两种内共生体Megaira polyxenophila和Grellia numerosa,以及侵染M. polyxenophila的噬菌体(MAnkyphage)的基因组进行测序。与来自其他宿主密切相关的内共生体相比,这些内共生体大部分具有类似的代谢和基因组特征,除了与隐藻属共生的M. polyxenophila拥有丰富的转座子,并展现高度的基因组可塑性。我们在MAnkyphage的基因组中发现了大量与真核细胞相互作用的基因以及毒素-抗毒素系统,且该基因组可以编码数个与真核细胞中类似的蛋白。总体来说,该隐藻细胞是一个具有七个独立进化的基因组的内共生集合体,这些基因组显示出各类群间相互冲突的证据,但即使已经培养了约4380代,这一系统仍然保持稳定。
Symbiosis between prokaryotes and microbial eukaryotes (protists) has broadly impacted both evolution and ecology. Endosymbiosis led to mitochondria and plastids, the latter spreading across the tree of eukaryotes by subsequent rounds of endosymbiosis. Present-day endosymbionts in protists remain both common and diverse, although what function they serve is often unknown. Here, we describe a highly complex community of endosymbionts and a bacteriophage (phage) within a single cryptomonad cell. Cryptomonads are a model for organelle evolution because their secondary plastid retains a relict endosymbiont nucleus, but only one previously unidentified Cryptomonas strain (SAG 25.80) is known to harbor bacterial endosymbionts. We carried out electron microscopy and FISH imaging as well as genomic sequencing on Cryptomonas SAG 25.80, which revealed a stable, complex community even after over 50 years in continuous cultivation. We identified the host strain as Cryptomonas gyropyrenoidosa, and sequenced genomes from its mitochondria, plastid, and nucleomorph (and partially its nucleus), as well as two symbionts, Megaira polyxenophila and Grellia numerosa, and one phage (MAnkyphage) infecting M. polyxenophila. Comparing closely related endosymbionts from other hosts revealed similar metabolic and genomic features, with the exception of abundant transposons and genome plasticity in M. polyxenophila from Cryptomonas. We found an abundance of eukaryote-interacting genes as well as many toxin-antitoxin systems, including in the MAnkyphage genome that also encodes several eukaryotic-like proteins. Overall, the Cryptomonas cell is an endosymbiotic conglomeration with seven distinct evolving genomes that all show evidence of inter-lineage conflict but nevertheless remain stable, even after an estimated 4,380 generations in culture.
向下滑动阅览摘要原文
中文内容仅供参考,请以英文原文为准
述评人简介
 鲁丽敏
鲁丽敏中国科学院植物研究所研究员
中国科学院青年创新促进会会员
liminlu@ibcas.ac.cn
鲁丽敏,博士,中国科学院植物研究所研究员,中国科学院青年创新促进会2020届会员。主要从事植物生命之树重建与生物多样性保护研究。迄今为止,以第一或通讯作者在Nature、National Science Review、New Phytologist等国际学术期刊发表论文30余篇,研究成果入选2018年度“中国生命科学十大进展”。先后得到中国科协青年人才托举工程和国家自然科学基金优秀青年科学基金等项目支持。现担任Australian Systematic Botany和Molecular Phylogenetics and Evolution副主编。
Limin Lu, Ph.D., Professor at Institute of Botany, Chinese Academy of Sciences. She has been a member of “Youth Innovation Promotion Association CAS” since 2020. Her research interests focus on plant tree of life reconstruction and biodiversity conservation. She has published more than 30 papers in journals such as Nature, National Science Review and New Phytologist as the first or corresponding author, and the research in Nature has been selected as one of the “2018 top 10 scientific advances in life sciences of China”. She has been supported by the Young Elite Scientists Sponsorship Program by China Association for Science and Technology and the Excellent Young Scientists Fund by National Natural Science Foundation of China. She now serves as Associate Editor for Australian Systematic Botany and Molecular Phylogenetics and Evolution.
向下滑动阅览英文简历
相关论文信息
原文刊载于CellPress细胞出版社
旗下期刊 Current Biology 上,
点击“阅读原文”或扫描下方二维码查看论文

 中国科学院青年创新促进会(Youth Innovation Promotion Association,Chinese Academy of Sciences)于2011年6月成立,是中科院对青年科技人才进行综合培养的创新举措,旨在通过有效组织和支持,团结、凝聚全院的青年科技工作者,拓宽学术视野,促进相互交流和学科交叉,提升科研活动组织能力,培养造就新一代学术技术带头人。
中国科学院青年创新促进会(Youth Innovation Promotion Association,Chinese Academy of Sciences)于2011年6月成立,是中科院对青年科技人才进行综合培养的创新举措,旨在通过有效组织和支持,团结、凝聚全院的青年科技工作者,拓宽学术视野,促进相互交流和学科交叉,提升科研活动组织能力,培养造就新一代学术技术带头人。Youth Innovation Promotion Association (YIPA) was founded in 2011 by the Chinese Academy of Science (CAS). It aims to provide support for excellent young scientists by promoting their academic vision and interdisciplinary research. YIPA has currently more than 4000 members from 109 institutions and across multiple disciplines, including Life Sciences, Earth Science, Chemistry& Material, Mathematics & Physics, and Engineering. They are organized in 6 discipline branches and 13 local branches.
 孟庆华述评:深度学习虚拟压头实现纳米尺度材料硬度的快速无损测量 | Cell Press青促会述评
孟庆华述评:深度学习虚拟压头实现纳米尺度材料硬度的快速无损测量 | Cell Press青促会述评 光化学铁催化脱羧叠氮化反应:配体-金属电荷转移和自由基配体转移的串联催化 | Cell Press青促会述评 青促会述评》
光化学铁催化脱羧叠氮化反应:配体-金属电荷转移和自由基配体转移的串联催化 | Cell Press青促会述评 青促会述评》本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




