- +1
代谢重编程的TI-Tregs:肿瘤治疗中的“特洛伊木马”?
原创 Cell Press CellPress细胞科学
 生命科学Life science
生命科学Life science在精准肿瘤治疗时代,尽管靶向肿瘤代谢治疗与免疫治疗配合进行,但由于忽视了肿瘤微环境(TME)中免疫细胞的代谢,导致其抗肿瘤疗效并不稳定。肿瘤浸润Treg细胞(tumor-infiltrating Treg cells, TI-Tregs)是一类独特的免疫细胞亚群,其能克服代谢限制(缺氧、酸性、营养匮乏)的肿瘤微环境,并继续维持自身的免疫抑制功能。然而,当前的Treg靶向疗法特异性不足,易诱发系统免疫失稳和继发自身免疫疾病,成为悬在其头上的“达摩克利斯之剑”。近日,南京医科大学第一附属医院吕凌教授和古鉴教授团队应邀在Cell Press细胞出版社旗下期刊Trends in immunology发表了题为“Targeting the metabolism of tumor-infiltrating Treg cells”的观点文章。该论文系统总结了该团队及国内外同行在肿瘤代谢调控TI-Tregs功能领域的最新进展,提出靶向代谢对于特异性清除TI-Tregs的重要潜力和意义,并着重归纳了未来的研究重点。
代谢重编程的TI-Tregs:肿瘤治疗中的“特洛伊木马”?
Foxp3是Treg特异性转录因子,参与调节免疫和代谢。Treg可作为代谢中心,响应局部或全身代谢信号并调节人体免疫耐受。在人卵巢癌和小鼠卵巢、结肠癌和黑色素瘤模型中,活性氧(ROS)可以诱导Treg细胞凋亡。一定的乳酸浓度也为TI-Tregs提供了功能所需的碳源。然而,尚不清楚代谢限制对TI-Tregs是有益还是有害,以及它如何影响肿瘤预后。一般来说, TI-Tregs会损害免疫治疗和代谢干预,是两种治疗方法的共同障碍。
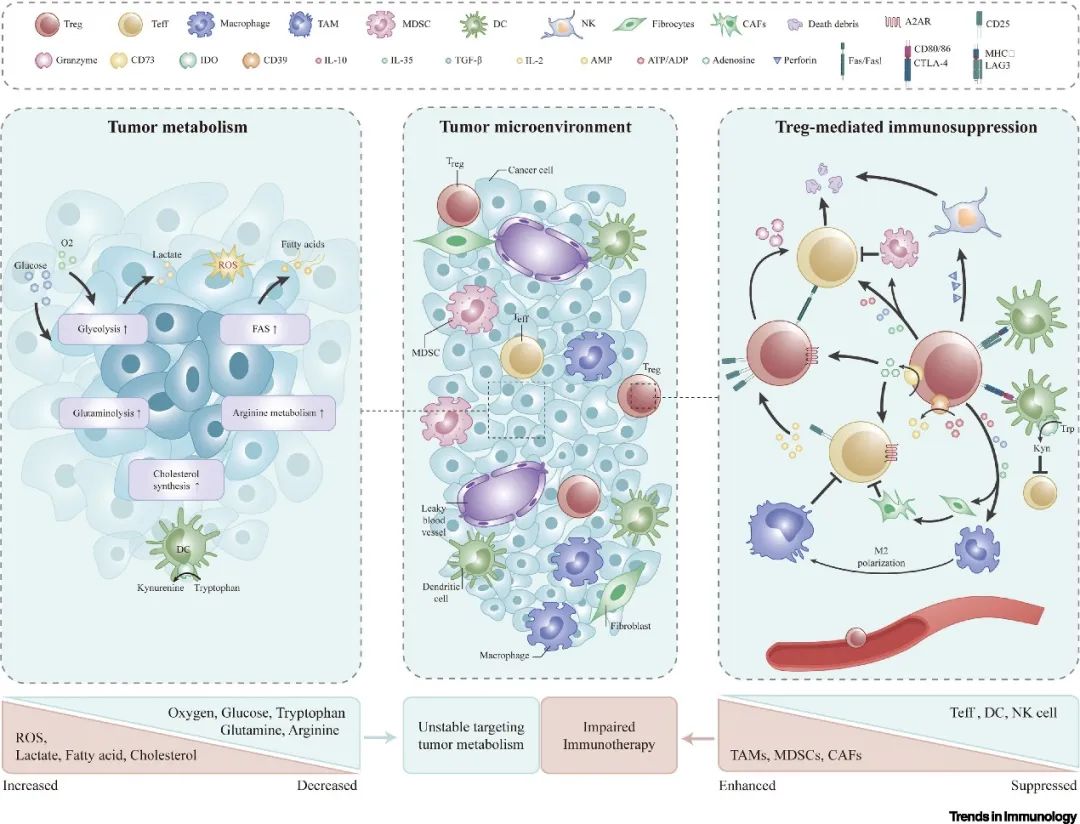 ▲图1 肿瘤代谢产物与Treg细胞介导的免疫抑制
▲图1 肿瘤代谢产物与Treg细胞介导的免疫抑制靶向代谢:TI-Tregs的“阿克琉斯之踵”?
由于TI-Tregs与效应T细胞(Teffs)和外周Tregs有共同的靶标,因此靶向TI-Tregs十分困难。Teffs依赖于糖酵解,而Tregs优先激活氧化磷酸化(OXPHOS)并减少肿瘤中的葡萄糖摄取。与外周Treg相比,TI-Tregs在黑色素瘤模型中通过脂质信号表现出功能特化。在黑色素瘤模型中,CD36拮抗剂破坏脂质代谢选择性地消耗TI-Tregs,恢复抗PD-1治疗的效果而没有诱发严重的自身免疫。因此,基于代谢的靶标可能为TI-Tregs消耗提供高效、安全、可控的方法。
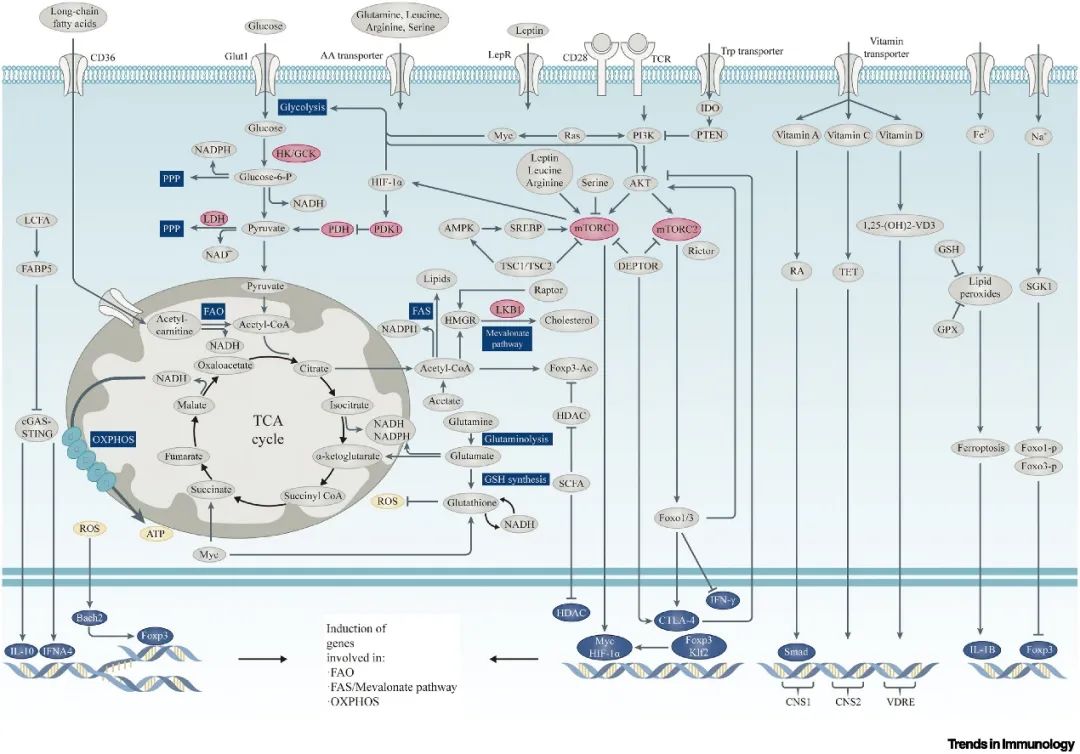 ▲图2 Treg细胞代谢概览
▲图2 Treg细胞代谢概览TME代谢限制对TI-Tregs的影响
肿瘤诱导的免疫抑制和TME代谢是相互关联的,某些营养素和代谢物的增加(ROS、乳酸、脂肪酸和胆固醇)或减少(氧、葡萄糖、色氨酸、谷氨酰胺和精氨酸)均可对TI-Tregs产生影响。
1 缺氧
缺氧是TME的一个特征,主要由代谢活跃的肿瘤细胞和功能失调的血管系统引起。缺氧激活了TME中的HIF-1α通路,促进了Tregs从外周向胶质瘤内的浸润,机制上与糖酵解和脂肪酸氧化的上调有关。但在自身免疫性脑炎小鼠模型中,缺氧增强了HIF-1α对Foxp3启动子区域的结合与降解,阻碍了Treg的功能。这些研究表明,在不同的模型中,缺氧可能会对TI-Tregs产生截然不同的影响。
2 葡萄糖缺乏
为避免与肿瘤细胞竞争葡萄糖,TI-Tregs利用OXPHOS产生能量。在AOM-DSS诱导的小鼠结直肠癌模型中,抑制MondoA-TXNIP(糖酵解的负调节因子)导致Treg不稳定并转化为Th17样表型。相比之下,与SKOV3卵巢癌细胞共培养的Tregs通过过表达葡萄糖转运蛋白(如Glut1和Glut3)和代谢酶(如葡萄糖-6-磷酸异构酶)存活并发挥功能。在黑色素瘤模型中,Toll样受体8信号通过抑制mTOR-HIF-1α轴,抑制TI-Tregs的糖代谢并减少其数量。这些研究强调,在不同的癌症类型中,葡萄糖可用性对TI-Tregs的功能和分化有不同的影响。
3 乳酸富集
乳酸是一种由肿瘤细胞产生的免疫抑制性糖酵解代谢物,可干扰Tconvs而不干扰TI-Tregs。在肝转移性肿瘤中,TI-Tregs通过上调的单羧酸转运蛋白1 (MCT1)增加乳酸摄取,随后通过乳酸脱氢酶(LDH)转化为丙酮酸,进入三羧酸循环,生成ATP。乳酸吸收导致Treg上的PD-1上调,降低PD-1阻断的疗效。乳酸还通过调节MOESIN的乳酸化和增强TI-Tregs来促进肝癌的发生。这些研究一致认为,肿瘤产生的乳酸上调PD-1,支持TI-Treg增殖,从而抑制CD8+ T细胞,促进肿瘤发生。
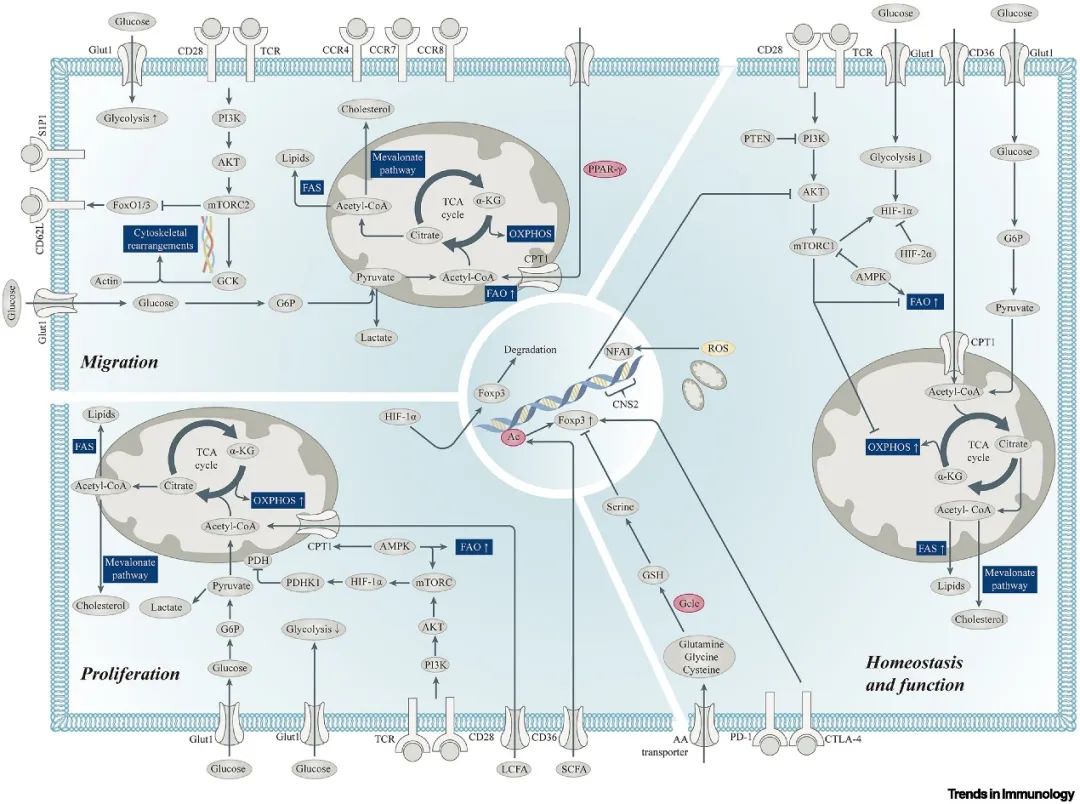 ▲图3 Treg细胞在迁移、增殖、功能中的代谢变化
▲图3 Treg细胞在迁移、增殖、功能中的代谢变化基于代谢的Treg靶向治疗
代谢重编程是TI-Tregs的一个标志。相应的代谢调节因子为其精确、有针对性的消除提供了希望(图4)。
1 糖代谢
糖酵解抑制剂如2-脱氧-D-葡萄糖(2-DG)、2-巯基乙醇等可降低人类卵巢癌和小鼠黑色素瘤或结肠癌模型中Tregs的功能和增殖。PI3K-AKT-mTOR信号通路在其中发挥了关键作用。在小鼠黑色素瘤模型中,mTOR抑制剂通过限制葡萄糖摄取来限制TI-Tregs的数量和功能。在纤维肉瘤模型中,促进PI3K-AKT-mTOR通路会减弱Tregs的分化和功能稳定性。此外,阻断糖代谢可与多种代谢途径交联,如PI3K-β抑制剂可减少胃癌中Treg游离脂肪酸的产生、脂质摄取和代谢,抑制Treg的迁移和功能。这些广泛的证据表明,药物抑制PI3K-AKT-mTOR通路可降低Treg功能和增殖,并结合代谢和免疫调节因子导致癌症治疗取得进展。
2 脂代谢
5-十四环氧基-2-呋喃酸通过抑制TI-Tregs中的乙酰辅酶A羧化酶而损害脂肪酸合成(FAS),改善小鼠肝癌。然而,本研究中Treg的功能障碍可能是由药物直接毒性引起的,而不是通过干扰免疫代谢引起的。相比之下,在黑色素瘤模型中,CD36抑制剂可以有效且安全地阻断TI-Tregs中的脂肪酸的摄取和脂质代谢,阻碍Treg的积累,而不会造成系统性Treg缺失。同样,依托莫西通过抑制肉毒碱棕榈酰基转移酶1A (CPT1A)干扰脂肪酸氧化(FAO),降低Treg/Teff比率,从而改善胶质瘤小鼠模型的预后。这些令人鼓舞的研究表明,靶向TI-Tregs中的脂质代谢可改善癌症治疗效果,然而,需要进一步规避直接的药物毒性问题以开发更安全的治疗方法。
3 氨基酸代谢
通过吲哚胺2,3-双加氧酶(IDO)靶向犬尿氨酸途径有可能消除胶质母细胞瘤中的Treg。多种IDO1抑制剂已被开发,但没有一种被FDA批准用于癌症治疗。因此,IDO抑制剂值得进一步的临床尝试,而其他的氨基酸靶点仍有待在小鼠模型中探索。
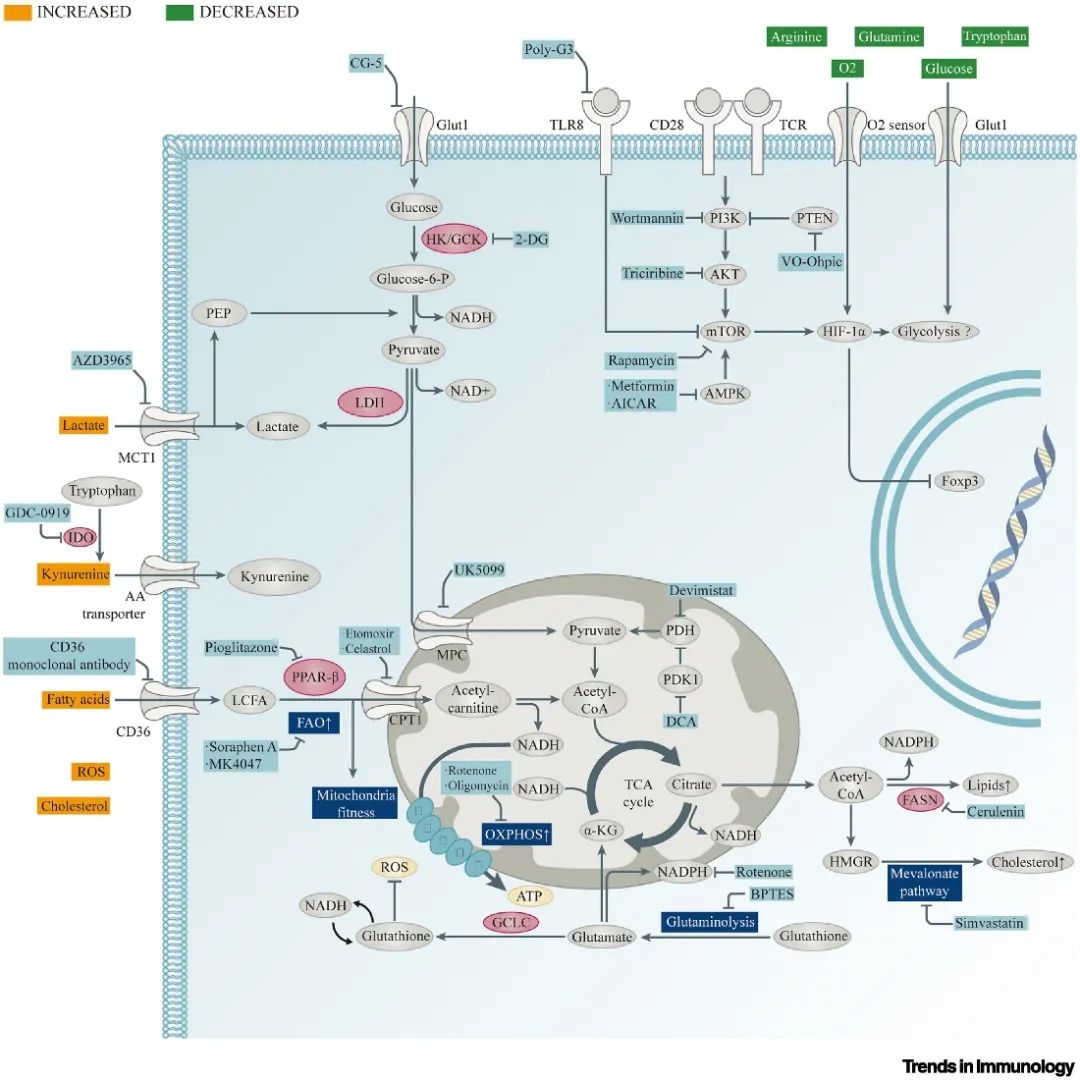 ▲图4 靶向TI-Tregs代谢途径的药物
▲图4 靶向TI-Tregs代谢途径的药物结论与展望
TI-Tregs是否引起靶向肿瘤代谢和免疫治疗的耐药性仍然是一个悬而未决的问题,基于代谢的TI-Tregs疗法可能是辅助肿瘤代谢治疗和免疫治疗的良好候选靶点。由于改变细胞代谢的药物已经存在,靶向免疫细胞代谢是一个可行的方向。但由于不同器官或来源肿瘤具有不同的代谢特征,代谢靶点的筛选需要更加个性化。基于当前的基础研究成果,即TME可作为Treg代谢促进剂,体外培养功能性和持久性Treg可能最终提高临床Treg再输注治疗免疫疾病和移植排斥反应的疗效。
因此,未来的研究方向应着重聚焦于:靶向肿瘤细胞和TI-Tregs共同的代谢靶点;利用多组学剖析Treg的代谢;干扰Treg稳态和表型转化相关的靶标;通过药物组合进行更多的临床研究,以期通过将免疫代谢与免疫治疗相结合的方法来帮助克服免疫治疗中的代谢障碍。
本文参考文献(上线划动查看)
1. Stine, Z.E. et al. (2022) Targeting cancer metabolism in the era of precision oncology. Nat Rev Drug Discov 21, 141-162. 10.1038/s41573-021-00339-6
2. DePeaux, K. and Delgoffe, G.M. (2021) Metabolic barriers to cancer immunotherapy. Nature reviews. Immunology 21, 785-797. 10.1038/s41577-021-00541-y
3. Elia, I. and Haigis, M.C. (2021) Metabolites and the tumour microenvironment: from cellular mechanisms to systemic metabolism. Nat Metab 3, 21-32. 10.1038/s42255-020-00317-z
4. Artyomov, M.N. and Van den Bossche, J. (2020) Immunometabolism in the Single-Cell Era. Cell Metab 32, 710-725. 10.1016/j.cmet.2020.09.013
5. Bader, J.E. et al. (2020) Targeting Metabolism to Improve the Tumor Microenvironment for Cancer Immunotherapy. Mol Cell 78, 1019-1033. 10.1016/j.molcel.2020.05.034
6. Shan, F. et al. (2022) Therapeutic targeting of regulatory T cells in cancer. Trends Cancer 8, 944-961. 10.1016/j.trecan.2022.06.008
7. Lu, L. et al. (2017) The regulation of immune tolerance by FOXP3. Nat Rev Immunol 17, 703-717. 10.1038/nri.2017.75
8. Angelin, A. et al. (2017) Foxp3 Reprograms T Cell Metabolism to Function in Low-Glucose, High-Lactate Environments. Cell Metab 25. 10.1016/j.cmet.2016.12.018
9. Watson, M.J. et al. (2021) Metabolic support of tumour-infiltrating regulatory T cells by lactic acid. Nature 591, 645-651. 10.1038/s41586-020-03045-2
10. Lim, S.A. et al. (2021) Lipid signalling enforces functional specialization of T cells in tumours. Nature 591, 306-311. 10.1038/s41586-021-03235-6
 论文作者介绍
论文作者介绍 吕凌
吕凌主任医师
吕凌
主任医师,教授,博士生导师。南京医科大学第四临床医学院院长,南京医科大学第一附属医院(江苏省人民医院)(大)外科行政副主任。获国自然优秀青年科学基金、中国科协求是杰出青年成果转化奖、转化医学创新奖。入选国家百千万人才工程、科技部863青年科学家计划、江苏省“333工程”第一层次培养对象。任中国生物医学工程学会免疫治疗工程分会主任委员、江苏省研究型医院学会会长。以第一完成人获得江苏省科学技术奖一等奖、中华医学科技二等奖、江苏医学科技奖一等奖。2014-2022连续入选爱思唯尔中国“高被引学者”榜单。主要成果发表于Nat Rev Immunol、 Cancer Discov、 J Hepatol、 Gut、 Hepatology、 EMBO J、 PNAS、 Blood、 Cell Mol Immunol、 Cell Rep等。
 古鉴
古鉴主治医师
古鉴
主治医师,副教授,硕士生导师。2016年获得南京医科大学普通外科学博士学位。2020年至今任南京医科大学第一附属医院(江苏省人民医院)肝移植外科主治医师。2018年获国自然青年科学基金,2022年获国自然面上基金。入选江苏省“333工程”第三层次培养对象。任中国生物医学工程学会免疫工程分会青年委员会副主任委员、中国生物医学工程学会免疫工程分会副秘书长、中国免疫学会青年委员会委员。曾获2016年江苏省医学科技奖青年科技奖(排名第一),2017年南京市科技进步奖一等奖(排名第二)。主要成果发表于Cell Mol Immunol、 Cell Rep、Cell Death Dis、Front Oncol等。
相关论文信息
相关研究发表在Cell Press细胞出版社旗下期刊Trends in Immunology
▌论文标题:
Targeting the metabolism of tumor-infiltrating regulatory T cells
▌论文网址:
https://www.cell.com/trends/immuno-logy/fulltext/S1471-4906(23)00109-6
▌DOI:
https://doi.org/10.1016/j.it.2023.06.001
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




