- +1
急性脑卒中CT灌注成像的技术实现
原创
CT灌注(CTP)是一种功能性成像技术,它提供了有关脑实质毛细血管水平血流动力学的重要信息,是对非增强CT和CT血管造影在评估急性卒中、血管痉挛和其他神经血管疾病方面优势的自然补充。CTP对于确定不可逆梗死的脑组织(梗死 "核心")和严重缺血但有可能挽救的组织("半影")的范围至关重要。这是通过生成脑血流、脑血量和平均运输时间的参数图来实现的。
本综述的第一部分介绍了CT灌注(CTP)的临床背景。接下来,讨论了使用最大斜率法和2种主要的去卷积技术,即傅里叶变换和奇异值分解(SVD)(后者是CTP中最常用的数字方法)构建CTP图(参见:)。第二部分讨论了CTP图的 "珍珠和陷阱",1)采集,2)后处理,和3)图像解释。讨论的问题包括减少辐射剂量的策略、纠正动脉输入功能(AIF)延迟的方法、AIF选择的横向影响、血管像素的消除、正确的脑血流(CBF)和脑血量(CBV)阈值选择的重要性,以及选择适当的灌注参数以正确估计半影。该综述强调,需要对重要的CTP参数进行验证和标准化,以改善患者的预后,并设计未来的随机临床试验,为核心/半影 "错配 "在目前3小时的静脉溶栓治疗窗口之外的患者分流中的重要性提供证据。
技术实现
CTP采集
在最近由美国国立卫生研究院(NIH)和美国神经放射学会主办的华盛顿特区脑卒中放射学家、神经学家、急诊医生、美国国立卫生研究院(NIH)管理人员和业界领袖会议上,讨论了有关高级急性中风成像的技术和临床问题。专家们就标准化CTP和MRP采集达成共识,并在《美国神经放射学和卒中杂志》上同时发表了立场文件。增加心脏多排CT(MDCT)以检测可能的左心房附件血栓是可选的,但可能会越来越受欢迎,因为心脏栓塞性卒中约占所有缺血性卒中的三分之一(而且随着用于颈动脉栓塞性卒中一级预防的支架置入/动脉切除术越来越普遍,其发病率似乎在增加)。最近的一项研究报告称,与更具侵入性的经食道超声心动图相比,心脏MDCT的特异性为80%,敏感性为73%,阴性预测值为92%。最近的另一项研究报告称,心脏MDCT的阳性预测值为99%,阴性预测值为96%,使心脏MDCT成为综合神经血管方案中具有吸引力的组成部分。根据会议的普遍共识和机构协议,使用64排CT(LightSpeed;GE Healthcare,Waukesha,Wis)的CTP扫描参数样本见表1。
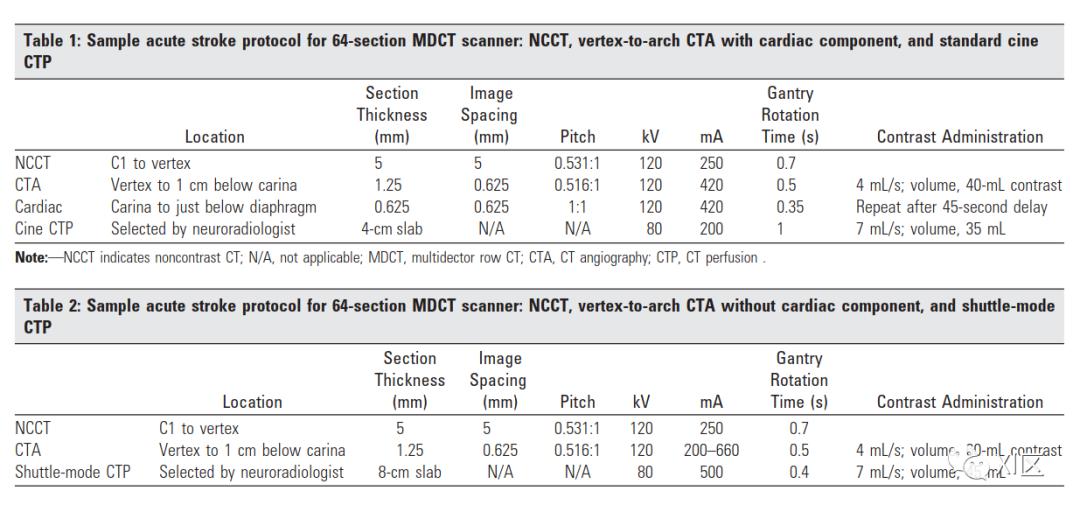 对比剂的使用
对比剂的使用对于CTP,通过动力注射器以7 ml/s的速度注射35-45 ml的造影剂,并以相同的注射速度注射20-40 ml的盐水 "追击"。使用的造影剂应该是高浓度的,最好是350-370g/dl的碘,以产生最大的峰值增强,从而为CTP图的计算提供最佳的信号强度-噪声比。
图像采集
注射后几秒钟开始在电影模式下成像(CT检查床静止)。在过去,方案的设计是在45秒内每秒获取1幅图像,主要是为了尽量减少辐射剂量。然而,这种相对较短的成像时间有可能获得不完整的组织浓度Ctissue(t)曲线,特别是在心输出量不足、心房颤动和颈内动脉近端闭塞或毛细血管腔的患者中。此外,通过时间衰减曲线(TDC)可以测量血脑屏障(BBB)的通透性,但这也需要更长的采集时间。
基于这些考虑,采集时间至少为60秒,通常为75-90秒已成为标准。然而,这样做的一个潜在问题是,延长扫描时间会增加病人的辐射量。一个解决方案是使用由2期或甚至3期组成的采集(如果需要进行渗透性成像,则采用后者)。在第一阶段,可以每秒钟采集一次图像,持续40秒。在第二阶段,可以每2-3秒采集一次图像,再持续35-45秒(总共至少75秒)。如果需要进行渗透性测量,还可以增加第三阶段,即每10-15秒采集一次图像,持续2分钟。因为造影剂增强的后期变化发生得不那么快,所以后期图像的获取频率可以低于第一阶段图像的要求。
然而,BBB破坏的严重程度已被证明与缺血性卒中的预后相关,在不久的将来,更多的常规渗透性测量有可能被纳入。同样,最近的一项研究表明,渗透性MR成像有可能确定急性缺血性卒中患者发生出血性转变的风险较高。现有的去卷积技术可以扩展到对BBB渗透性进行量化。同时,较少的取样可确保整体辐射量不会明显增加。
图像采集参数
CTP成像协议一直是在80kV下进行的,而不是更传统的120-140kV。理论上,在恒定的毫安秒(通常为200毫安)下,这种千伏设置不仅可以减少病人的辐射剂量,而且还可以增加静脉造影的明显性,部分原因是80kV光子的光电效应更为重要,因为它更接近碘的 "k边界"。
Z轴方向的覆盖范围和层厚
在首过CTP研究中,脑组织的体积受到CT探测器宽度的限制。因此,每次采集的Z轴覆盖范围取决于CT扫描仪的制造商。这种限制来自于常规的快速早期采集速度,即每秒1张图像,这使得没有足够的时间进行检查床移动。探测器的配置可以改变,以便可以同时获得一些不同的断面厚度。例如,用16排探测器的扫描仪,可以获得2cm的覆盖范围,由两个10mm或4个5mm厚的切片组成。用64排探测器的扫描仪,每次注射可以获得4cm的覆盖范围。
通过使用 "摇篮床模式 "技术,检查床来回移动,在两个不同的电影视图之间切换,尽管数据采集的时间分辨率降低,但每次注射的最大垂直覆盖度有可能翻倍。另外,可以使用2次注射来获取不同水平的2块CTP数据,使整体覆盖度翻倍,但与摇篮床模式不同,需要两倍的对比度和两倍的辐射剂量。
随着探测器阵列的扩大和技术的改进,覆盖量将继续增加。具有320排探测器的扫描仪提供了16cm覆盖的可能性。然而,准确测量CBF、CBV和平均通过时间(MTT)的最佳时间分辨率还没有解决。Wintermark等人研究了将采样间隔改为0.5、1、2、3、4、5和6秒,分别对导出的CBF、CBV和MTT参数的影响,方法是以0.5秒的间隔逐渐跳过原始图像序列中的更多图像。如果允许在1秒的图像间隔下得出的CBF、CBV和MTT参考值有10%的偏差,那么正常和缺血组织的图像间隔可以增加到2-3秒,而在量化方面没有实质性的差异。因此,采样间隔为3秒的摇篮床技术可能是一种相对直接和廉价的方法,可以将64排扫描仪的Z轴覆盖范围从4cm增加到8cm。
减少辐射剂量的策略
神经放射学家熟悉影响病人剂量的因素,如螺距、mAs、千伏峰值(kV[p])和准直,但还有其他方法可以进一步减少辐射暴露。低千伏(80 kV[p])与低毫安秒(通常为200 mAs)的组合已经被注意到,是一种公认的减少剂量的策略。(球管电流与剂量成正比,但代价是噪声增加,增加了1/√mA)。
另一种减少剂量的方法是通过降低CTP首过数据的图像采集频率。如上所述,Wintermark等人计算了缺血性卒中患者的时间采样间隔为0.5、1、2、3、4、5、6秒的图。在使用40毫升造影剂的方案中,采样间隔长达3秒,没有表现出CBF、CBV或MTT的明显高估或低估。只有当采样间隔超过4秒时,CBF和CBV被高估,MTT被低估。这些结果表明,在首过阶段,辐射剂量可以减少三分之二,而不改变CTP的定量准确性(如在摇篮床模式采集中实现)。有效辐射剂量在0.852和1.867 mSv之间变化,取决于扫描协议。使用两个40毫升造影剂的电影模式和使用一个60毫升造影剂的摇篮床模式技术的剂量最低。
为了正确看待上述剂量范围,在一台标准的64排CT扫描仪上,轴向获取的头部CT的有效辐射剂量通常为3.2mSv。作为比较,一个在波士顿生活了一年的人的背景辐射约为3mSv,或约为1次标准头部CT的剂量。在我们机构进行的4厘米覆盖率、1幅图像/秒、单次团注标准CTP的辐射量约为3.7mSv或略高于1次标准头部CT。摇篮床模式可提供两倍的覆盖范围,但总剂量却大大降低,因为我们每3秒成像一次,持续75-90秒。
后处理
一般原则
在CTP数据采集之后,源图像通常被转移到一个独立的工作站,以处理成参数化伪彩图。有多个厂家的软件包能够进行这种处理。尽管其中一些软件包是根据最大斜率法处理伪彩图的,但由于前面概述的原因,越来越多的基于去卷积的软件被使用。后处理可以是手动的、半自动的或全自动的。CTP图计算所需的输入包括AIF和静脉输出功能(VOF)。一些软件包还结合了图像处理算法,自动识别一系列组织和血管结构,这一过程被称为 "图像分割"。通过图像分割,使用基于衰减测量的阈值,非脑组织,如脑沟、动脉和静脉,很容易从CTP图中去除。灰质的测量值一般为30-40HU,白质为20-30HU;去除<0HU或>60-80HU的像素可以有效地消除CT平扫图像中的骨、脂肪和空气。
选择AIF时,可在操作者放置的较大兴趣区域内确定一个像素子集,以包括候选动脉。重要的是尽量选择与成像平面正交的血管,以减少容积平均。接下来选择一个感兴趣的静脉区域,作为静脉输出功能。静脉输出函数的目的是作为CTP定量参数值归一化的参考,相对于非容积平均的最大血管内对比度测量。因为静脉(尤其是后上矢状窦)通常比动脉大,静脉TDC不像动脉TDC那样受部分容积平均化的影响。如前所述,准确的CTP定量需要选择适当的静脉流出区,有足够的对比剂 "洗入 "和洗出,作为CTP参数值的正常化或比例因子。通过比较静脉和动脉TDC的面积,可以纠正动脉TDC的部分容积平均化。根据这些选择对原始数据进行处理,可以得到CBV、CBF和MTT的定量参数图,其原理参见:。
外周血管和船只动脉应从CTP图中排除,因为它们可能模拟出脑组织内虚假的高灌注区域。Kudo等人评估了CTP成像中与正电子发射断层成像(PET)相比,血管像素消除的效果。任何CBV值高于8 mL/min阈值的像素都被标记并从CBF计算中消除。当CBV值高于该阈值的像素被消除后,CT-CBF和PET-CBF测量的相关性明显提高。当皮质灰质的CBF定量值受到关注时,血管像素的消除似乎特别有用。这种方法消除了在蛛网膜下腔沟中几乎总是存在的脑膜血管,从而防止了CBF的高估。
纠正AIF的延迟和扩散的方法
CBF的计算需要对AIF的了解,在实践中,人们从一条大动脉上估计,假设它代表了对感兴趣的组织体素的准确和唯一的输入,既没有延迟也没有扩散。然而,在一些临床情况下,AIF的TDC会滞后,而组织TDC会滞后于AIF曲线("延迟";图1)。AIF延迟可能是由于颅外原因(心房颤动、严重颈动脉狭窄、左心室射血分数低)或颅内原因(近端颅内梗阻性血栓且通畅性差)。此外,在这种情况下,形成AIF的造影剂可以在感兴趣的组织区域附近的多个途径上扩散。延迟和扩散可导致严重低估CBF和高估MTT。
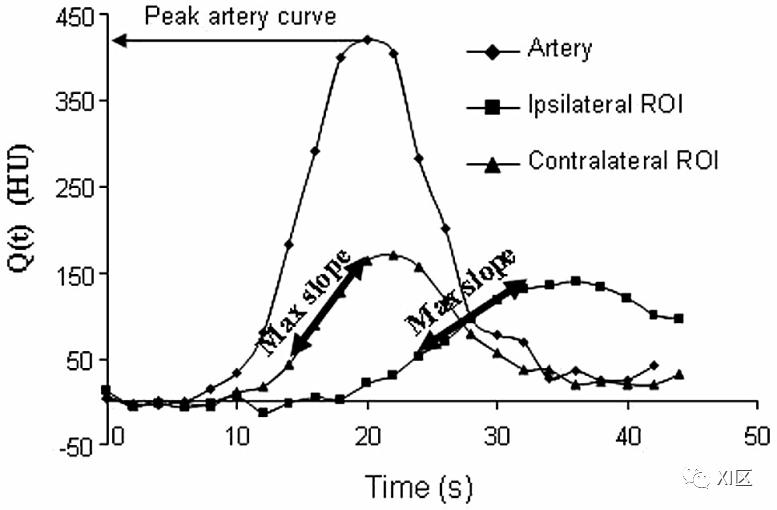 图1 最大斜率法。CBF可以从Q(t)的最大斜率(Max Slope)与最大动脉浓度的比率来计算。对侧感兴趣区(ROI)(即没有中风的感兴趣区)的最大斜率越高,CBF就越高,而同侧感兴趣区的CBF会降低。
图1 最大斜率法。CBF可以从Q(t)的最大斜率(Max Slope)与最大动脉浓度的比率来计算。对侧感兴趣区(ROI)(即没有中风的感兴趣区)的最大斜率越高,CBF就越高,而同侧感兴趣区的CBF会降低。在SVD方法中,有几种方法被用来减少延迟和扩散的影响。值得注意的是,虽然傅里叶技术对延迟不敏感,但对噪声非常敏感,因此不适合CBF计算。Wu等人报告了一种示踪剂到达时间不敏感的技术,使用SVD与块环状分解矩阵。研究者取消了SVD中的因果关系假设(即感兴趣的组织信号强度不能在AIF之前到达)。如果AIF是从病变血管测得的,这当然是可能的。因此,计算出的R(t)会因时间延迟而发生偏移,但如果假设有因果关系,R(t)就不能通过去卷积方程13正确估计。然而,通过使用圆形而不是线性去卷积(标准SVD),现在可以表示计算出的R(t),R(t)被时间延迟循环移位了。换句话说,循环去卷积避免了线性去卷积的时间混叠。
块状环形去卷积被证明对数字模拟和临床获得的数据都不敏感。最重要的是,当没有示踪剂到达时间差异时,环形去卷积的表现与标准SVD相当。最近一项对大面积脑梗塞患者的研究证实,环形去卷积优于线性去卷积。此外,采用大于2秒的成像采集间隔,在不降低信号强度-噪声比的情况下降低了辐射暴露。日本急性中风成像标准化(ASIST)小组成员目前正在与分析软件供应商合作,在其商业系统中实施块环形去卷积(http://plaza.umin.ac.jp)。
另一种延迟校正的方法是使用从更接近相关组织的小血管中估计的局部AIF。最初尝试测量局部AIF时,由于部分体积的影响,出现了问题。最近,MRP的局部AIF自动选择算法取得了很好的效果,但在CTP方面还缺乏经验。另外,独立成分分析也可作为定义局部AIF的工具。独立分量分析可用于识别空间独立模式,其基础是假设感兴趣的信号可被分解为统计学上独立分量的线性组合。Calamante等人对这种方法进行了全面描述,并将其与各种脑血管异常患者的MRP成像数据中的全局AIF的传统方法进行了比较。与全局AIF方法相比,独立成分分析方法在AIF失真的区域产生了更高的CBF和更短的MTT值,表明延迟和扩散的影响被最小化了。此外,独立成分分析由于其 "去噪 "能力而显示出更好的信噪比。
然而,另一种方法是通过曲线拟合确定AIF(t)和Ctissue(t) TDCs之间的相对时间差。Ibaraki等人使用逐个像素的最小二乘法拟合作为SVD去卷积前的初始准备步骤。只对AIF(t)峰之前的数据进行拟合以确定延迟,因为数据的 "尾巴 "部分反映了对比剂的组织通过,而不是示踪剂到达的时间。还有一种方法是将延迟的估计直接纳入去卷积算法中。后面这两种方法比循环去卷积和独立成分分析更容易实现。这些延迟校正技术已经成功地纠正了SVD去卷积所固有的CBF的低估问题。为确保CTP图计算的可重复性和可靠性,需要将稳健的AIF延迟校正纳入市售CTP软件并使之标准化(图2)。到目前(2009年)为止,只有极少数的厂商推出了这样的后处理软件,尽管如前所述,这是一个快速变化的领域,厂商经常发布新的软件(见ASIST-Japan网站:http://plaza.umin.ac.jp)。
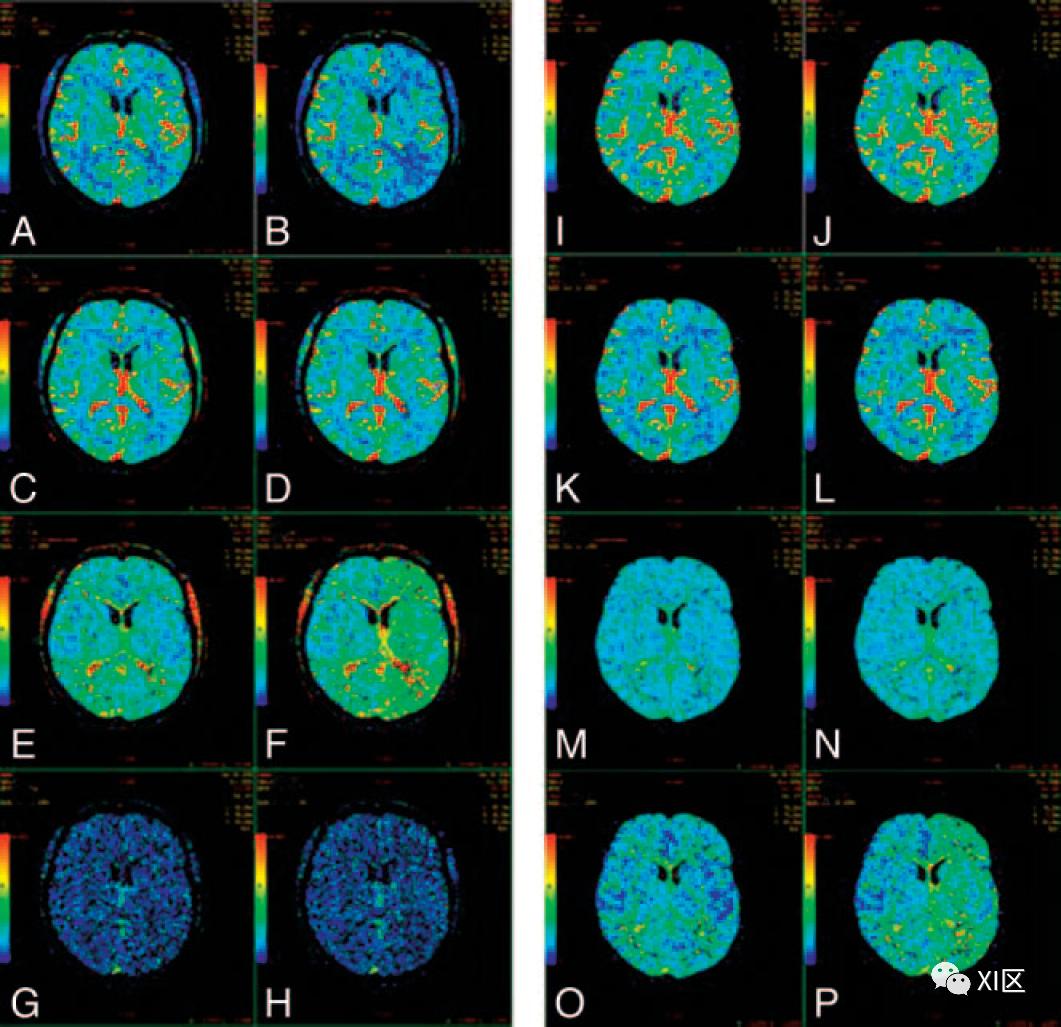 图2 A-H,通过使用延迟敏感的去卷积算法计算的CTP图,该算法受动脉输入和组织曲线之间的延迟(To)影响。为了模拟一定范围内的To,我们对一个脑瘤患者的CTP研究中的单个切片的动态图像进行了处理,使整个左半球的时间-增强曲线相对于右半球的时间向前移动了2秒。然后用Perfusion 3 (GE Healthcare)处理原始和时间偏移的CTP研究,使用相同的动脉输入曲线和右半球的静脉曲线。A和B,原始和To=2秒研究的CBF图。C和D,相应的CBV图。E和F,相应的MTT图。G和H,相应的To图。随着To的增加,CBF减少,MTT增加,而CBV保持不变。去卷积算法不能估计To。I-P,通过使用延迟不敏感的去卷积算法计算的CTP图,该算法不受动脉输入和组织曲线之间的To影响。I-P的原始和时移CTP研究的处理方式与A-H相同,只是使用了延迟不敏感的去卷积算法(Perfusion 4,GE Healthcare)。I和J,原始和To=2秒研究的CBF图。K和L,相应的CBV图。M和N,相应的MTT图。O和P,相应的To图。随着To的增加,CBF和CBV保持相对不变,MTT略有增加。去卷积算法能够检测到To的增加,但对To的估计并不准确。
图2 A-H,通过使用延迟敏感的去卷积算法计算的CTP图,该算法受动脉输入和组织曲线之间的延迟(To)影响。为了模拟一定范围内的To,我们对一个脑瘤患者的CTP研究中的单个切片的动态图像进行了处理,使整个左半球的时间-增强曲线相对于右半球的时间向前移动了2秒。然后用Perfusion 3 (GE Healthcare)处理原始和时间偏移的CTP研究,使用相同的动脉输入曲线和右半球的静脉曲线。A和B,原始和To=2秒研究的CBF图。C和D,相应的CBV图。E和F,相应的MTT图。G和H,相应的To图。随着To的增加,CBF减少,MTT增加,而CBV保持不变。去卷积算法不能估计To。I-P,通过使用延迟不敏感的去卷积算法计算的CTP图,该算法不受动脉输入和组织曲线之间的To影响。I-P的原始和时移CTP研究的处理方式与A-H相同,只是使用了延迟不敏感的去卷积算法(Perfusion 4,GE Healthcare)。I和J,原始和To=2秒研究的CBF图。K和L,相应的CBV图。M和N,相应的MTT图。O和P,相应的To图。随着To的增加,CBF和CBV保持相对不变,MTT略有增加。去卷积算法能够检测到To的增加,但对To的估计并不准确。当存在颅内或颅外循环障碍的原因时,延迟校正尤为关键。最近的一项研究发现,在极少数病例中,溶栓后的最终梗死面积似乎小于使用老一代延迟敏感软件计算的入院核心CBV病变大小所预测的面积。在使用最新的延迟不敏感软件重新计算时,最初的11个可逆CBV病变中只有2个是真正可逆的,这表明CBV梗死核心的真正可逆性是极其罕见的。值得注意的是,延迟敏感软件根据中心容积定理(CBV=MTT×CBF)从MTT和CBF计算CBV;而MTT和CBF又是通过使用去卷积算法得出的,没有上述任何延迟校正策略。因此,大多数明显的CT-CBV可逆性的情况(这种情况很罕见)实际上是假性可逆的,可能是由于CTP图后处理中缺乏延迟校正而引起的技术问题。
选择AIF的侧向性的影响
关于AIF应该选择在受累半球的同侧还是对侧,目前还没有达成普遍共识,据我们所知,很少有研究涉及这一争议,不过未来使用标准化的延迟校正后处理软件应该会使这一问题失去意义。有些人认为,大多数灌注模型所依据的假设,最好是选择2个AIF--左半球的AIF和右半球的AIF。
Sanelli等人在3名患者的梗死核心区构建CTP图,并报道CBF、CBV和MTT值与AIF选择的感兴趣区域的位置和大小无关。选择颅内近端大动脉与梗死同侧或对侧较小的远端动脉并不影响所得的定量灌注值。最近一项对18例急性卒中患者的研究也报道了同侧和对侧AIF的选择,梗死核心和半影CBV和CBF值有明显的相关性。用不同AIF得到的梗死核心MTT值的相关性低于CBF和CBV,但不明显;半影的MTT值没有明显相关性。值得注意的是,在上述两项研究中,没有专门研究因严重狭窄或心房颤动而出现大量延迟的AIF。
有学者对14名急性卒中患者的CTP图用延迟不敏感的软件处理后,未发表的数据也表明AIF感兴趣区域的横向性对梗死核心区的CBV、CBF和MTT值没有明显影响。使用基于CTP软件的延迟校正去卷积来选择AIF,与使用标准的现有MRP软件相比,对侧向的敏感度较低,后者通常不进行延迟校正。从梯度回波MR成像源图像中选择最佳AIF的固有困难也可能增加了用MRP可靠测量灌注参数的不精确性。此外,由于迄今为止,CTP是美国食品和药物管理局批准使用的碘化CT对比剂的 "标签"(“on label”),而MRP仍然是钆剂的 "非标签"(“off label”),因此可以理解,人们对开发CTP而不是MRP商业软件包更感兴趣。
卒中CTP的全自动处理
最近发布的软件分析包可以可靠而快速地完全自动构建CTP图,从而实现真正的一键式交钥匙功能。我们初步评估了一个这样的系统,从20名急性卒中患者身上构建CTP图,首先是手动,然后是自动(Perfusion 4; GE Healthcare)。在正常组织中对灰质和白质感兴趣的区域进行了采样,并对CBV、CBF和MTT进行了定量测量。总的来说,人工构建的彩图和自动处理的彩图之间有很好的一致性,除了白质CBF值的最小分歧。CTP图的自动处理有可能对急诊中风患者的分流有实际价值,因为它更快、更容易,而且可能与人工构建的彩图一样准确。
CTP定量值的精确度与后处理程序的可重复性直接相关。大多数市售的CTP后处理软件要求操作者主观选择感兴趣的区域并定义参数,然后应用于生成CBV、CBF和MTT图的计算。最近的一项研究报告称,不同经验的技师处理的CTP数据的变异性分别为CBV、CBF和MTT的31%、30%和14%。40 AIF感兴趣区域、静脉功能感兴趣区域和预增强间隔(另一个用户定义的参数,描述造影剂到达前应用TDC的基线)的选择是非常可重复的。技术人员在选择增强后间隔(用于定义再循环等因素)方面有很大不同。在这方面,如上所述,对中风CTP图进行全自动处理,有可能提高CBF和CBV测定的精度和准确性。
CTP图的图像解释,挑战和局限性
CBF和CBV的阈值
有证据表明,通过对CBF和CBV值应用阈值,可以实现梗死核心区和半影区的区分。缺血核心区的两个参数都有相应的下降,而半影区表现为CBF减少,CBV保持,甚至相对于正常对侧值升高。半影中CBV的维持可归因于毛细血管前动脉的扩张和静脉因灌注压下降而充血。缺血核心中CBF和CBV的匹配性降低被认为是由于严重灌注不足导致的自动调节失败。为了定义半影区和缺血核心,必须选择CBF和CBV的阈值。
关于这些操作上定义的核心区和半影区的阈值,虽然还没有达成共识或高水平的证据,但目前的专家意见倾向于使用相对的而不是绝对的CTP值,因为CTP图谱参数的绝对量化有可能出现变异,而且这些值取决于适当的但往往是任意的VOF比例系数。
在一项关于梗死的CTP阈值的试验研究中,我们发现,半影中CT-CBF减少<50%,区域存活的概率很高,而半影比基线值减少>66%,梗死的概率很高。没有绝对CBV<2.2毫升/100克的区域存活。后者与Wintermark等人选择的定义核心区的CBV阈值2.0毫升/100克非常吻合。然而,由于灰质和白质的CBV和CBF的基线值不同(灰质CBV∼4 mL/100 g/min,白质CBV∼2 mL/100 g/min;灰质CBF∼40-60 mL/100 g/min,白质CBF∼20-30 mL/100 g/min),用于正常化的对侧感兴趣区域与同侧缺血区域的灰质/白质比率相同至关重要。
尽管绝对阈值存在这些潜在的问题,但它们在一些中心的应用取得了良好的效果,尤其是在核心CBV评估方面。对130名疑似急性缺血性卒中患者进行的接收操作特征曲线分析表明,相对MTT是最能准确描述可救治半影的CTP参数,而绝对CBV是最能准确描述入院时梗死核心的参数,最佳阈值同样为2.0mL/100g。
另一种确定灰质半影和核心的阈值的方法与以前的工作不同,因为它包含了CBF和CBV之间的相互作用。Logistic回归适用于闭塞血管再通的患者的数据点,以定义分离核心和半影的阈值。由于梗死区的CBF略低,CBV远低于半影组织,所以当基于两个值的乘积(CBF×CBV)的阈值作为判别因素时,梗死区和半影区之间的分离达到最大化。CBF×CBV使梗死和半影之间的分离明显优于单独的CBF或CBV,这表明梗死的CBV阈值随CBF而变化。未来的前瞻性研究将确定这种方法的临床效用。同一研究小组将这一方法应用于白质,对梗死和半影进行了同样好的分离。
定义可挽救的半影的最佳灌注参数是什么?
CBV、CBF和MTT的计算需要离线处理,通常需要去卷积,而其他参数可能需要不太复杂的数据处理,尤其是MRP,通常在扫描仪上就能获得。峰值时间(TTP)提供了对转运时间的测量,正如其名称所示,通过对TDC的直接分析来计算。造影剂通过大脑所需的时间延长,MTT和TTP延长,是缺血组织的一个常见发现。然而,MTT和TTP延长也可能是缺血的假阳性,在严重的颅外颈动脉狭窄/闭塞或因心房颤动或射血分数低导致的颅内血流延迟的情况下,会出现少血症和低灌注,但不是真正的缺氧。
迄今为止,不同的中心采用不同阈值的灌注参数进行半影评估,可能会导致对异常灌注的不同估计和不同的病人管理决策。这种差异性需要在明确的试验中加以解决,验证最佳的后处理和图像解释程序,然后在不同的中心实现方法的标准化。
迄今为止,已发表的调查各种灌注图的研究对预测结果的最佳入院半影参数有时得出不同的结论。两项MRP研究报告称TTP与基线NIH卒中量表(NIHSS)评分相关,一项研究认为MTT与Scandinavian卒中量表评分相关,两项研究报告MTT与NIHSS评分相关,三项研究报告MTT与60天或90天后续T2病变相关,Kane等人(2007)的最新报告通过对32例急性缺血性卒中患者的10种不同MRP处理方法进行比较解决这一问题。不同的灌注参数对同一患者的相同数据产生了非常不同的异常灌注估计,因此,对半影体积的估计也不同。所有5种MTT指标都与基线NIHSS评分和最终梗死面积有关;其中1种MTT指标是拟合到达时间,这也与临床结果有关。我们亟需在其他数据集中验证这些发现,以便就哪些灌注措施和处理方法应常规使用达成共识。
最后,关于CTP图像的显示,日本的ASIST小组主张用自动色标显示取代依赖操作者的色标调整,以尽量减少对灌注图视觉解释的变化。
临床意义
灌注成像对缺血核心区和半影区的鉴别能力在目前和未来的临床试验中非常重要。目前有很好的二级证据表明,核心区/半影区的不匹配将对中风再通疗法的患者选择非常重要,超过了目前静脉溶栓术后3小时和动脉内溶栓术后6小时的任意界限。
最佳的采集需要至少60-75秒的扫描时间,以及最大限度地覆盖Z轴的策略。在目前由CT平扫、CTA和CTP组成的综合神经血管方案中,增加心脏MDCT部分来评估心源性中风是一个很有吸引力的补充。
最佳的后处理可通过非参数去卷积技术实现,如SVD。用现有的几种方法中的一种进行血管像素消除和栓塞-示踪剂延迟校正,可能会被证明是后处理优化的关键,而随着延迟校正后处理软件的广泛应用,AIF的侧向选择不太可能是一个重要的考虑。
最佳的图像解释需要选择适当的CBV和CBF阈值,并选择最合适的灌注参数来操作定义半影。这是一个有争议的话题;尽管最近的研究表明,到达时间拟合的MTT图与临床和放射学结果有很好的相关性,但仍有许多工作要做,以使灌注成像 "准备就绪 "。核心区和半影区的相对或绝对CTP阈值是否最佳,以及这种区分的重要程度也是一个未解决的问题。
CTP方法的验证和标准化对于在选择新的卒中治疗方法的病人时广泛接受先进的成像技术至关重要。2007年秋季在华盛顿举行的急性卒中治疗高级神经影像学会议上,专家们已经就CTP图像采集的标准化达成了共识。然而,该小组和日本的ASIST小组都强调继续需要对市售的CTP后处理软件进行明确的优化和验证,特别是在去卷积方法和延迟校正的必要性方面。
一旦实现验证,标准化将最大限度地减少观察者之间和医院之间在选择病人接受新疗法时的差异性,包括在目前公认的时间窗之外的溶栓治疗。当然,使用先进的灌注成像改善患者预后的一级证据是最终目标。CTP采集、后处理和解读技术的标准化可能会促进未来的随机对照试验,从而提供CTP错配在患者选择下一代新型卒中疗法中具有价值的I级证据。
更多干货,关注XI区!
编译整理自:Konstas AA, Goldmakher GV, Lee TY, Lev MH. Theoretic basis and technical implementations of CT perfusion in acute ischemic stroke, part 2: technical implementations. AJNR Am J Neuroradiol. 2009 May;30(5):885-92. doi: 10.3174/ajnr.A1492. 仅供专业人士交流目的,不用于商业用途。
2023年12月22日
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




