- +1
【学术前沿】Cell Stem Cell | 陈水冰等利用胰腺癌类器官平台筛选靶向突变 KRAS …
胰腺导管腺癌 (PDAC) 有着“癌王”之称。因缺乏特异的筛查和诊断指标,许多患者在发现之初就已经失去了手术的机会。大规模基因组研究发现超过 90% 的 PDAC 存在 KRAS 驱动突变。突变的KRAS与胰腺肿瘤的增殖、迁移、转化、存活、逃避肿瘤免疫以及细胞代谢重编程都存在密切联系。在 PDAC 中,KRAS 蛋白的12号氨基端是最常受累的突变位点,其中以KRASG12D 突变类型最为常见,其次是 KRASG12V。长期以来,肿瘤驱动基因KRAS一直被认为是“不可成药”的靶标,直到最近几款针对 KRASG12C 突变的特异性抑制剂的研发,这一领域才迎来突破性进展,包括 AMG510 (sotorasib)、MRTX849 (adagrasib)、MTRX1257、ARS-853 和 ARS1620。在这些药物中,AMG510 和 MRTX849 已获批进去临床,显示对非小细胞肺癌患者有一定疗效作用,但反应有限且很快产生耐药性,中位无进展生存期分别约为 6 至 11个月。与KRASG12C相比,针对KRASG12D或KRASG12V的可选择药物则更加有限。其中仅有选择性靶向 KRASG12D的MRTX1133进入1期临床实验。除此之外,科学家发明了新的靶向策略,选择性共价抑制剂通过与激活状态的KRAS以及亲环素A之间形成稳定的、高亲和力的三复合物,从而干扰KRAS与RAF激酶等下游效应蛋白的相互作用。采用这一策略的共价抑制剂有KRASmulti (RMC 6236)、KRASG12C (RMC 6291)、KRASG12D (RMC 9805) 和 KRASG13D (RMC-8839)。其中,RMC 6236 (NCT05379985) 和 RMC 6291 (NCT05462717) 已进入 1 期临床试验。然而,这些候选药物都尚未使用等基因癌症模型进行验证。
肿瘤类器官已成为临床前与癌症转化研究的强大工具。FDA 也批准使用类器官模型来代替体内小鼠模型,这进一步强调了类器官在未来对药物研发的重要性。2023年12月26日,来自美国康奈尔医学院的陈水冰团队在Cell Stem Cell 杂志上发表题为 A Pancreatic Cancer Organoid Platform Identifies an Inhibitor Specific to Mutant KRAS的文章。他们开发了一组等基因小鼠胰腺类器官平台,其中包含常见的 PDAC 驱动突变 KRASG12D、Tp53R172H 和 SMAD4 缺失。基于这一胰腺类器官筛选了约 6000 种化合物,并鉴定出了 Perhexiline maleate,它可在体外和体内特异性抑制携带 KRASG12D 突变的 PDAC 类器官的生长。进一步研究表明Perhexiline maleate 通过下调 SREBP2 的表达来抑制胆固醇代谢途径,从而逆转KRAS突变诱导的PDAC 类器官的代谢重编程。该研究为筛选靶向胰腺癌的抑制剂提供了强有力的研究工具,同时鉴定了SREBP2是胰腺癌治疗的潜在靶点。
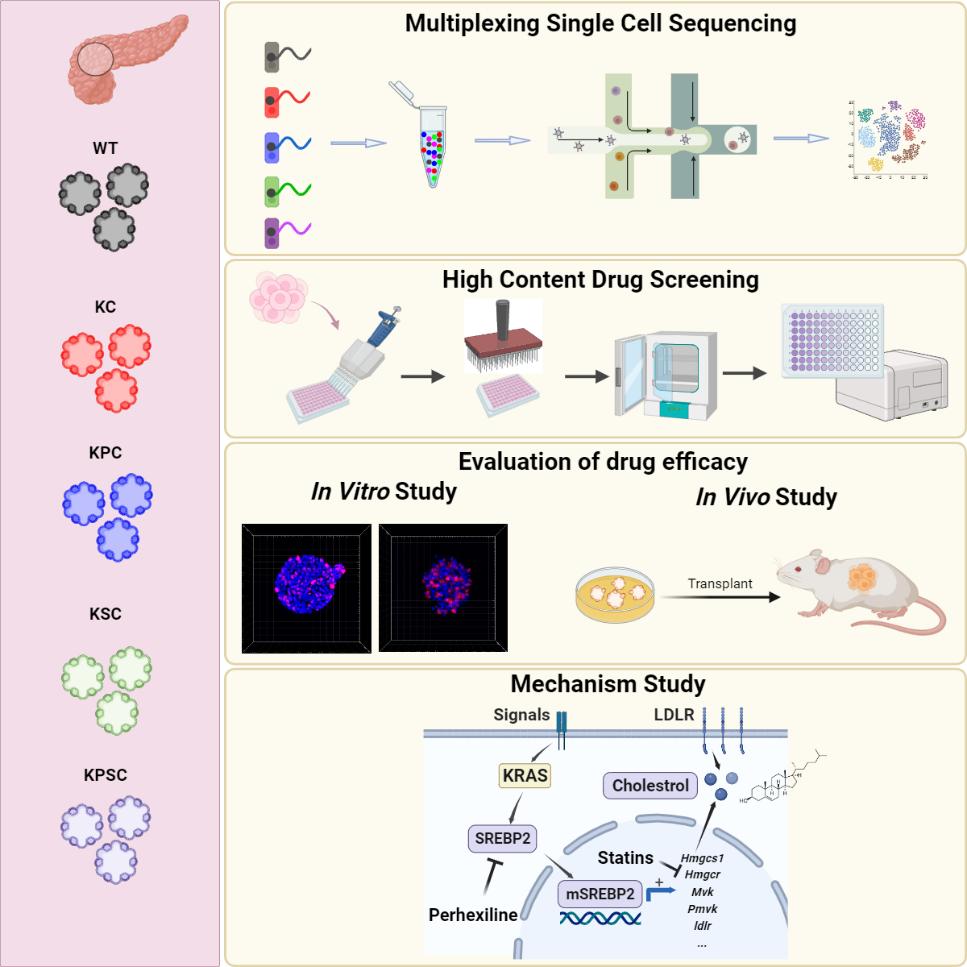
 研究者利用类器官培养技术与CRISPR/Cas9技术相结合,在实验室构建了一套等基因胰腺类器官平台,野生型胰腺类器官 (WT);Pdx1-Cre,KrasLSL-G12D/+ 类器官 (KC);Pdx1-Cre,KrasLSL-G12D/+,Tp53LSL-R172H/+ 类器官 (KPC);Pdx1-Cre,KrasLSL-G12D/+,Smad4-/- (KSC) 与 Pdx1-Cre,KrasLSL-G12D/+,Tp53LSL-R172H/+,Smad4-/- (KPSC)。他们利用多重单细胞 RNA-seq (multiplexing scRNA-seq) 技术对 WT、KC、KPC、KSC、KPSC 类器官的转录组进行了表征,以监测胰腺癌驱动突变引起的转录变化。通过无监督数据分析和条形码投影识别的细胞簇匹配良好,这表明细胞簇的基因特征主要受基因型影响。接下来,作者研究了胰腺细胞谱系的转录因子谱,包括导管谱系、外分泌谱系(腺泡)和内分泌谱系。结果表明胰腺癌类器官主要表达胰腺导管细胞标记基因。除此之外,为了在单细胞水平上阐明肿瘤分子亚型,作者利用 SCENIC 同时重建基因调控网络并识别 KSC、KPC 和 KPSC 细胞状态。结果显示在 KSC 类器官中鉴定出类似基底细胞亚型(basal-like)的调节子(regulons),包括 Myc、Est1、Hmga2 和 Zeb1。以往的研究表明,Gata6 表达与 PDAC 中的经典亚型(classical)相关。他们的研究结果也表明Gata6、Sox9、Hnf1b 和 Onecut2 是 KPC 和 KPSC 类器官中的主要表达的regulons。然而,一些basal-like regulons,包括 Nr3c1、Mxi1、Taf1、Klf7、Fosl1,也可以在 KPC 和 KPSC 类器官中表达。因此,basal-like和classical两种分子亚型的表达特征可以在 KPC 和 KPSC 类器官中共存,这就赋予它们潜在的细胞可塑性。
研究者利用类器官培养技术与CRISPR/Cas9技术相结合,在实验室构建了一套等基因胰腺类器官平台,野生型胰腺类器官 (WT);Pdx1-Cre,KrasLSL-G12D/+ 类器官 (KC);Pdx1-Cre,KrasLSL-G12D/+,Tp53LSL-R172H/+ 类器官 (KPC);Pdx1-Cre,KrasLSL-G12D/+,Smad4-/- (KSC) 与 Pdx1-Cre,KrasLSL-G12D/+,Tp53LSL-R172H/+,Smad4-/- (KPSC)。他们利用多重单细胞 RNA-seq (multiplexing scRNA-seq) 技术对 WT、KC、KPC、KSC、KPSC 类器官的转录组进行了表征,以监测胰腺癌驱动突变引起的转录变化。通过无监督数据分析和条形码投影识别的细胞簇匹配良好,这表明细胞簇的基因特征主要受基因型影响。接下来,作者研究了胰腺细胞谱系的转录因子谱,包括导管谱系、外分泌谱系(腺泡)和内分泌谱系。结果表明胰腺癌类器官主要表达胰腺导管细胞标记基因。除此之外,为了在单细胞水平上阐明肿瘤分子亚型,作者利用 SCENIC 同时重建基因调控网络并识别 KSC、KPC 和 KPSC 细胞状态。结果显示在 KSC 类器官中鉴定出类似基底细胞亚型(basal-like)的调节子(regulons),包括 Myc、Est1、Hmga2 和 Zeb1。以往的研究表明,Gata6 表达与 PDAC 中的经典亚型(classical)相关。他们的研究结果也表明Gata6、Sox9、Hnf1b 和 Onecut2 是 KPC 和 KPSC 类器官中的主要表达的regulons。然而,一些basal-like regulons,包括 Nr3c1、Mxi1、Taf1、Klf7、Fosl1,也可以在 KPC 和 KPSC 类器官中表达。因此,basal-like和classical两种分子亚型的表达特征可以在 KPC 和 KPSC 类器官中共存,这就赋予它们潜在的细胞可塑性。随后,为了识别针对 KRASG12D 突变的小分子抑制剂,作者利用上述平台筛选了约 6000 种 化合物,包括FDA 批准的药物、信号通路抑制剂和天然产物库等。经过几轮筛选与验证,作者最终聚焦在了Perhexiline maleate这一小分子上。体外实验表明Perhexiline maleate可以有效KC、KPC、KSC 和 KPSC 类器官细胞生长,而WT 类器官生长影响较小。体内原位移植瘤药效评价模型也表明Perhexiline maleate可抑制肿瘤生长,同时与FOLFIRINOX有一定联合治疗效果。
接下来,作者在人源胰腺癌类器官、大肠癌类器官、肺癌类器官对Perhexiline maleate的抗肿瘤作用进行了测试。结果表明Perhexiline maleate可以抑制携带 KRASG12V 突变的胰腺癌类器官WCM744和 WCM773的活力。除此之外,对于两种携带 KRASG12D 突变的 WCM2326 和 WCM2171 PDAC 类器官,Perhexiline maleate也表现出类似的抑制作用。随后,他们探讨了Perhexiline maleate对具有不同 KRAS 状态的大肠癌类器官的影响,包括 KRASWT (WCM392)、KRASG12D (WCM1403) 和 KRASG12C (WCM1050)。同样,他们评估了其对携带 KRASG12C (WCM1712)、KRASG12D (WCM2332) 和 KRASG12V (WCM2363) 突变的肺癌类器官的影响。研究结果表明Perhexiline maleate 可以抑制不同 KRAS 突变的多种癌症类器官,而与KRASWT 类器官相比,Perhexiline maleate对 KRASG12D KRASG12V和 KRASG12C 癌症类器官表现出较低的 IC50。这些结果表明 Perhexiline maleate 可以特异性地针对多种 KRAS 突变类型,而且KRASWT影响较小。
通过对机制的探讨,作者发现突变的 KRAS 可以活化下游 PI3K/AKT/mTOR 通路,激活胆固醇生物合成途径,从而促进致癌信号传导和肿瘤进展。而这条通路可以特异性被Perhexiline maleate所抑制。由于Srebf2 基因编码的甾醇调节元件结合蛋白 2 (SREBP2) 通过控制参与胆固醇合成和摄取的酶来调节胆固醇稳态。SREBP2 增强胆固醇生物合成基因的表达,为癌细胞提供生长优势,是胶质母细胞瘤、结肠癌和肝细胞癌等癌症的主要驱动因素, 因此,作者研究了Perhexiline maleate是否是通过调节SREBP2介导的胆固醇生物合成来发挥抗肿瘤作用。结果表明Perhexiline maleate 抑制 KPSC 类器官中 Srebf2 的转录水平,同时可以抑制胆固醇合成和摄取相关基因相关,包括 Ldlr、Hmgcs1、Hmgcr、Mvd、Fdps 等。接下来作者利用遗传学手段与化学小分子对SREBP2进行干扰,结果均表明SREBP2是胰腺癌治疗的潜在靶点。综上,致癌 KRAS 突变激活 SREBP2,导致胆固醇代谢发生重编程。积累的胆固醇反过来又通过提供能量和抵抗细胞凋亡来促进肿瘤生长。Perhexiline maleate通过降低SREBP2表达水平,逆转致癌KRAS诱导的代谢重编程,并最终抑制携带KRAS突变的胰腺癌类器官的生长。
 综上所述,作者首次利用等基因胰腺类器官平台进行了高通量药物筛选研究,最终鉴定出了 Perhexiline maleate,它可以在体外和体内抑制携带 KRAS突变的胰腺类器官以及原代人 PDAC 类器官的生长并诱导细胞凋亡。同时他们还发现胆固醇合成在 KRAS 突变类器官中特异性上调, Perhexiline maleate 可以降低 SREBP2 表达水平,从而发挥对KRAS 突变体的抑制作用。
综上所述,作者首次利用等基因胰腺类器官平台进行了高通量药物筛选研究,最终鉴定出了 Perhexiline maleate,它可以在体外和体内抑制携带 KRAS突变的胰腺类器官以及原代人 PDAC 类器官的生长并诱导细胞凋亡。同时他们还发现胆固醇合成在 KRAS 突变类器官中特异性上调, Perhexiline maleate 可以降低 SREBP2 表达水平,从而发挥对KRAS 突变体的抑制作用。康奈尔医学院Fong Cheng Pan博士, 陈水冰教授与Todd Evans教授为该论文通讯作者。康奈尔医学院段晓华博士、张拓博士和华中师范大学冯玲玲教授为该论文第一作者。
原文链接:
https://doi.org/10.1016/j.stem.2023.11.011
制版人:十一
原标题:《【学术前沿】Cell Stem Cell | 陈水冰等利用胰腺癌类器官平台筛选靶向突变 KRAS 的特异性抑制剂》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




