- +1
【学术前沿】重磅综述|衰老和寿命的演化
以下文章来源于老顽童说 ,作者老顽童说
老顽童说.
公众号致力于传播衰老相关的前沿科研进展和趣味科普,帮助大家更深入地了解衰老背后的科学故事~
 关注我们,获取更多相关资讯
关注我们,获取更多相关资讯翻译 by 张添翔、陆晓雍、方帅淇、
张彬、尹剑、马米阳
夏虫朝菌,龟鹤遐龄,大千世界中,不同生物经过千万年的演化后,形态特征不尽相同,寿命更是天壤之别。衰老是一个几乎所有生命体都将经历的过程,也同样经历了漫长的演化历程,在不同生命体中受不完全相同的机制调控。2023年11月,美国加利福尼亚大学的Peter Sudmant教授等人在Trends in Genetics上发表了题为“The evolution of aging and lifespan”的综述,讨论了衰老和寿命的演化理论,包括物种间巨大寿命差异的演化轨迹,基因组多样性,以及特定年龄选择影响和突变率在衰老与寿命演化中的作用。
衰老是所有生命体中一个几乎不可避免的历程,但是不同的物种寿命差异非常大,仅仅在脊椎动物中,不同物种的寿命长度就差了几个数量级。这种巨大的表型差异是由不同的演化轨迹和选择权衡所驱动的,并反应在生物体基因组的多样化和约束模式中。特定年龄的选择压力同样也会影响种群中的等位基因频率,从而影响疾病的易感性和特定环境的死亡风险。此外,在生殖细胞和体细胞中,产生这种遗传多样性的突变过程会受到年龄和生活史的强烈影响。在这篇文章中,作者从生物个体,种群和细胞层面讨论了目前关于衰老和寿命演化的研究进展,并强调了亟待解决的问题。
要点
不同生物寿命间的广泛差异,提供了用于探索寿命演化权衡的自然数据集。
长寿物种的比较基因组学中,几个关键通路成为热点。总体来说,与寿命较短的物种相比,这些通路受到更多的调控,且在单个类群中观察到明显的多样化选择特征。
大型队列研究表明,在人类群体中,即使是生命晚期才发挥作用的有害基因似乎也受到强烈的净化选择。
体细胞突变率与寿命成正比, 且显著高于对应的生殖细胞突变率。
极端衰老体外细胞模型的建立,正不断促进生物体衰老过程中,关键基因型-表型互作的表征。
衰老的演化理论
演化理论认为,相比于在生命晚期发挥作用的基因,衰老是对影响生命早期生存以及繁殖的基因选择压力不断增加的必然结果。这一论断建立在R. A. Fisher提出的年龄特异生殖价值概念的基础上,由Peter Medawar最先提出,这一概念模拟了个体的年龄依赖的未来遗传贡献。
实际上,许多衰老演化理论的开创性贡献都可以追溯到现代综合理论的建立者身上。Medawar的突变累积理论认为,在生命晚期阶段发挥作用的有害基因积累可能是由于自然选择在老年个体中的作用减弱(有时被称为“选择阴影”)。一个与其相似,但是不同的衰老理论——拮抗多效性理论,指出在生命早期有益,但是在生命晚期有害的基因会不断累积。这两个理论之间的关键不同在于:在拮抗多效理论中,衰老是由年轻年老个体之间演化权衡的适应性演化而来的;相比之下,在突变累积理论中,与衰老相关的等位基因在年轻个体中是中性的。虽然拮抗多效性和突变累积的相对贡献尚不明确,但不同生物体的寿命之间存在广泛而巨大的差异,这表明不同的演化情景和演化权衡可能会导致寿命长度出现截然不同的结果。Mesawar还注意到“衰老(aging)”一词的相对模糊性,即它被用来指代在生物个体中几乎任何与时间相关的变化。这与“寿命(lifespan)”和“细胞衰老(senescence)”不同,“寿命”用来指代一个生物体死亡的年龄,而“细胞衰老(senescence)”指的是随着年龄的增长而导致死亡概率增加的生物学变化。最近,几项科学技术的进展和大规模数据组的应用重新激起了人们对衰老演化和年龄结构种群遗传学的兴趣。作者强调了从对不同生物体生活史的新见解,和使人类能够鉴别衰老基因和年龄相关生物学现象的新方法(图1)。
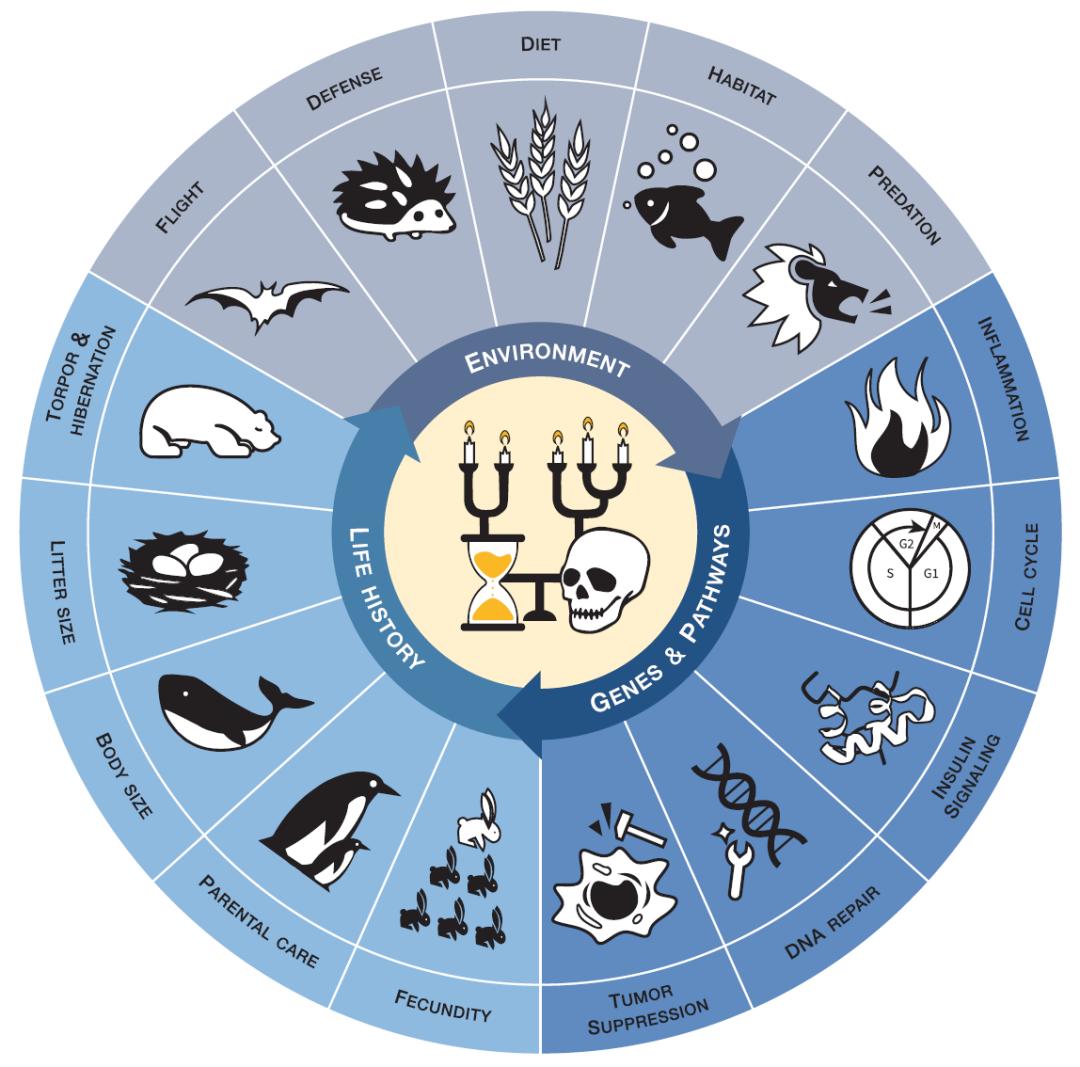 图1. 衰老和寿命背后的演化动力。基因、生命史特征和环境因素之间的相互作用驱动着衰老和寿命的演化。每个区域中重点标注的是已知的与衰老和长寿有关的几个关键因素。图片中心的图像用Vanitas风格描绘了寿命(蜡烛高度)和他们演化关系的差异。
图1. 衰老和寿命背后的演化动力。基因、生命史特征和环境因素之间的相互作用驱动着衰老和寿命的演化。每个区域中重点标注的是已知的与衰老和长寿有关的几个关键因素。图片中心的图像用Vanitas风格描绘了寿命(蜡烛高度)和他们演化关系的差异。从极端衰老动物中获得见解
长寿的生命史
演化理论预测,在低外在死亡率的情况下(即几乎没有环境死亡威胁的情况下),寿命会增加。相比之下,在高外在死亡率(例如捕食)下,生物会向短寿方向演化。寿命,以及其他许多生活史特征,倾向于表现出强烈的异速生长,即体型更大的动物寿命更长。然而,即使在控制了体型和系统发育相关性之后,寿命也会与其他生活史特征共同变化,其中大部分的差异可以通过两个独立的轴来解释。第一条是世代时间和初次生殖年龄随寿命变化的轴,而年龄特异的死亡率和生殖率沿着另一条轴同步变化。因此短寿物种倾向于身体更小,且具有更短的世代时间和成熟时间。它们还具有较高的多次生殖率,更多的子代以及高度集中的死亡风险(例如幼体存活率很低)。重要的是,这些生活史相关性意味着极端寿命可以从共同变异特征的间接选择中产生。
年龄和死亡率之间的关系通常使用Gompertz风险函数(框1)来建模,这个简单的经验模型显示死亡率随着年龄增加呈指数增长。尽管随着年龄增长死亡率逐渐增加被认为是生物体的普遍特征,但最近对陆龟、非鸟类爬行动物和两栖动物的比较研究发现,在一些情况下,衰老率可以忽略不计,甚至为负数。除此以外,其他一些物种例如石斑鱼和裸鼹鼠也被认为表现出所谓的“可忽略的衰老”。这些物种中的许多种类,尤其是鱼类,一些爬行动物和两栖动物,表现出“不确定”的生长和繁殖能力,从而为它们的长寿提供了一个关键线索:在整个生命周期中,持续的生长以及后代的繁殖会给生命晚期有害突变带来强烈的选择代价。除此之外,在石斑鱼和其他许多鱼类中,繁殖力的大小与个体体型之间不成比例,这意味着年老的,体型更大的雌鱼会比年轻的,体型较小的雌鱼产下更多后代。其他的一些与寿命相关的因素已经被确定,其中包括代谢率,温度和体温调节模式,保护性表型(例如毒素,外壳,飞行)以及性别因素。因此极端寿命在许多不同的表型轴上演化。
框1. 死亡率建模
生物体的寿命通常使用Gompertz-Makeham方程进行建模,该方程采用风险函数的形式(方程I)。
其中m(t)是死亡风险,表示在时间t时的瞬时死亡概率,m(t)dt是从t到t + dt死亡的种群比例。该方程指出,生物体的死亡概率可以通过随年龄呈指数增长的年龄相关分量(Gompertzian分量)和与年龄无关的分量(Makeham分量)来建模。参数G反映了指数死亡率系数或“衰老速率”。A0是表示内在脆弱性或初始死亡率(Initial Mortality Rate,IMR)的常数,而M0是与年龄无关的死亡率或外在死亡率(Extrinsic Mortality Rate,EMR)。由于区分IMR和EMR存在挑战,因此通常使用简化的Gompertz方程来拟合死亡率,其中M0术语被删除。生存函数S(t)(方程II)表示个体存活到时间t的概率,可以从风险函数推导出来,其形式为:
更复杂的死亡率函数,如Siler模型,允许死亡率在整个生命周期中更灵活地变化,并明确量化婴儿和生育后成人死亡率的增加。图I显示了几种不同物种的死亡率和生存曲线,包括长寿人类和超长寿岩鱼,以及表现出“负衰老”的海龟和蜥蜴。
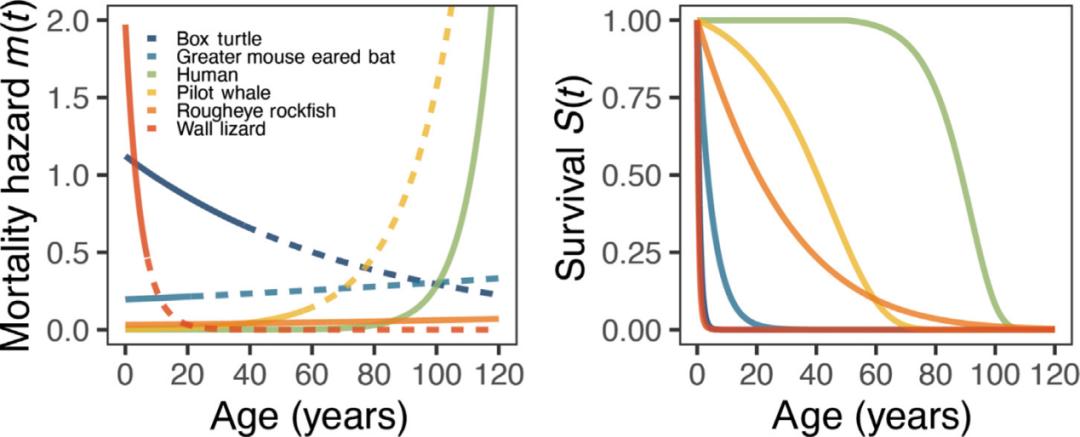 图I 六种不同物种的死亡风险(瞬时死亡概率)和生存曲线。死亡风险线在达到物种的最长寿命后被打破。
图I 六种不同物种的死亡风险(瞬时死亡概率)和生存曲线。死亡风险线在达到物种的最长寿命后被打破。死亡与性别(染色体)
寿命的性别差异在许多物种中广泛存在。有趣的是,这种效应始终有利于同配性别(即,XY系统中的雌性,如哺乳动物,以及ZW系统中的雄性,如鸟类)。事实上,最近对299个物种的比较发现,同配性别的平均寿命比异配性别长17.6%,对哺乳动物和两栖动物的深入分析也显示出类似的结果。对这种现象的一种解释,即“无保护的X假说”,认为X(或Z)染色体上的隐性突变只会在异配子环境中暴露出来。然而,群体遗传模型表明,异配性别和同配性别之间寿命差异的影响太大,无法仅通过隐性突变来解释。另一种解释是,由于重复DNA的去抑制和错误表达,Y(或Z)染色体本身会随着年龄的增长而具有毒性。最近对果蝇的研究证实了这一假说,该研究表明Y染色体拷贝数增加与寿命呈负相关。对多个分类群的进一步生物信息学分析支持了这一假设,并发现哺乳动物的Y染色体与寿命有关(尽管鸟类的Y染色体与Z或W染色体无关)。在几个物种中,异染色质随着年龄的增长而减少;而Y染色体中异染色质抑制的重复序列十分多。由于测序技术的局限性,这种重复的异染色质序列通常具有挑战性。几种新的长读长测序方法的出现有望打开这些区域,以研究具有不同寿命的物种以及单个生物体的整个生命周期。
极端长寿的比较基因组学
虽然经典模式生物(包括酵母、蠕虫、果蝇和小鼠在内)为寿命变异的分子基础提供了大量见解。但是地球上存在大量的长寿野生物种,在实验室中研究它们非常困难,而基于新的长读长测序和基因组组装方法,能采用比较基因组学的方法对它们进行研究(框2)。
框2. 比较基因组学的演化
长读长测序技术极大地重塑了现代进化基因组学方法。在过去的十年中,nanopore和PacBio测序技术的快速变革使基因组组装取得了显著进展。这些技术还使研究者们能够识别基因组中众所周知具有挑战性的区域,包括片段重复、端粒、着丝粒和其他可以跨越许多兆碱基的富含重复序列的区域。相比之下,短读长序列非常零碎且难以分析。长读方法通过直接对长度高达数兆碱基的高分子量DNA单分子进行测序来避免这些困难,从而可以覆盖上述区域。历史上只有少数物种(例如人类和小鼠)可以使用完整的参考质量基因组,并且是大规模合作努力的结果。相比之下,长读长测序以及基因组组装的最新改进使单个实验室能够贡献近乎完整的基因组。来自不同物种的完整基因组能够分析以前未表征的编码和非编码序列。通过长读长测序技术,可以首次对基因组中存在的许多结构重排进行评估:此前由于短读长组装的技术缺陷,将基因组结构变异与表型关联分析的探索仍然相当匮乏。归根结底,整个生命之树的全面比较基因组学需要所谓的端粒到端粒组装,这些组装是无间隙的,甚至可以覆盖结构上最具挑战性的基因座。然而,目前的比较基因组学依赖于组装到不同完成水平的基因组,这些基因组适合不同的比较基因组学分析(表I)。
表I. 比较基因组学和进化基因组学参考基因组资源的简要概述
 来自基因组组装的见解
来自基因组组装的见解最近已经产生了几种极端长寿的非模式物种的完整基因组,包括弓头鲸(Balaena mysticetus,>200岁)、巨龟(Chelonoidis abingdonii和Aldabrachelys gigantea,>100岁)、亚洲和非洲象(Loxodonta africana和Elephas maximus,分别为>80岁和>65岁)、裸鼹鼠(Heterocephalus glaber,>35岁)、加拿大海狸(Castor canadensis,>23岁)、Sebastes分支的几种长寿命岩鱼(100-200岁)、“永生的”刺胞动物水母(Turriitopsis dohrnii)和各种蝙蝠。对野生短寿命物种基因组的关注要少得多,但短寿命的非洲绿松石鳉鱼(Nothobranchius furzeri,4-6月龄)已成为研究衰老和假死状态的关键模式生物。对这些不同物种基因组的单独分析一再强调了关键衰老通路的选择特征,包括胰岛素信号传导、脂肪酸代谢、DNA修复、炎症、细胞周期和肿瘤抑制途径等。在长寿物种中,这些通路通常表现出正向选择的特征,突出了极端寿命所必需的演化创新。有趣的是,在短寿命的鳉鱼中,有证据表明,这些关键的年龄相关通路处于松弛约束,这是由于对具有维持和长寿作用的后期作用基因的选择压力降低。
在基因组的结构和拷贝数变化中也观察到这种特征。弓头鲸表现出与DNA损伤修复和癌症相关的基因重复,岩鱼表现出与年龄相关的嗜乳脂蛋白基因的拷贝数扩增,这些基因具有免疫抑制功能,永生的刺胞动物水母表现出与DNA修复和复制、端粒维持、氧化应激、干细胞维持和细胞间通讯相关的基因扩增,蝙蝠具有丰富的APOBEC3基因库,这些基因具有抗病毒功能,并具有已知的突变特征。相比之下,短寿命的一年生鳉鱼表现出基因组大小的增加,这归因于移动元件含量的增加,这可能是由于这些物种基因组维护的松弛选择所促进的。
来自基因组集合的见解
虽然对单个基因组的研究提供了大量信息,但对系统发育多样、相关表型差异较大的类群进行比较分析的方法也能产生独特的见解。从广义上讲,这些方法试图确定基因或区域的演化速率与跨分类群感兴趣的表型之间的相关性。这种方法已成功用于量化与整个哺乳动物分支寿命延长相关的遗传约束、不同岩鱼物种的寿命,以及与其他哺乳动物几种不同表型相关的基因和非编码区约束的差异。总体而言,它们强调长寿物种在许多关键的衰老通路(包括DNA修复、细胞周期、细胞死亡、胰岛素信号传导和免疫)中往往表现出限制增加的特征。相比之下,短寿命的鳉鱼种群表现出较小的有效种群大小,并且在相似的通路中积累了有害突变。结合来自单个基因组的见解,作者发现,一般来说,关键的衰老通路在长寿分类群中处于强大的净化选择之下,并且在单个物种的选择基因中观察到独立的特性。这在岩鱼中得到了很好的说明,其中几种长寿物种在DNA修复基因中表现出正向选择的特征;然而,在不同的物种中发现了不同的正向选择基因。在岩鱼中,这些方法还被用于剖析极端寿命的直接遗传驱动因素(主要与营养信号传导有关)和间接遗传驱动因素,间接遗传驱动因素通过增加体型(与DNA修复和mTOR信号传导相关基因相关)来延长寿命。
尽管这些比较方法很强大,但它们仍然存在一些缺点,例如依赖于大型多序列比对(Multiple Sequence Alignments,MSAs)。虽然在这一领域已经取得了进展,但全基因组MSA的生成在计算成本上仍然非常昂贵。此外,MSA无法很好地描述遗传变异,例如结构变异(Structural Variation,SV)会被忽略。另一个重要的警告是,低质量的输入基因组可能会导致不可靠的推论,并排除复杂和快速演化的基因座(框2)。虽然最近的努力优先考虑广泛的分类学采样而不是基因组质量,但未来的项目,如脊椎动物基因组计划,则专注于构建高质量的资源,这些资源对于极端表型的比较基因组学具有重要价值。
来自功能基因组学的见解
从比较基因组学研究中鉴定的基因和通路的功能特性对于充分解析寿命差异的机制基础至关重要。然而,这类工作主要会面临到在非模式、长寿生物中探索分子机制的困难(框3)。尽管如此,有几项研究利用细胞培养模型探索了比较基因组学研究的假设。在大象及其大型亲属(长鼻目动物)的研究中,已经发现了几个肿瘤抑制基因的基因重复;其中两个基因,LIF6和TP53-RETROGENE9,代表了一类在表达时诱导凋亡的功能基因。而在长寿抹香鲸中进行的类似研究发现抹香鲸倾向的修复机制不是清除受损细胞。这项研究证明克隆细胞周期调节因子CDKN2C的转座基因在应对DNA损伤时可以增强细胞周期阻滞和细胞存活能力,以及抹香鲸细胞展示出增强的DNA损伤修复反应。在长寿啮齿动物的研究中,已经揭示了对衰老相关压力的一系列响应,其中许多响应对每个物种来说都是独特的。这些研究突显了利用复杂多样的物种细胞模型来理解诸如体型和衰老等高度复杂的表型的可能性(框3)。
框3. 细胞培养中的衰老研究
尽管衰老相关的假设和治疗的最终检验是在体内进行的,但在长寿物种中进行延长寿命年限或健康年限的纵向研究是昂贵且复杂的,甚至是不可能的。细胞培养模型长期以来一直在科研试验和临床试验之间起着桥梁作用,但关键是必须使用适当的模型,以避免浪费。
许多与衰老相关的过程是组织特异性的,非细胞自主性的。虽然原则上任何细胞类型都可以用于候选基因和通路的初步探索,但对衰老相关基因和干预措施的有力表征需要更符合真实情况的实验体系。类器官模型和器官芯片研究是解决这个问题的有效手段。这些方法要么在实验条件下在体外培养器官组织,要么建立由诱导多能干细胞(induced pluripotent stem cells, iPSCs)衍生的类器官。与体内研究相比,体外类器官体系提供了独有的实验可追踪性和对外在混杂因素的控制。
由于这些需要对目标物种进行侵入性甚至可能致命的取样手段,另一种方法是使用基于干细胞的方法从头构建类器官模型。具体而言,iPSCs提供一个强大的研究手段,能够通过对动物进行伤害最小的非致命性取样来生成任何科研人员感兴趣的组织。iPSCs研究体系的局限性在于,与衰老相关的表观遗传变化在重新编程过程中丢失。在关键的模型物种(如人源模型和鼠源模型)之外生成iPSC仍然具有挑战性。虽然有许多将细胞转化为iPSCs的方法,但其中许多方法依赖于或可能会导致物种基因组或物种基本细胞生物学特征的改变,因此必须特别注意确保所生成的iPSCs能够复刻其原始来源物种的真实生物学特征。
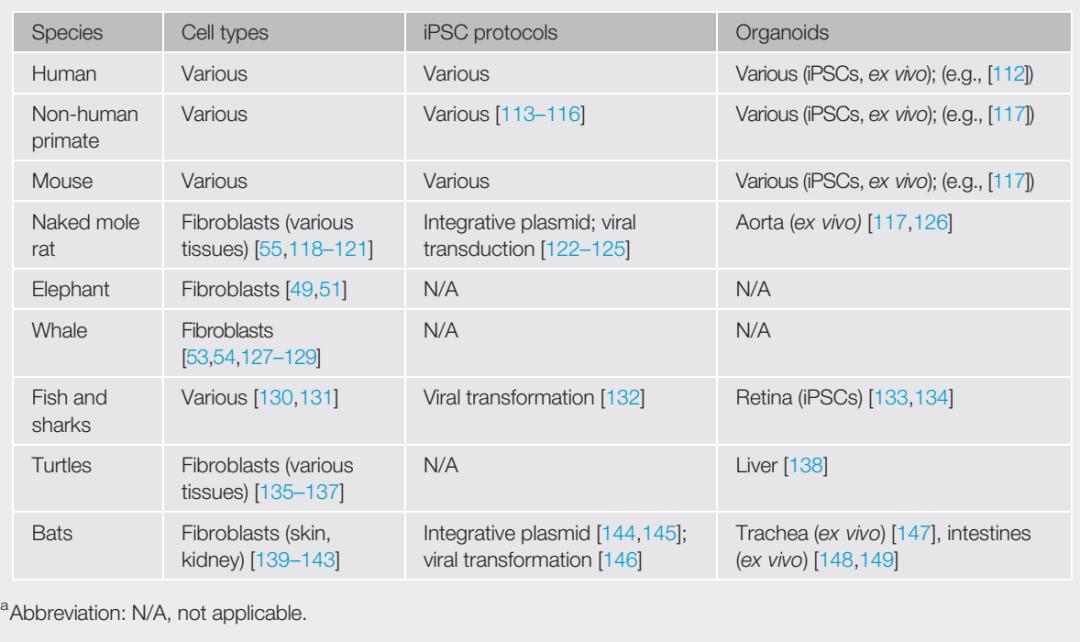
表I展示了一些利用不同长寿物种的细胞模型进行的研究,这些研究旨在推动改善在体外研究衰老这一先进的科研方法
表I. 利用长寿物种的细胞和类器官模型进行的研究
 衰老的群体遗传学
衰老的群体遗传学选择的年龄特异性影响
越来越多的大规模队列研究,如UK Biobank和All of Us Research Program项目为从人群遗传学的角度研究人类衰老提供了新机遇。不同年龄段等位基因的频率变化趋势,有望揭示变异效应的纵向动力学。在人类中,突变积累和拮抗性多效性都被认为可以解释分离的致病等位基因的存在。虽然全基因组关联研究(genome-wide association studies,GWAS)已经发现了这方面的证据,但还存在统计和逻辑缺陷。Mostafavi等人利用超过175,000名参与者的GWAS数据,只发现了少数几个常见的强烈影响年龄特异性死亡的基因变体。这些变体位于APOE ε4和CHRNA3基因座,分别使人易患阿尔茨海默病和易吸烟成瘾。这些结果强调了净化选择对清除有害等位基因的强大影响,即使它们在晚年起作用。
流行病学研究已经证实了生殖特征(如青春期开始年龄或初次生育年龄)与女性寿命之间的关联。Mostafavi等人通过计算这些特征的多基因预测分数,能够显示将青春期延迟和初次生育年龄推迟与增加寿命相关联的遗传变异。相比之下,多基因预测的体质指数(body mass index, BMI)、胆固醇和冠状动脉疾病风险的增加与减少寿命相关。
在人类中观察到净化选择强烈影响迟发致病等位基因的结果很有趣,因为这些等位基因应该在女性绝经和生育高峰期后发挥其作用。确实,对于许多晚发疾病,致病基因的变异体往往是进化上较新的,并以较低的频率分离。为了将这些观察结果与理论相一致,Pavard和Coste开发了一个演化的人口统计学模型,该模型解释了男性生育力延续到老年,以及父母或祖父母家庭照顾的作用该模型预测,在许多情况下,由于绝经后父母和祖父母照顾的影响,导致晚年疾病的变异确实预计会受到强有力的净化选择。
为了预估寿命的可遗传性,研究者们对寿命的演化和遗传之间的复杂关系进行了研究。尽管有研究预估寿命特征有30%的可遗传性,但近期研究分析发现这一预估的可遗传性是由于实验模型的同型交配而被高估的,实际的可遗传性可能小于10%。实际上,寿命的一些最强预测因素是地理和环境因素。综上所述,这些数据强调了社会文化和环境因素在影响人类寿命方面的明显重要性。
基因与环境之间的相互作用(G×E)也起着重要作用,尽管在人类中很难进行细致的解析。最近在果蝇中的一项研究发现了与寿命相关的等位基因在饮食压力(高糖与对照)下的表达情况。令人惊讶的是,三分之一的等位基因介导了一个环境特异的(G×E)效应,缩短了寿命。这些等位基因在演化上较新,并在野外表现出选择的迹象。这些结果支持了“演化错配假说”,即古代环境与现代环境之间的差异对疾病的影响。值得注意的是,人类在过去几千年中经历了从狩猎采集模式到农业生计为主的巨大的饮食结构变化。
虽然许多后期作用的致病基因似乎处于强烈的净化选择之下,但与生命早期表达的基因相比,老年表达的基因通常展现出减弱的选择迹象。对几种哺乳动物和昆虫的基因表达分析发现,在生命晚期表达的基因中,非同义替换(dn/ds)的比率明显更高。晚期表达的基因还表现出更多的分离性非同义替代和较低的选择效力(Nes)。在鳉鱼中也发现了类似的迹象,早期表达的基因重新显现了选择的严格性。为了更广泛地探索人类群体中的这些模式,Yamamoto等人开发了一个统计模型,用于量化可归因于年龄或遗传的948人中27个不同组织的基因表达差异的比例。有趣的是,尽管对于大多数组织来说,净化选择的力量在生命早期表达的基因上确实更强,与其他物种的研究相吻合,但一些增殖能力较强的组织则呈相反趋势。这些“non-Medawarian”组织表现出高癌症发病率和年龄相关体细胞突变。驱动这一迹象的基因在与DNA修复、细胞增殖、分化和癌症相关的途径上富集。这种迹象的一个解释是,这些基因具有高度的多效性,在早期发育和后期的这些特定的“non-Medawarian”组织中起着关键作用。
突变:衰老和死亡的原因和/或结果
衰老的生殖系细胞
突变是遗传变异的根本来源。通过观察研究患有软骨发育不全的高龄父系样本获得了一些初步线索,这些线索表明生殖系的突变率会随着年龄的增长而增加。最新的测序方法能够直接测量许多生物的突变率,从而将衰老和一些其他生活史特征与这一关键的生物学特征联系起来。
目前已经进行了一些年龄对人类突变率影响的深入分析。一项对1548个家系进行的研究表明,父亲的突变率(1.51个突变/年)随着年龄的增长而增加,其速度大约是母亲(0.37个突变/年)的四倍。来自精子和卵子的新生突变也有显著差异,并观察到几个卵子特异性突变热点。有趣的是,对来自患有自闭症谱系障碍(ASD,Autism Spectrum Disorder)和正常的多个单代家庭的近10,000人的分析没有发现任何年龄与SV形成率的相关性,尽管SV在ASD先证者中被观察到的比率明显更高,并且更有可能起源于父亲。这些结果与最近对恒河猴父母/后代的分析是一致的,未能确定SV形成与年龄的任何关联。然而,这些观察结果与随年龄增长精子不稳定性和分裂性显著增加的分析结果不一致。未来的研究还需要新的测序技术,用来解决家系研究和配子直接观察结果之间的差异。特别是,使用短读长测序来从头识别SV极具挑战性。基于长读长的测序方法,包括那些利用新的端粒到端粒组装的方法,可能在检测新生SV事件时提供更高的灵敏度(框2)。
生殖系突变率在物种之间也有很大差异,这反映了不同物种生活史和生殖策略的差异。最近对不同哺乳动物、鱼类、鸟类和爬行动物进行的一项标志性研究发现,脊椎动物的平均种系突变率为1.17×10−8,较高的突变率主要是由繁殖时较大的亲代年龄驱动的。然而,不同物种之间,每代突变率相差高达40倍。哺乳动物和鸟类的突变率具有父系偏向,但在爬行动物和鱼类中没有。成熟年龄和世代时间都与突变率呈正相关,而在哺乳动物中,每代后代的数量与突变率呈负相关。突变谱在脊椎动物类别之间也有很大差异。差异最大的是鱼类A>C和C>A突变。生活史的变化会对生殖系突变率和突变谱有强烈的影响。一个极端的例子是家养动物,它们被选择的世代时间很短,导致每年的突变率异常高。在岩鱼中,长寿的物种表现出更多分离的CpG>TpG突变。这种突变特征是甲基化胞嘧啶自发脱氨的特征,突出了种群平均世代时间的变化可以影响分离遗传的变异谱。尚未对物种间的新生SV的速率和变异谱进行广泛的比较。然而,这些结果共同强调了突变率与衰老之间的密切关系。
体细胞突变
体细胞突变随着年龄的增长而积累。事实上,普遍认为体细胞突变的积累是衰老的“标志”,但是尚不清楚这种突变在多大程度上是导致衰老的原因。体细胞突变很难测量,因为它们的频率很低,而且很难将它们与测序错误区分开来。新开发的单分子测序技术,如Nano-seq (双重测序),可以高度精确地识别体细胞突变以确定体细胞突变率。体细胞突变率往往比匹配的种系突变率高出1-2个数量级;然而,它们在不同的组织和细胞类型之间有所不同。这种增加的体细胞突变率与一次性体细胞理论是一致的,该理论假设生物体在生殖系和体细胞修复的投入方面面临着资源权衡。
虽然绝大多数关于体细胞突变的研究都集中在人类身上,但最近对16种哺乳动物肠道隐窝的分析为体细胞突变的演化提供了一些关键的见解。观测到的突变中以内源性突变为主,而不是环境相关的突变,尽管这种趋势可能在细胞类型和组织之间有所不同。在哺乳动物中,观察到的突变特征在很大程度上是相同的,与在新生代生殖突变中的结果相似,后者只发现了脊椎动物类群之间的突变谱差异。最引人注目的是,体细胞突变率与寿命呈负相关,82%的种间变异可以用这一发现来解释。令人惊讶的是,体型的变化与体细胞突变率无关。此外,无论寿命如何,不同物种的寿命结束时体细胞突变程度的差异只有3倍,这支持了体细胞突变积累可能是影响寿命的关键因素。总之,这些发现表明,至少在某些细胞类型中,体细胞突变程度高度准确地代表了物种的绝对年龄。
癌症是体细胞突变激活不受控制的细胞增殖引起的,不同细胞类型的癌症风险不同。因此,如果每个细胞都具有某种内在的肿瘤发生风险,那么拥有更多细胞的较大生物体就应该具有更大的患癌风险。物种内部确实如此:例如,在人类中,许多不同癌症的风险随着身高的增加而增加。同样,在犬类中,大型犬的癌症发病率更高。然而,物种之间的寿命、体型和癌症风险之间并没有明显的相关性,这一现象被称为Peto悖论。寿命较长的生物体,由于突变负担的增加,也会导致患癌症的风险增加。
最近一项对191种哺乳动物的110,148只圈养个体的研究确定了癌症死亡风险(CMR, Cancer Mortality Risk;死于癌症的可能性)的巨大差异。超过20%的物种显示出与癌症相关的死亡实质性风险(超过10%的CMR)。然而,体重和寿命分别仅占CMR跨物种变异的0.78%和2.94%,这有力地支持了哺乳动物的Peto悖论。这一证据与寿命和体细胞突变率之间的负相关关系结合,支持了缓解癌症的生命历程依赖性演化。然而,在较大的生物体中,很大程度上仍未找到支持增强抗癌能力的遗传驱动因素,但最近的研究发现了多种可能机制(框3)。
总结语和未来展望
衰老和演化领域的范围非常广泛,超过了本文所讨论的主题,包括表观遗传修饰、端粒磨损和其它衰老标志。本文也选择在这里主要关注脊椎动物,尽管许多衰老背后的分子机制在无脊椎动物中,甚至在植物模型中都是保守的,正如在其他综述中所描述的那样。
在整个生命之树中,寿命的差异已经演化了无数次。寿命的长短与几种不同的表型和环境条件密切相关。这意味着极端寿命可以间接地从共同变异特征的选择或对新环境的适应中产生,这些特征将留在它们的基因组中。剖析选定的基因和通路影响仍然具有挑战性;然而,细胞和类器官模型已经成为探索这些延长寿命适应性的潜在工具。
特定于年龄的选择压力现在第一次在人类身上被揭示出来,表明强烈有害的等位基因,即使在作用较晚的时候,也表现出净化选择的特征。总体而言,除了少数高增殖的“non-Medawarian”组织外,早期表达的基因相比于晚期表达的基因其约束力更强。然而,对于表达时间和约束的细胞类型特异性模式仍需进一步探索。这些研究有可能揭示每种细胞类型中的“Medawarian”和“non-Medawarian”模式的异同。未来在整个生命周期中对细胞表型的分析也将使个体细胞现象与生物体水平的表型和演化模式联系起来。
衰老和寿命的演化与突变率的演化密切相关。虽然在剖析单核苷酸突变方面取得了进展,但研究者们对生殖系和体细胞SV的理解仍不完整。随着体细胞突变分析方法成本的下降,未来的研究也有可能增加研究者们对不同类型细胞衰老的理解。这些研究有望为比较基因组学确定的寿命相关通路提供进一步的见解,并阐明它们细胞类型特异性的作用。
几种基因组技术的出现极大地推动了研究者们对衰老演化的理解。然而,这些技术直到最近才开始大规模应用于探索进化生物学的基本问题。因此,当研究者们开始全面探索生物多样性,以揭示地球生命史差异的诸多不同起源时,未来(见主要问题)就拥有了前所未有的希望。
主要问题
基因与环境(G×E, Gene-by-environment)的相互作用在影响寿命和其它生活史性状方面起着极其重要的作用。然而,即使在模式生物中,识别G×E相互作用也是具有挑战性的,而且这些作用在人类中仍未得到充分的探索。一个主要的挑战是研究设计和统计方法的发展,这些方法能够识别大型人类队列中的G×E相互作用,并阐明这些相互作用对人类健康和寿命的影响。
寿命与其他几个生活史特征的协方差表明,共同的遗传通路塑造了衰老作用方式。这些通路中有许多是极其保守和必要的。虽然这些通路通过比较基因组学研究被反复发现,但解开这些通路中扰动的许多多效性和上位性影响仍然极具挑战性。
长度长测序揭示了存在于以前棘手区域的广泛结构差异,如着丝粒、端粒和核糖体(r)DNA重复,以及大型SV,如倒置和易位。然而,目前基于多序列比对的比较基因组学方法并没有用来评估这种变异。一个悬而未决的问题是,这些结构重排如何影响表型。回答这个问题除了需要高质量的基因组和表型数据外,还需要新的计算和统计比较方法。
性染色体上异染色质的重复序列与衰老有关,但它们在不同物种中的被抑制的纵向动力学及其毒性机制尚不清楚。
虽然最近的研究强调了寿命演化与生殖系和体细胞单核苷酸突变模式之间的紧密联系,但我们对衰老相关的体细胞和生殖系SV的理解仍然不完整。

原标题:《【学术前沿】重磅综述|衰老和寿命的演化》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




