- +1
Cell子刊:激活GCN2,可代谢重编程T细胞,增强其抗肿瘤免疫
原创 生物世界
撰文丨王聪
编辑丨王多鱼
排版丨水成文
使用体外扩增T细胞进行的过继细胞治疗(ACT)在癌症治疗展现了巨大潜力。利用从切除的肿瘤组织中获取的自体肿瘤浸润淋巴细胞(TIL)的ACT方案在转移性黑色素瘤患者中取得了令人印象深刻的临床反应。值得注意的是,在之前使用其他免疫疗法(例如免疫检查点抑制剂)仍病情进展的患者中,使用TIL疗法可产生持久反应。除了TIL疗法,还开发了其他ACT方案,其中T细胞可以被设计为靶向特定的肿瘤表达抗原。这些方案包括从患者外周血中获取的T细胞,进而改造为CAR-T细胞或TCR-T细胞。
迄今为止,CAR-T细胞疗法已经在某些血液类恶性肿瘤的治疗中取得了革命性进展,约40%的接受治疗的难治性大B细胞淋巴瘤患者实现了完全缓解。针对实体瘤,靶向Claudin 18.2的CAR-T细胞疗法以及靶向各种癌症睾丸抗原(例如MAGE A4)的TCR-T细胞疗法在早期临床试验中取得了有希望的结果。
尽管取得了这一成功,但挑战仍然存在——大多数接受细胞治疗的患者难以获得持久的临床益处。因此,确定可用于制造这些ACT产品的试剂或操作以增强其临床疗效具有重要意义。
2024年3月8日,多伦多大学的研究人员在 Cell 子刊 Cell Reports Medicine 上发表了题为:Ex vivo activation of the GCN2 pathway metabolically reprograms T cells, leading to enhanced adoptive cell therapy 的研究论文。
该研究证实,体外激活GCN2通路可代谢重编程T细胞,从而增强过继细胞治疗效果。
 操纵T细胞代谢已成为增强过继细胞治疗(ACT)疗效的诱人途径。之前的研究显示,在临床前模型中,通过药物或基因增强T细胞的线粒体氧化磷酸化(OXPHOS)可以改善对肿瘤的控制。有趣的是,最近还有研究发现,体外短暂葡萄糖饥饿也可以导致T细胞的代谢重编程和更好的肿瘤控制。这些数据表明,进化上保守的代谢应激通路可能是提高ACT疗效的诱人目标。
操纵T细胞代谢已成为增强过继细胞治疗(ACT)疗效的诱人途径。之前的研究显示,在临床前模型中,通过药物或基因增强T细胞的线粒体氧化磷酸化(OXPHOS)可以改善对肿瘤的控制。有趣的是,最近还有研究发现,体外短暂葡萄糖饥饿也可以导致T细胞的代谢重编程和更好的肿瘤控制。这些数据表明,进化上保守的代谢应激通路可能是提高ACT疗效的诱人目标。GCN2激酶是氨基酸饥饿的重要传感器,一旦被激活,GCN2将释放出大量蛋白质,包括TNF-α、IL-6和IL-10。这些蛋白质可以促进细胞的生长和分裂,从而提高细胞的免疫应答能力。GCN2磷酸化真核起始因子2a并诱导蛋白质翻译重编程,从而普遍抑制全局蛋白质翻译,同时促进转录激活因子4(ATF4)和其他参与细胞自噬和蛋白质摄取诱导的转录因子的表达,以协调基因和蛋白质表达的程序,称为综合应激反应(ISR)。
GCN2-ATF4诱导的综合应激反应(ISR)在CD8+ T细胞和抗肿瘤免疫中的作用尚不清楚。早期研究表明,吲哚胺2,3-双加氧酶1(IDO1)活性导致色氨酸耗竭而激活GCN2,抑制了CD8+ T细胞的功能和增殖。相反,缺乏GCN2的T细胞在激活过程中存在增殖缺陷。在小鼠胶质瘤模型中,缺乏GCN2的CD8+ T细胞表现出受损的抗肿瘤免疫。然而,在B16黑色素瘤模型中,GCN2的特异性缺失并未影响抗肿瘤免疫。
鉴于上述相互矛盾的研究结果,该研究团队尝试确定GCN2通路的激活对效应性CD8+ T细胞的代谢、效应器功能和抗肿瘤能力的影响。
在这项最新研究中,研究团队发现,使用GCN2激动剂halofuginone(halo)在体外激活效应性CD8+ T细胞的氨基酸饥饿反应,可以增强其氧化代谢和效应器功能。
从机制上来说,该研究确定了自噬与CD98-mTOR信号轴是halo治疗所诱导的表型的关键下游介质。将halo处理的CD8+ T细胞过继转移到荷瘤小鼠模型中,导致了强大的肿瘤控制和治愈反应。在体内,halo处理的T细胞与4-1BB激动性抗体协同作用,在免疫治疗耐药的小鼠模型中抑制了肿瘤生长。重要的是,使用halo处理人类CD8+ T细胞也导致了类似的代谢和功能重编程。
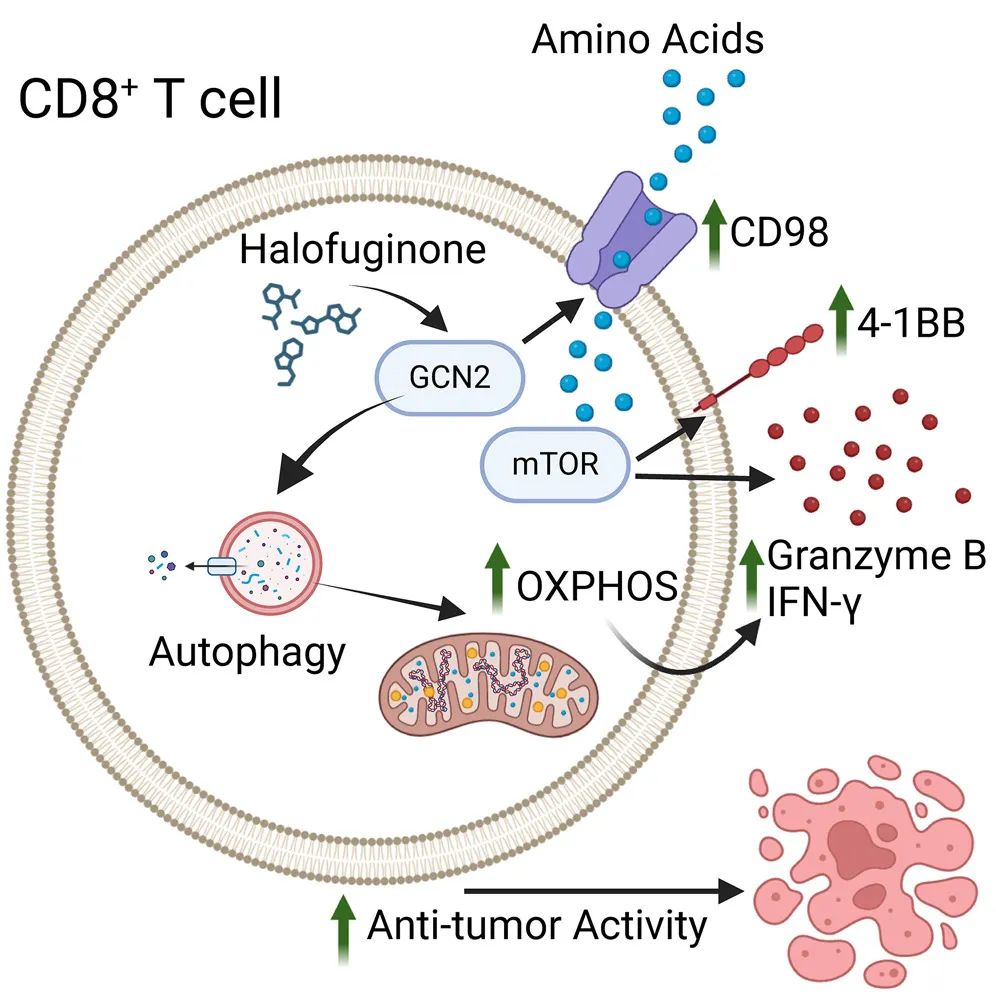 这些发现表明,使用GCN2激动剂halofuginone(halo)激活氨基酸饥饿反应可以增强T细胞代谢及其抗肿瘤活性。
这些发现表明,使用GCN2激动剂halofuginone(halo)激活氨基酸饥饿反应可以增强T细胞代谢及其抗肿瘤活性。论文链接:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00109-5
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




