- +1
武汉两高校合作发表Nature论文,揭开这种病毒防御机制的工作原理
原创 生物世界
撰文丨王聪
编辑丨王多鱼
排版丨水成文
众所周知,噬菌体(Phage)是细菌等原核生物的天敌,而它们也进化出了抵御噬菌体的防御系统,包括限制修饰系统、CRISPR系统,以及Gabija系统。Gabija系统存在于大约15%的细菌和古菌基因组中,Gabija仅由两个基因组成——GajA和GajB。
GajA是克服溶解缺陷(overcoming lysogenization defect,OLD)核酸酶家族的一员,含有N-末端ATP结合盒(ABC)ATP酶域和C-末端Toprim催化域,与其他OLD核酸酶类似,GajA是一种DNA内切酶,利用双金属催化机制通过保守的E和DxD基序进行DNA裂解。然而,与OLD核酸酶家族不同的是,GajA可被ATP抑制,这表明它是一种独特的抗噬菌体防御调节机制。GajB被预测为UvrD/PcrA/Rep样螺旋酶,通常与OLD核酸酶一起发现,GajB不结合DNA或表现出螺旋酶活性,而是感应单链DNA(ssDNA)并水解ATP。
在噬菌体感染时,GajA和GajB都需要通过降解噬菌体和细菌基因组DNA来发挥对噬菌体的强大抵抗力。但其抵抗噬菌体感染的具体分子机制尚未被阐明。
2024年3月12日,武汉大学王隆飞教授团队与华中科技大学朱斌教授团队合作,以加速预览形式在国际顶尖学术期刊 Nature 发表了题为:Structures and activation mechanism of the Gabija anti-phage system 的研究论文。
该研究通过解析Gabija系统的结构,进而在分子层面完整揭示了Gabija系统的抗噬菌体工作机制。该研究加深了我们对自然免疫系统的理解,为探索代谢物作为免疫防御的潜在危险信号提供了新的研究方向。

细菌等原核生物进化出了复杂的固有免疫系统来抵御噬菌体感染。Gabija是一种在原核生物中高度丰富的防御系统,其由两个组件组成——GajA和GajB。
在这项研究中,为了揭示Gabija系统如何被激活以进行抗噬菌体防御,研究团队使用单颗粒冷冻电镜等技术手段,解析了Gabija系统在不同状态下的冷冻电镜结构。首次捕捉到了GajA核酸酶与DNA结合的激活状态和与ATP结合的抑制状态,从而在分子层面完整解析了Gabija系统的工作机制。
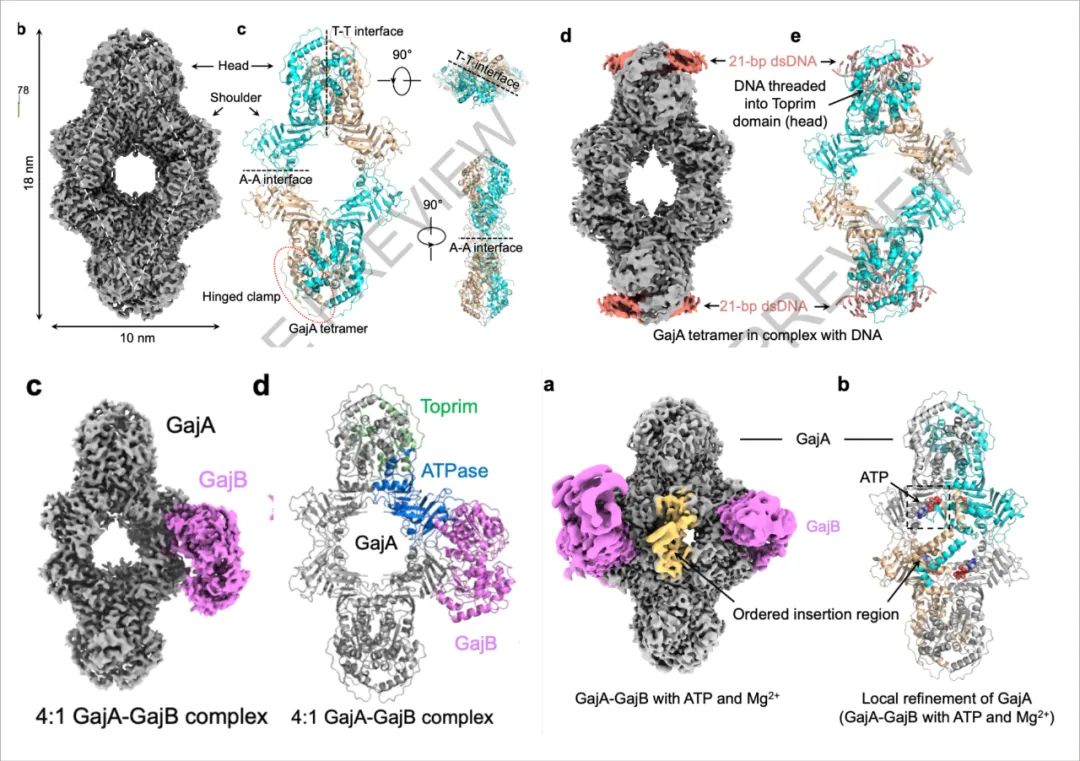
具体来说,Gabija系统在细胞正常生理状态下被ATP抑制,在噬菌体感染细菌后,噬菌体在细菌中的快速复制会消耗大量ATP,从而使GajA不再被ATP抑制。GajA是一个菱形四聚体,其两端的Toprim结构域向两边打开以方便DNA的结合,DNA在切割位点附近发生弯曲,以便于GajA的切割。带切口的DNA又可以激活GajB的ATP水解活性,GajA和GajB这两种酶活性巧妙配合最终导致细菌死亡和噬菌体感染的失败。
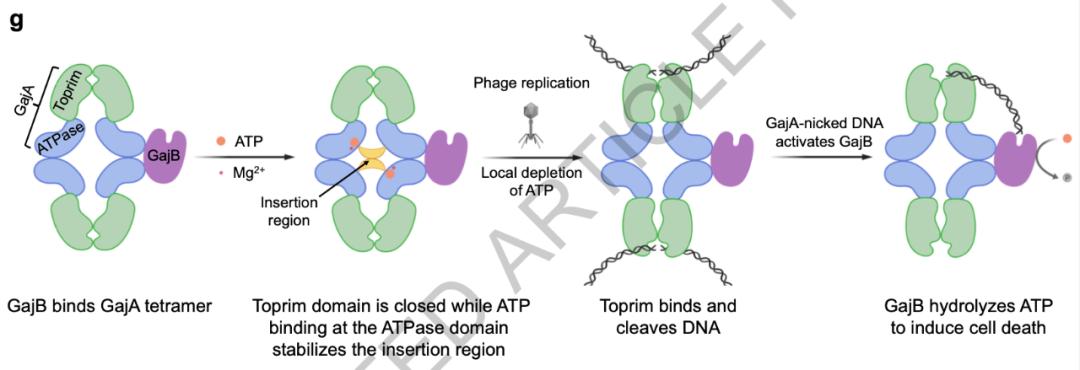
因此,Gabija系统可能是以代谢物的耗竭作为危险信号,是一种独特的原核生物免疫系统。该研究加深了我们对自然免疫系统的理解,为探索代谢物作为免疫防御的潜在危险信号提供了新的研究方向。
武汉大学药学院王隆飞教授和华中科技大学生命学院朱斌教授为该论文的共同通讯作者,武汉大学药学院博士生李静、华中科技大学生命学院博士后成锐、武汉大学药学院副研究员王之明为论文共同第一作者。
论文链接:
https://www.nature.com/articles/s41586-024-07270-x
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




