- +1
【科学普及】渐冻症:当清醒的灵魂困在逐渐“冻住”的肉体中
作者简介:

许多,上海科技大学生命科学与技术学院,本科生
周玉洁,上海科技大学生命科学与技术学院,本科生
栾童舒,上海科技大学生命科学与技术学院,研究生
姚正为,上海科技大学生命科学与技术学院,本科生
王彤,上海科技大学生命科学与技术学院,助理教授 研究员
起初不过是手脚有些笨拙无力,说话有点含混不清,后来喝水吃饭时会出现呛咳,身体逐渐消瘦,直到全身上下的每一处都被一股无形的力量牵制,每个动作都仿佛被按下了慢放键。
身体虽然仍旧和头脑相连,却不受意志支配,好像已不再属于自己。
当最后一根手指的力量也被剥夺,耗尽力气却只能从喉咙里挤出只言片语,连吞咽和呼吸都变成了奢望。飞扬的思绪和自由的灵魂被冰封在一具“麻木不仁”的躯壳中,热烈澎湃的生命在绝望之境渐渐冷却……结尾是被彻底冻结。
这就是肌萎缩性侧索硬化症(Amyotrophic lateral sclerosis, ALS),又称为渐冻症,一种神经退行性疾病。它使著名的优秀棒球手卢伽雷早早断送职业生涯,也将传奇思想巨人霍金囿困于轮椅之上。渐冻症在我国的发病率超过五万分之一,目前有超过20万的患者。随着人口老龄化,预计到2040年,渐冻症的发病率将上升69%。然而,我们至今仍未参透其确切病因。
01
什么人会得渐冻症

统计显示,渐冻症发病患者中,5-10%属于家族遗传,而高达85%以上是没有明显基因突变的散发型病例。
渐冻症的疾病原因十分复杂,涉及到遗传、环境和生活方式等多方面因素的影响。在遗传层面,亚洲患者主要与超氧化物歧化酶1(SOD1)基因的突变相关 (1),而在白种人中更普遍的是C9Orf72基因的重复扩展致病(2)。这些渐冻症的突变基因会遗传到子代,从而导致家族性渐冻症的发生。
渐冻症在男性中的发病率通常比女性高1.2至1.5倍 (3),这可能是由于男性更多暴露于外源性危险因素,如吸烟、从事体力劳动等 (4);对女性而言,渐冻症与运动相关的体力活动之间的关联已被证明在绝经后不那么明显,从而揭示雌性激素可能是预防渐冻症导致的神经退行和肌肉萎缩的一类潜在保护因素(5)。
02
人的身体如何被渐渐“冻”住

人体所有的运动都是在肌肉的控制下实现的,即自由意志通过从脑到脊髓的神经传导最终支配躯体行动。在解剖上,神经信号从上运动神经元,也就是运动皮层这类高级中枢传递到下运动神经元,也就是脊髓这类低级中枢,然后通过神经肌肉接头转换为肌肉收缩。
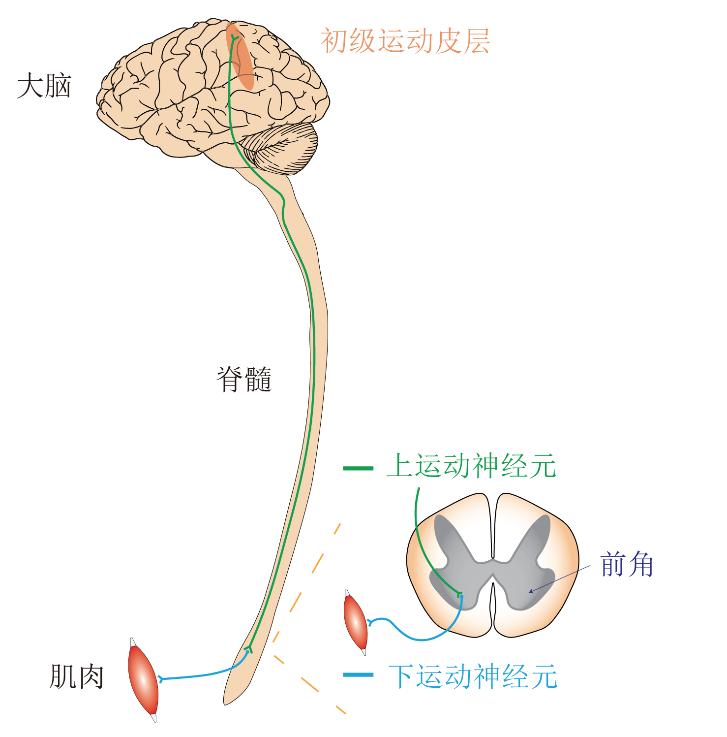
图1:神经系统中运动神经元支配肌肉示意图。(译自(6))
神经元是神经系统的基本结构和功能单元,负责接收、处理和传递信息。神经元由细胞体、轴突、树突和突触四部分组成。研究表明,渐冻症发病后,运动神经元的轴突部分逐渐开始退化,并伴有电生理的改变和行为的异常(7, 8)。随后,这些兴奋性电位改变会引起神经肌肉接头和轴突的变化,导致运动神经元退行性病变 (9, 10),让人们在奔跑途中不自主地摔倒,在拿取东西时不自觉地掉落等。随着时间的推移,这些病理变化加剧并扩散到其他运动单位,导致运动神经元的广泛死亡和肌肉麻痹 (11)。到最后,患者可能只有眼球能动,吃饭靠胃管,呼吸需要机器维持,必须有人24小时进行护理。

图2:渐冻症患者霍金生活图。(引自(12))
03
为何运动神经元会死

人的身体里有约50万亿个细胞,为何偏偏运动神经元这一小群细胞会死?难道它们格外孱弱、脆弱?
其实不然。
为了高效地传递各种物质和信号,神经元轴突的长度往往比较长,而运动神经元恰恰拥有所有神经元当中最长的轴突。坐骨神经是人体最长最粗大的神经,其下运动神经元的轴突可以从腰附近的脊髓一路延伸到脚趾,甚至可以超出1米。
我们可以把轴突比作一条连接神经中枢和下游效应器的高速公路,上面来来往往的货车运输着各种各样的货物。有的专门负责将建造公路所需的货物从胞体运送到轴突末端,有的负责将部分废弃垃圾从轴突末端运送回胞体进行处理。因此,拥有超长轴突的运动神经元,就需要大量能量和资源来维持道路的通畅和往来车辆的正常运行。
轴突的长距离物质运输是以马达蛋白为首的一系列专门负责在轴突上运输货物的蛋白质推动的。它们运送的货物包含了细胞必需的脂质、蛋白质、信使RNA、细胞器等,驱动着它们的燃油则是细胞专用的“能量货币”三磷酸腺苷(ATP)。一旦轴突运输因为各种原因受到阻碍,尤其是来自“ATP的供应商”线粒体的能量供给被切断时,轴突就会难以维持稳定的结构和功能,从而导致神经元退行性病变 (13)。因此,运动神经元对于能量代谢极其敏感,细胞中的“燃油”ATP必须时刻保持充足,否则轴突运输就无法维持,运动神经元也会逐渐死亡。
04
轴突:运动神经元的阿喀琉斯之踵


图3:忒提斯将阿喀琉斯浸入冥河。(引自(14))
在古希腊神话中,阿喀琉斯全身刀枪不入,只有脚踝(踵)是唯一没有浸泡到冥河水的地方,也是唯一致命的弱点。
运动神经元纤长的轴突好比阿喀琉斯之踵,是运动神经元最脆弱的地方。哪怕是一个小小的基因突变都有可能导致轴突损伤,从而将运动神经元拖入死亡的深渊。在渐冻症患者中,反式激活应答DNA结合蛋白-43(TDP-43)基因的突变是一种常见的致病因素。一方面,TDP-43基因突变会导致这些粘稠的蛋白在轴突中形成的大的固体的聚集,如同摧毁窄路的泥石流,让轴突运输中道而止,运动神经元也因各种必需品无法送达指定地点而死亡(如图4所示)(15)。
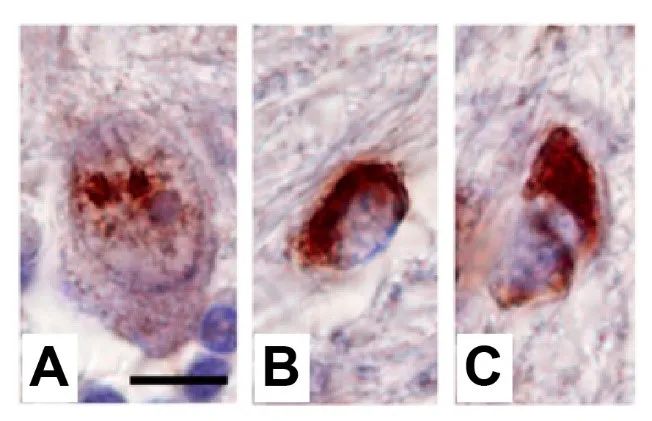
图4:97%的渐冻症患者运动神经元中存在TDP-43蛋白聚集体。渐冻症患者的神经元细胞质中,存在圆形(A)、弧形(B)或子弹状(C)的TDP-43聚集体(褐色)。(修改自(16))
另一方面,突变的TDP-43蛋白聚集体还会像口香糖一样,黏上线粒体内的蛋白,共同形成更大的聚集体。这些线粒体蛋白跟突变的TDP-43在一起后,也无暇顾及它们本来的工作,最终导致细胞能量的主要供应商——线粒体罢工了。失去了能量来源,轴突上来来往往的货车也就失去了动力,轴突运输陷入停滞。此时的运动神经元就像堰塞湖一样,一触即溃。
05
渐冻症不会永远是“不治之症”

尽管尚未取得完全成功的突破,但治疗渐冻症的药物研发正以前所未有的速度推进。目前,许多药物已进入临床试验阶段,包括缓解症状的小分子药物、针对清除蛋白聚集体的抗体药物、以及针对异常蛋白生成的反义寡核苷酸(ASO)等 (17-19)。此外,高效安全的腺相关病毒(AAV)依赖的基因治疗也在进行中。例如,神济昌华公司开发了AAV基因治疗药物SNUG01,并于去年进行了国内首例渐冻症患者的AAV基因治疗,在三个月后的随访中发现患者部分指标有所改善 (20)。随着社会对渐冻症关注度的提高,在科学家、临床医生和患者的共同努力下,渐冻症的病理机制越来越清晰,而其有效治疗方法也即将出现。
拥有阿喀琉斯之踵的运动神经元如此脆弱,重塑运动神经元的活力以逆转渐冻症又何其困难!但是,近年来涌现出的研究成果如同闪耀的星星之火,在这片黑暗的荒漠上发出点点光亮。“路漫漫其修远兮,吾将上下而求索”。
参考文献
1.Rosen DR (1993) Mutations in Cu/Zn superoxide dismutase gene are associated with familial amyotrophic lateral sclerosis. Nature 364(6435):362.
2.DeJesus-Hernandez M, et al. (2011) Expanded GGGGCC hexanucleotide repeat in noncoding region of C9ORF72 causes chromosome 9p-linked FTD and ALS. Neuron 72(2):245-256.
3.Manjaly ZR, et al. (2010) The sex ratio in amyotrophic lateral sclerosis: A population based study. Amyotroph Lateral Scler 11(5):439-442.
4.Chiò A, et al. (2017) Secular Trends of Amyotrophic Lateral Sclerosis: The Piemonte and Valle d'Aosta Register. JAMA Neurol 74(9):1097-1104.
5.Trojsi F, D'Alvano G, Bonavita S, & Tedeschi G (2020) Genetics and Sex in the Pathogenesis of Amyotrophic Lateral Sclerosis (ALS): Is There a Link? Int J Mol Sci 21(10).
6.https://www.physio-pedia.com/Motor_Neurone
7. Raoul C, et al. (2002) Motoneuron death triggered by a specific pathway downstream of Fas. potentiation by ALS-linked SOD1 mutations. Neuron 35(6):1067-1083.
8. Bories C, Amendola J, Lamotte d'Incamps B, & Durand J (2007) Early electrophysiological abnormalities in lumbar motoneurons in a transgenic mouse model of amyotrophic lateral sclerosis. Eur J Neurosci 25(2):451-459.
9.Bruijn LI, et al. (1997) ALS-linked SOD1 mutant G85R mediates damage to astrocytes and promotes rapidly progressive disease with SOD1-containing inclusions. Neuron 18(2):327-338.
10.Fischer LR, et al. (2004) Amyotrophic lateral sclerosis is a distal axonopathy: evidence in mice and man. Exp Neurol 185(2):232-240.
11.Frey D, et al. (2000) Early and selective loss of neuromuscular synapse subtypes with low sprouting competence in motoneuron diseases. J Neurosci 20(7):2534-2542.
12.https://intensivecareathome.com/why-stephen-hawking-lived-a-good-life-until-76-on-a-ventilator-with-tracheostomy/
13.Vandoorne T, De Bock K, & Van Den Bosch L (2018) Energy metabolism in ALS: an underappreciated opportunity? Acta Neuropathologica 135(4):489-509.
14.https://www.mutualart.com/Artwork/Thetis-dipping-the-infant-Achilles-into-/45A12DCDC36AF23E
15.Taylor JP, Brown RH, Jr., & Cleveland DW (2016) Decoding ALS: from genes to mechanism. Nature 539(7628):197-206.
16.Arai T, et al. (2006) TDP-43 is a component of ubiquitin-positive tau-negative inclusions in frontotemporal lobar degeneration and amyotrophic lateral sclerosis. Biochemical and Biophysical Research Communications 351(3):602-611.
17.https://www.clinicaltrials.gov
18.https://trialsearch.who.int
19.https://www.chictr.org.cn
20.https://www.sineugene.com/cn/ndetail/35.html
原标题:《【科学普及】渐冻症:当清醒的灵魂困在逐渐“冻住”的肉体中》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




