- +1
双源光子计数CT:心脏CT和冠脉CTA应用概述
 原创 赵喜同学 长按识别下方二维码关注我
原创 赵喜同学 长按识别下方二维码关注我大家好,欢迎大家访问XI区!
无创心脏成像正在快速发展,最近取得了重大技术突破。临床对于不同成像技术的需求都在不断增长,其主要驱动力是排除明显的冠状动脉管腔狭窄或冠状动脉异常、调查心肌组织特征、评估冠状动脉粥样硬化斑块的形态和特征,以及为介入手术提供充分的术前支持(参见XI区:)。CT是解决这些问题的有力工具,在需要进行血管造影/解剖评估时,它已被视为心血管疾病的主要诊断工具。然而,对于心脏和冠状动脉而言,仍存在一些局限性(也取决于相关技术),主要包括对比分辨率有限、对严重钙化和支架患者进行血管造影的空间分辨率不够理想、金属/钙化/线束硬化伪影以及组织特征描述能力不够理想。此外,CT扫描还存在一些直接风险,如电离辐射暴露增加,以及造影剂引起不良反应或造影剂肾病的可能性。
光子计数计算机断层扫描(PCCT)是一种新引进的CT探测器技术,已开发超过20年,最近才进入临床领域。西门子医疗于2021年9月通过了美国食品药品管理局(FDA)的认证,并发布了全球首台商用PCCT扫描仪(NAEOTOM Alpha)。2023年10月,该设备获得了NMPA的认证,正式在中国上市。来自意大利的学者总结了PCCT在心血管疾病中的应用,我们一块学习一下。
PCCT基于全新一代的X射线探测器。迄今为止,CT探测器的标准技术是能量积分探测器(EID),光子撞击探测器表面,检测到的信号与所有光子沉积的总能量成正比,而没有关于单个光子或其能量的具体信息;这是因为光子转换成光时存在一些固有的局限性,如空间分辨率有限、散射、低能量光子丢失以及没有能级区分。而PCCT探测器是由碲化镉、碲锌镉或硅制成的半导体探测器材料组成,可直接将每个X射线光子转化为电子空穴对。这样就能直接检测到光子,对其进行计数(即光子计数)并将其分离到特定的能量水平,同时消除电子噪声(参见XI区:)。这种探测器特性在心血管成像中具有重大临床益处,可将空间分辨率提高一倍以上,减少伪影,降低X射线剂量和造影剂用量,并可同时采集多种能量,以确定心肌组织和/或冠状动脉粥样硬化斑块的特征。
与PCCT技术有关的基本特点和技术改进
PCCT有两种不同的工作模式:传统模式和能谱模式。第一种模式与单能量CT相对应,在这种模式下,X射线光子不按能量进行区分,而只进行加总。第二种模式时,光谱数据可通过两种不同的机制使用:能量加权和材料分解。
与传统的先进CT扫描仪相比,通过第一种方法,PCCT可改善噪声性能。为了提高图像质量,我们可以为特定的能量区分配自定义权重。这可以使低能量X射线光子的权重正常化,从而改善软组织之间的对比-噪声比,或纠正线束硬化伪影。
材料光谱分析的分解则是通过测量与能量相关的特定材料X射线衰减,提供图像中某些元素(如碘、钙和钆)的分布信息。这种PCCT技术还能生成虚拟单色图像。与双能量计算机断层扫描(DECT)相比,PCCT可在三种或三种以上的能量机制下获取数据,从而可在诊断能量范围内用K-edge(如金和钆)识别和量化两种以上不同的造影剂。这种能量阈值能力也使PCCT能够提高对比噪声比,并使CT能够为每种成分生成单独的定量图谱。
此外,PCCT的探测器元件尺寸小于EID。由于PCCT探测器直接将X射线光子转换为电子电荷,而不需要闪烁层,因此PCCT的空间分辨率不会受限于需要用反射层分隔相近的探测器元件,以尽量减少相邻探测器元件之间的串扰,防止图像质量下降。与传统CT相比,该技术可实现更高的空间分辨率。
光子计数CT技术的临床意义
光子计数CT新技术在心脏领域应用的主要临床意义在于更高的空间分辨率和所收集信息的多参数/多能量性质。
半导体材料的存在和探测器元件的尺寸使得空间分辨率更高。这样就能以更高的对比分辨率更详细地观察较小的解剖结构,包括冠状动脉管腔和支架的通畅性。空间分辨率的提高还有助于更好地评估高风险斑块特征,即低密度斑块、点状钙化、正性重构和餐巾环征。PCCT技术可对光子的累积数量及其能量分布进行计数,从而提高对比噪声比和能量辨别能力。这可以提高碘对比度,减少放射剂量,或减少获得类似增强效果所需的造影剂量。最后,PCCT探测器的多能量功能可用于减少金属伪影、区分冠状动脉粥样硬化斑块的成分以及鉴别不同的外源性造影剂。
冠状动脉管腔
PCCT系统在冠状动脉管腔评估方面具有临床优势,可提高空间分辨率和对比噪声比。
最近的一项前瞻性研究对14名同时接受PCCT和传统CT血管造影术的患者进行了研究,结果显示PCCT在总体质量和诊断可信度方面的得分分别提高了57%和55%,在冠状动脉近端管腔、冠状动脉远端管腔和冠状动脉壁方面的得分分别提高了48%、51%和69%。一项模型研究也支持这些发现,该研究报告称,与传统CT图像相比,PCCT图像对冠状动脉管腔的检测指数提高了2.3倍。在一项体外研究中,PCCT与EID在模拟患者不同体型的不同条件下进行了比较,结果显示,与EID相比,PCCT的噪声幅度更低,噪声频率峰值更高,空间分辨率更好。此外,与传统的CT扫描仪相比,PCCT在量化重度钙化斑块的管腔狭窄方面具有优势。Li等人也报告了类似的结果,他们证明了由于部分容积和开花伪影的减少从而可以更精细地进行狭窄评估。与此同时,PCCT还能使用钆基造影剂进行CCT K-edge成像。一项体外冠状动脉研究显示,血管内钆基造影剂、钙化斑块和支架材料之间的分界清晰,从而改善了管腔描绘。最近使用碘造影剂也得到了类似的结果。
评估血管腔的另一种方法是使用基于多能量CT的新兴图像重建算法。Allmendinger等人研究了一种新型钙质去除图像重建算法(称为PureLumen)的性能,该算法只去除拟人胸腔模型的钙化部分,该模型可以模拟真实的心脏运动。作者展示了开花伪影的减少和图像可解释性的提高。PCCT实现了"随时可用"的多能量辨别,克服了当前心脏CT的一个难题,即高时间分辨率和多能量成像采集的不可行性。
此外,与传统CT扫描仪相比,PCCT空间分辨率的提高使冠状动脉周围脂肪组织的诊断质量提高了36%。
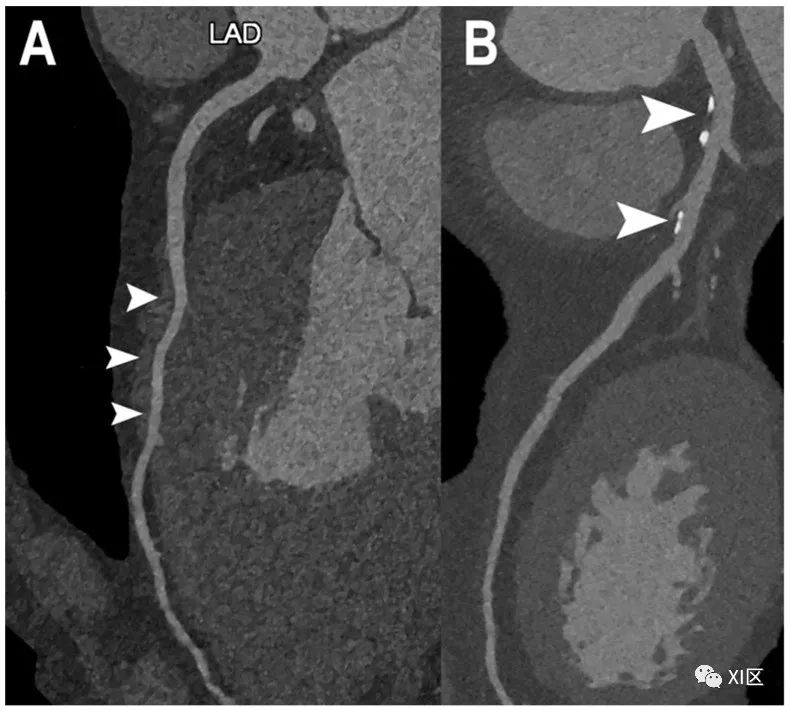
正常和非阻塞性CAD的心脏PCCT示例。图中显示了左前降支(LAD;(A,B))的两个示例。在(A)中,左前降支完全正常,没有任何CAD迹象;唯一的发现是中段((A);箭头)的心内膜走向较深((A))。在(B)中,至少有两个以钙化为主的动脉粥样硬化斑块((B);箭头),但冠状动脉管腔没有任何明显阻塞迹象。使用PCCT进行成像的特别之处在于,这种非常高的细节和空间分辨率是通过标准成像方案获得的,而且不需要高辐射剂量。
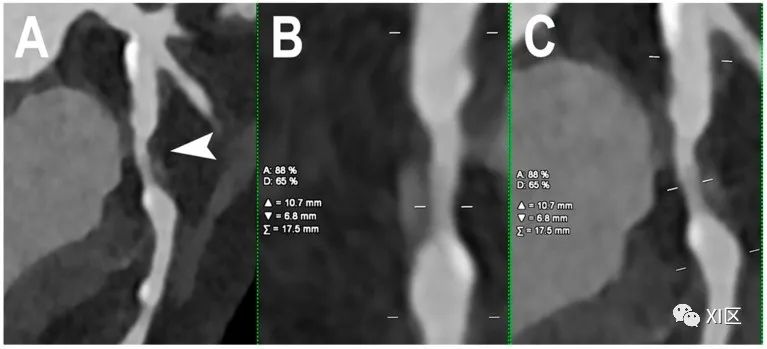
阻塞性CAD的心脏PCCT示例。图中显示的是一个左旋支动脉狭窄的病例,其原因主要是非钙化的动脉粥样硬化斑块,并伴有不明显的正性重构((A);箭头所指)。本例采用0.4mm层厚。对狭窄处的定量评估((B、C);狭窄处的正交纵向视图)显示,管腔直径缩小了65%,管腔面积缩小了 88%。
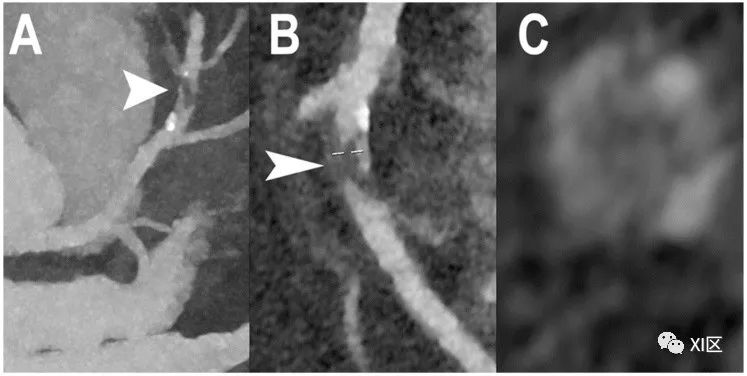
阻塞性CAD的心脏PCCT示例。图中显示的是左前降支(LAD)中段(A-C)严重狭窄的示例。斑块((A,B);箭头)主要呈非钙化表型,内核密度较低(C)。本例采用高分辨率模式重建(空间分辨率为100 μm,层厚为0.2 mm)。
冠状动脉支架
目前最先进的CT扫描仪由于一些技术问题(如金属、开花和线束硬化伪影以及有限的空间分辨率),并不总能对冠状动脉支架患者的血管腔进行最佳评估。
在最近的一项体外研究中,PCCT与传统CT扫描仪在评估18种不同冠状动脉支架方面进行了比较。作者报告称,PCCT的支架内可见度更高,开花和部分容积伪影更少,支架内腔的衰减增加较小。这些结果在不同的体外研究中也得到了证实。
最近,几项人体研究调查了PCCT在冠状动脉支架评估中的优势。Boccalini等人比较了PCCT和传统CT对体内冠状动脉支架的成像质量,结果表明,PCCT的支架和管腔可见度更高,伪影更少,辐射剂量更低(PCCT为25.7 mGy,传统CT为35.7 mGy,P=0.02)。Si-Mohamed等人也报告了类似的结果,他们比较了使用PCCT技术和传统CT扫描仪获得的CCT扫描质量。作者描述了使用PCCT图像对冠状动脉支架诊断质量的改善比例为92%,平均剂量-长度乘积较低。
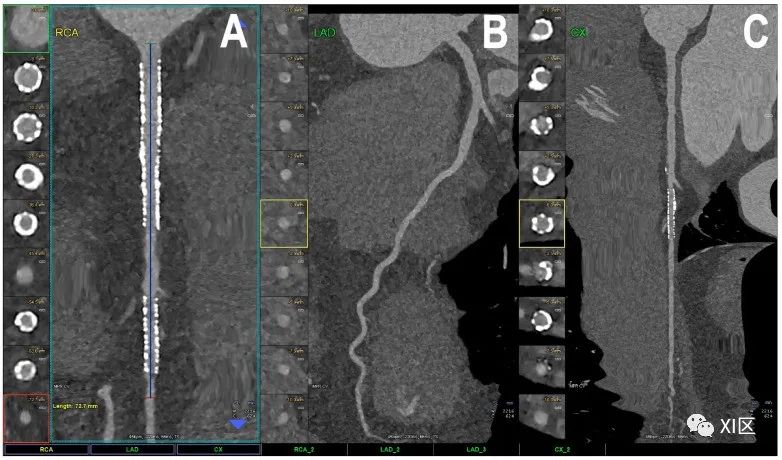
带有多个支架的完整冠状动脉树的心脏PCCT示例。图中显示的是随访时带有多个支架的患者的完整冠状动脉(A-C)。在右冠近端和中段(A)有两个支架,在左缘支(C)有一个支架;左前降支(LAD;(B))正常,没有任何可检测到的动脉粥样硬化疾病。所有支架的内支架和内腔都清晰可见,这在没有传统EID心脏CT上通常不能清晰显示。
这项新技术还可应用于心脏瓣膜和人工瓣膜并发症,尤其是超声检查视图不理想或心脏磁共振磁场不均匀时。
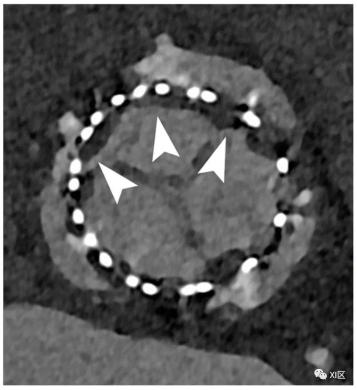
主动脉瓣假体的心脏PCCT。在这个示例中,我们展示了主动脉瓣人工瓣膜的随访情况,该人工瓣膜显示出明显的瓣叶低度增厚(HALT)迹象,这可能是由于血栓附着(箭头),并可能影响瓣叶运动。使用PCCT可以很容易地看到这层非常薄的低密度组织。
冠状动脉钙化评分
冠状动脉钙化(CAC)一般通过CT使用Agatston评分进行量化。用于计算Agatston评分的因子是根据固定的HU阈值选择的,与钙化斑块的最大衰减有很大关系。PCCT可消除电子噪声,从而减少图像噪声、条纹伪影,获得更稳定的Hounsfield单位(HU)数值。在一项体外研究中,比较了PCCT和EID-CT扫描仪的冠状动脉钙化评分,结果显示常规临床方案的CAC评分相当。此外,PCCT在减少层厚的情况下提高了CAC的可探测性和准确性。Symons等人在一个专用的心脏CT模型、十个体外心脏和十个无症状的志愿者身上研究了PCCT在标准和降低辐射剂量下的性能。模型和人体研究表明,PCCT有可能在保持诊断图像质量的同时,提高CAC评分图像质量和/或减少辐射剂量。
在5个尸体心脏的26个钙化冠状动脉病变中,PCCT得出的CAC评分与传统CT得出的CAC评分之间具有极好的相关性和一致性,这支持了PCCT得出的Agatston评分在临床实践中的潜在用途。
Eberhard等人研究了PCCT与传统CT扫描仪相比CAC评分的准确性,并在模型和患者身上探索了不同辐射剂量下的最佳虚拟单色图像和迭代图像重建算法。研究显示,随着迭代图像重建算法水平的增加和keV水平的增加,CAC评分下降。
PCCT对主动脉瓣钙化评分成像也有很大的益处。一项初步报告显示,五名患者使用新型PCCT进行了经导管主动脉瓣置换术规划CT,虚拟平扫图像和真实平扫图像之间的主动脉瓣钙化评分和体积具有极好的相关性。
动脉粥样硬化斑块组成
除狭窄评估外,越来越多的证据强调需要对动脉粥样硬化斑块的形态和特征进行更详细的评估。传统CT扫描仪无法直接观察到冠状动脉斑块的组成部分(如薄帽纤维瘤、微钙化)。PCCT由于提高了空间分辨率,对冠状动脉钙化和非钙化斑块的诊断质量分别提高了100%和45%。在一项体外研究中,与EID相比,PCCT对模拟0.5 mm非钙化斑块(AUC≈95% 对AUC≈75%)和富脂粥样硬化斑块(AUC=85% 对AUC=77.5%)的检测能力更强。
此外,能谱分析还可以通过材料分解算法进行多材料映射。一项初步的体外研究调查了PCCT在23个经组织学证实的冠状动脉粥样斑块中区分冠状动脉粥样硬化斑块成分的能力。研究表明,PCCT可通过测量造影剂浓度和光谱衰减的差异来识别斑块成分。另一项体外研究证实,PCCT在根据不同的光电效应和康普顿效应区分易损动脉粥样硬化斑块成分(钙、铁、脂质代用品和细胞代用品)方面具有巨大潜力,并且与组织学切片具有良好的相关性。此外,Jorgensen等人证明了PCCT能够量化血管密度,作为动脉壁灌注早期动脉粥样硬化变化的标志物。
最近的一项体外研究探讨了PCCT在量化易损斑块特征(如纤维帽厚度、纤维帽面积和富脂坏死核心面积)方面的有效性,并将PCCT特征与组织学测量结果进行了比较。PCCT与组织学测量的纤维帽厚度、纤维帽面积和富脂坏死核心区没有明显差异。
多种造影剂的应用
随着新型造影剂(如纳米粒子)的引入,这项改变游戏规则的技术能够辨别不同的外源性造影剂,并充分利用K-edge成像的能力。K-edge成像技术可将电子内壳与原子之间的结合能识别为特定特征,从而对不同的造影剂进行特定的定量评估。这些新型造影剂有望克服以碘为基础的造影剂的一些局限性,包括循环速度快、保留时间短,以及在高千伏管电压下碘的HU值与钙的HU值相似。最近在不同的模型研究中证实了使用PCCT对三种造影剂进行多重对比成像的可行性,可以为每种造影剂创建单独的物质密度图。
一项体内研究探讨了PCCT在动物模型中同时区分三种造影剂(静脉注射钆和碘、口服铋)的能力,并报告了PCCT在体内区分三种K-edge造影剂的可行性。
最近有学者研究了纳米粒子在PCCT中的应用。Si-Mohamed比较了结合金纳米粒子的PCCT K-edge成像与传统CT图像、组织学检查和透射电子显微镜数据,以检测兔动脉粥样硬化主动脉内的巨噬细胞负荷。研究发现,金浓度与巨噬细胞面积之间存在良好的相关性,这凸显了PCCT在动脉粥样硬化斑块组成和易损性方面的潜在作用。另一项体内和模型研究表明,PCCT与金高密度脂蛋白纳米颗粒造影剂联合使用,具有识别动脉粥样硬化斑块的巨噬细胞负担、钙化和狭窄的潜力。
同样,钨基和镱基造影剂也能改善动脉粥样硬化成像对管腔和斑块的观察。纳米粒子的其他潜在应用包括肿瘤血管的可视化、出血的检测以及治疗后的血管异常。Riederer等人研究了PCCT使用钽基造影剂区分液体栓塞剂和碘造影剂的潜力。作者在一项模型研究中证明,PCCT可以提供钽密度图,区分钽和碘,并能减少血管闭塞治疗后患者因液体栓塞剂产生的伪影。在一项体内研究中,金纳米粒子和脂质体碘被用来量化肿瘤血容量和血管通透性,作为癌症血管生成的指标。在Moghiseh等人的研究中,将 PCCT与金纳米粒子结合使用,可识别和量化特异性单克隆抗体标记的金纳米粒子,并准确检测肿瘤的异质性。
心肌组织成像
PCCT具有能量分辨能力,可确保在单个X射线管电位下获取双能量或多能量。与DECT相比,PCCT可在采集时在每个体素中区分两种以上的造影剂。
这项技术可用于使用双造影剂确定心肌梗塞的心脏损伤程度。首次体内实验是在犬心肌梗塞模型中注射钆基和碘造影剂进行的。作者证明,这些多重造影剂可以结合碘和钆图来区分血池、瘢痕和远端心肌。
材料浓度的量化可能对心肌灌注分析有用,因为这可以准确量化心肌中的造影剂。值得注意的是,碘图是评估心肌灌注的一种著名CT技术,在DECT上对心肌延迟碘增强的量化也已得到验证。PCCT的能量阈值功能使DECT的频谱重叠最小化,从而提高了对比-噪声比和估算造影剂浓度的定量能力。下图显示了使用PCCT进行心肌延迟增强的示例。已证明PCCT能在不同的模型尺寸下提供精确的碘定量(均方根误差为0.5mgI/cc)。
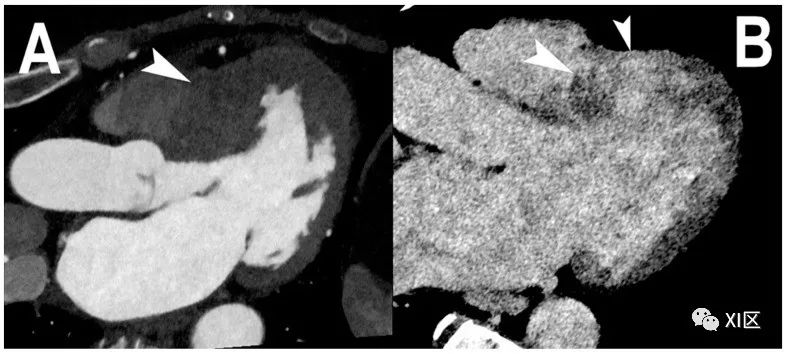
心肌延迟强化的心脏PCCT。本例(A,B)显示的是一名严重肥厚型心肌病患者的三腔投影,患者的左心室基底隔中段受到严重影响((A);箭头)。静脉注射碘基造影剂七分钟后,肥厚左心室壁的碘化CM跨壁聚集(也称为延迟增强)清晰可见((B);箭头)。这一现象与在心脏磁共振中观察到的现象相同,并在临床实践中得到证实。使用PCCT进行这种成像的特别之处在于,能谱成像与标准的心脏CT方案相关,不需要特定的方案。
最近的一份病例报告证明了能谱CT在临床实践中的实用性。Polacin等人描述了一个病例报告,一名61岁的男性因急性胸痛接受了PCCT扫描,怀疑是急性冠状动脉综合征。来自PCCT的双能衍生碘图显示了一个小的缺血性跨壁瘢痕,并经后期钆心脏磁共振证实。
最近的一项模型研究表明,碘/钆联合注射成像也可用于血管内渗漏评估。通过PCCT得出的物质图可以可靠地区分造影剂和动脉瘤钙化。
一项体内研究利用第一代全身双源PCCT探索了30名患者左心室心肌的放射组学特征,报告了冠状动脉钙化与纹理分析之间的关联。与EID-CT相比,PCCT具有更高的空间分辨率和对比噪声比,而且伪影较少,因此作者强调了PCCT在克服放射组学分析众所周知的局限性方面的潜在作用。Tharmaseelan等人利用PCCT研究了主动脉周围脂肪组织的纹理变化与主动脉钙化的关系,并利用放射组学分析证明了主动脉周围脂肪组织与局部主动脉钙化的存在有关。
最近,CT被证明是细胞外容积分数(ECV)定量的替代方法,可与代表当前无创参考标准的心脏磁共振进行比较。Mergen等人的体内研究强调了使用PCCT对心肌组织进行定性的能力。作者使用PCCT虚拟单色图和双能碘图对30名重度主动脉瓣狭窄患者的细胞外容积定量的可行性和准确性进行了研究。虚拟单色图和双能量衍生ECV定量显示出较高的相关性,协议范围较窄,平均误差为0.9%。
减少剂量和造影剂
PCCT可以增强碘化造影剂的衰减。众所周知,碘的线性衰减系数会随着X射线能量的降低而增加。这一物理特性可减少静脉注射造影剂的用量,获得与全剂量传统CT检查相同的诊断结果。在一项模型研究中,CCT就证明了这一点,在PCCT上使用40 KeV的虚拟单色图像重建,可将造影剂浓度降低 50%。多项研究表明,与传统CT扫描仪相比,使用PCCT可提高对比噪声比,从而降低碘造影剂浓度。Kappler等人在一个水模型中研究了这些特征,结果表明,与传统CT扫描仪相比,碘的衰减增加了,但图像噪声相似。
一项拟人化模型和体外研究调查了商用能量积分探测器和光子计数探测器在四种管电压设置下模拟四种病人体型的碘对比噪声比。作者发现,在80、100、120和140 kV电压下,与市售CT扫描仪相比,对比噪声比平均分别提高了11%、23%、31%和38%。此外,与能量积分探测器CT相比,尸体的PCCT显示高能量仓图像中的伪影(如线束硬化和开花)减少了,低能量仓图像的对比度提高了。
Sawall等人利用能量积分探测器、单仓PCCT和双仓PCCT,在不同尺寸(小型、中型和大型)的模型中探索了PCCT在增加碘对比度、减少给药辐射剂量或减少造影剂用量方面的潜力。使用所有管电压和模型尺寸,平均对比噪声比都有所提高,单箱能量可提高30%,双箱能量可提高37%,辐射剂量可减少46%。这些研究结果表明,PCCT可以减少造影剂的用量。在这方面,对碘有不良反应或肾功能不全的患者可能会从中受益。
在低辐射剂量下,PCCT对各种心血管应用中电子噪声对图像质量的改善进行了评估。一项体外、体内和体外研究描述了低辐射剂量下CAC评分的卓越质量。由于没有电子噪声,再加上软组织对比度提高,CAC评分的辐射剂量得以降低。使用PCCT的虚拟单色图像进行的拟人胸腔模型研究也表明,CAC评分的剂量明显减少(最多减少67%)。
挑战
与所有新兴技术一样,在临床实践中充分发挥PCCT的潜力之前,必须解决一些技术难题,包括与光子通量无关的效应(如电荷共享、电荷捕获和K逃逸)和与光子通量有关的效应(如脉冲堆积)。当X射线光子到达像素之间的边界附近时会发生电荷共享,云被计入多个相邻像素电极。特征光子的发射也会导致电荷共享。目前已开发出不同的方案来纠正这一现象。探测器中荧光产生的次级光子可在相邻像素中检测到,从而导致多个事件共享入射光子的总能量。这种效应是实际应用中探测器像素尺寸下限的原因。脉冲堆积的原因是,在非常高的X射线通量下,产生的电压脉冲会在时间上重叠,并被错误地计入单个光子,从而影响能量分辨率和图像质量。可以通过减小像素尺寸来降低脉冲堆积的概率。不过,在实际的CT通量率下,这种影响并不起主要作用。
随着空间分辨率和多能量采集的提高,相关的实际挑战也随之而来:更高的图像数据文件,以及人为操作员在数据存储、解释和后期处理方面的负担加重。关于多能量采集和K-edge成像,在考虑临床应用之前仍有一些问题需要克服。这些问题包括体内成像所需的钆剂量,与目前心脏磁共振所需和推荐的剂量相比较高,以及其他造影剂(如纳米粒子)实际上仍处于实验阶段。
然而,该技术的主要局限性仍然是成本高昂和缺乏普及性。事实上,生产高质量 PCD所需的高昂成本可能会在短期内对PCCT技术的大规模推广产生负面影响。
结论
PCCT有望在未来几年内极大地改变CT在心血管成像中的临床应用。
有必要开展进一步研究,评估PCCT对心血管成像临床实践的临床益处。具体来说,利用前瞻性试验的数据,可以首次尝试评估这种新CT技术与传统CT在心脏领域应用中的性能比较。特别是,PCCT将产生重要的临床差异,从而影响冠状动脉和支架成像中的患者管理。
更多干货,关注XI区!
编译整理自:Cademartiri F, Meloni A, Pistoia L, Degiorgi G, Clemente A, Gori C, Positano V, Celi S, Berti S, Emdin M, Panetta D, Menichetti L, Punzo B, Cavaliere C, Bossone E, Saba L, Cau R, Grutta L, Maffei E. Dual-Source Photon-Counting Computed Tomography-Part I: Clinical Overview of Cardiac CT and Coronary CT Angiography Applications. J Clin Med. 2023 May 23;12(11):3627. doi: 10.3390/jcm12113627. 仅供专业人士交流目的,不用于商业用途。
2024年4月1日
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




