- +1
CCS Chemistry | 膦催化苯并咪唑与环丙烯酮的不对称 [3+2]环加成去芳构化反应
以下文章来源于CCSChemistry ,作者CCS Chemistry
CCSChemistry.
CCS Chemistry是由中国化学会创办的高水平旗舰新刊,面向全球科学家,收录化学各领域高质量原创科技论文。关注CCS Chemistry,即时获取期刊相关资讯。
近日,中国科学院上海有机化学研究所游书力课题组发展了膦催化苯并咪唑与环丙烯酮的不对称 [3+2]环加成去芳构化反应。该方法具有底物范围广、反应条件温和、操作步骤简单等特点,为合成多种手性含氮杂环化合物提供了一种简洁、高效的策略。克级规模反应和产物转化实验,证明了该方法具有一定潜在的应用价值。
背景介绍:
芳香化合物作为一种简单、易得的起始原料,已被广泛应用于有机合成、药物化学等领域。杂芳烃化合物,特别是含有一个或多个氮原子的杂芳烃化合物,在芳香化合物中占据着特殊的地位,它们的衍生物也常常存在于许多天然产物和药物活性分子中。近年来,关于这类化合物的官能团化已经成为一个研究热点,受到了科学家们广泛的关注。催化不对称去芳构化 (CADA) 反应作为芳香化合物的一类重要转化反应,为简单的二维平面芳香化合物提供了一种直接转化为三维立体分子的有效途径。富电子杂芳香化合物参与的去芳构化反应已经取得了较多研究成果,然而缺电子杂芳香化合物特别是苯并咪唑、苯并噁唑和苯并噻唑的CADA反应报道较少,除了少数几例金属催化的CADA反应(图1),手性有机小分子催化的反应鲜有报道。因此,亟需进一步开发不同的催化体系来实现缺电子杂芳香化合物参与的去芳构化反应。另一方面,环丙烯酮作为一类重要的不饱和三元环化合物,其可以通过C−C断裂然后与C=C、C=N、C=O等不饱和双键进行环加成反应,为构建结构多样的有机分子提供了高效的合成方法。
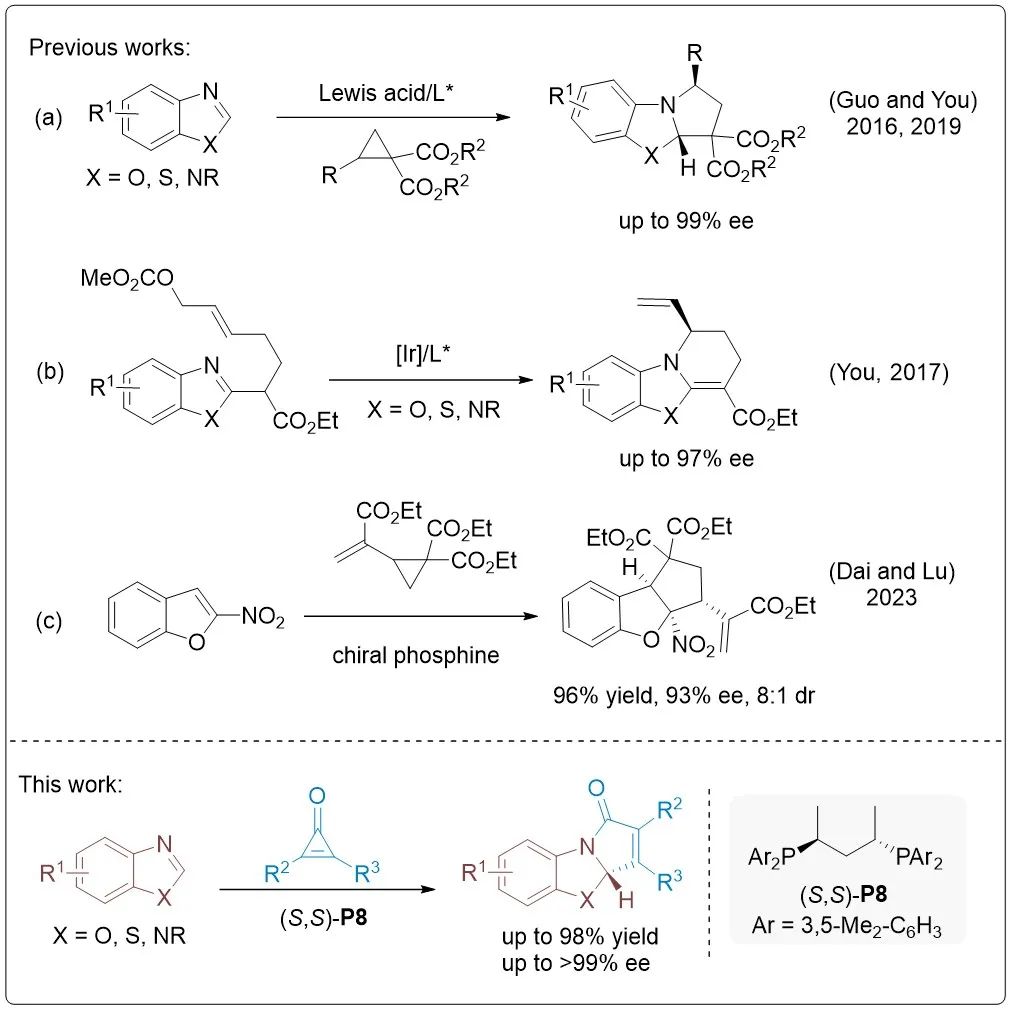 图1. 研究背景与本文工作
图1. 研究背景与本文工作本文亮点:
基于以上研究,作者利用商业可得的手性膦催化剂,实现了苯并咪唑与环丙烯酮的分子间不对称去芳构化反应,以高达98%的收率和大于99% ee的对映选择性合成了一系列去芳构化的吡咯唑氮杂环化合物。
在最优条件下,该不对称去芳构化反应表现出很好的底物普适性和官能团兼容性。对于环丙烯酮底物而言 (图2),当环丙烯酮的苯环上无论是带有给电子基还是吸电子基取代基,反应均能以优秀的收率和优异的对映选择性得到目标产物 (3ba-3bi, 82-98% yields, 90->99% ee)。值得注意的是,当环丙烯酮苯环的邻位带有取代基时,在标准条件下,反应并不能顺利地得到目标产物 (3bj-3bk),猜测原因可能是位阻因素造成的。当把环丙烯酮的苯环换成大位阻的萘环时,反应也能顺利地发生,但收率和对映选择性略有降低 (3bl, 30% yield, 89% ee)。对于杂芳烃取代的环丙烯酮底物2m而言,反应也能顺利地以98%的收率和73%的对映选择性得到目标产物3bm。接下来,还考察了非对称环丙烯酮底物对反应的影响,对底物2n来说,室温反应24小时只能以28%的收率和75% ee得到目标产物3bn,通过二维谱确定了该产物的结构。值得注意的是,烷基取代的环丙烯酮并不兼容该反应体系,可能原因是烷基取代的环丙烯酮反应活性较低导致的。
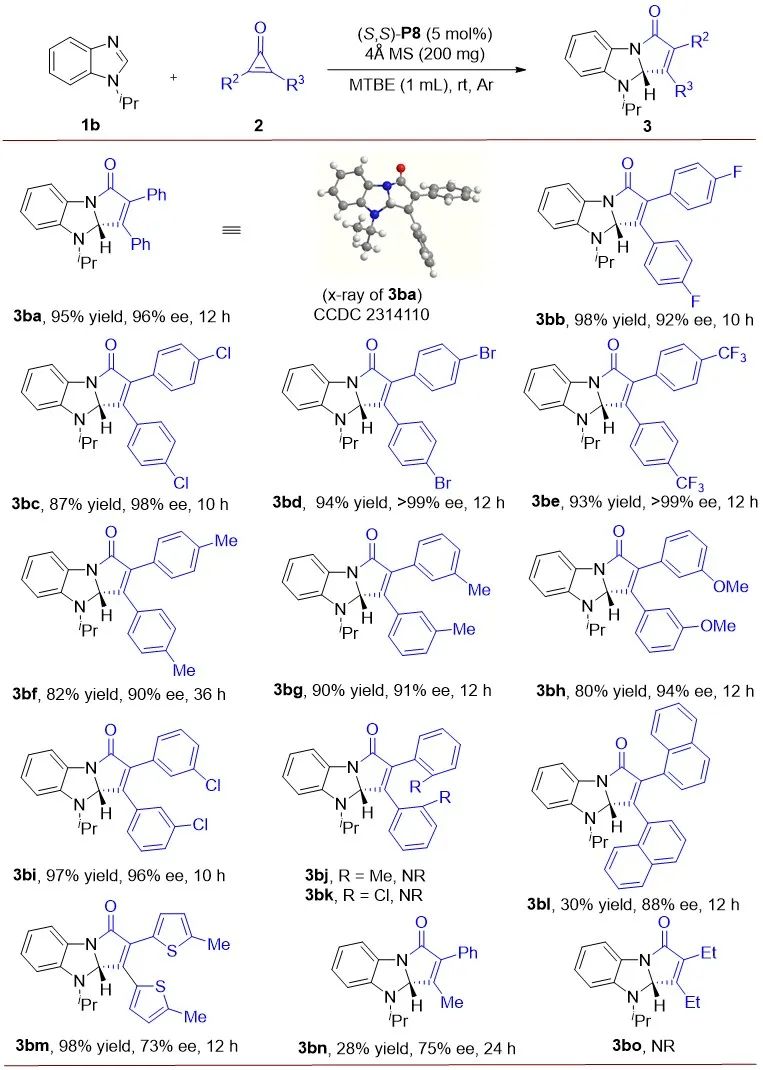 图2. 环丙烯酮底物拓展
图2. 环丙烯酮底物拓展随后,对不同取代的苯并咪唑底物进行考察,其结果如图所示 (图 3)。苯并咪唑N上不同类型的取代基对产物的收率和对映选择性都有重要的影响。除-iPr外,当苯并咪唑的N上带有苄基、甲基、乙基、叔丁基、萘甲基、环己基和炔丙基时,这些底物均表现出良好的兼容性,并以中等到优秀的收率以及良好到优异的对映选择性得到目标产物 (3aa-3ia, 37-98% yield, 79-96% ee)。对于炔基取代底物1j,反应只能以52%的产率和33% ee得到相应的产物3ja。而N-H没有被取代的苯并咪唑底物1k,反应虽然可以顺利地发生,但产物3ka只取得53%的收率和78% ee。对于N-Ts和N-Ac吸电子取代的苯并咪唑底物 (1l, 1m),在标准条件下分别以94%和44%的收率得到产物,但是其对映体选择性却很差 (3la-3ma, 15% ee和19% ee)。此外,作者还考察了苯并咪唑苯环上不同取代基对反应的影响。苯并咪唑苯环的5-位和6-位带有-Me或卤素 (-Cl, Br) 取代基时,在标准条件下,反应均可取得优秀的收率和优异的对映选择性得到去芳构化产物 (3na-3pa, 72-91% yields, 96-97% ee)。7-氮杂-苯并咪唑1q也能很好的兼容该体系,并以92%的收率和96% ee的对映选择性得到产物1qa。最后,也考察了苯并噻唑和苯并噁唑这两种类型的底物对反应的影响,反应虽然可以顺利地发生,并以良好的收率得到目标产物,但其对映选择性还不理想 (3ra, 73% yield, 51% ee; 3sa, 64% yield, 10% ee),猜测原因可能是位阻因素导致的。
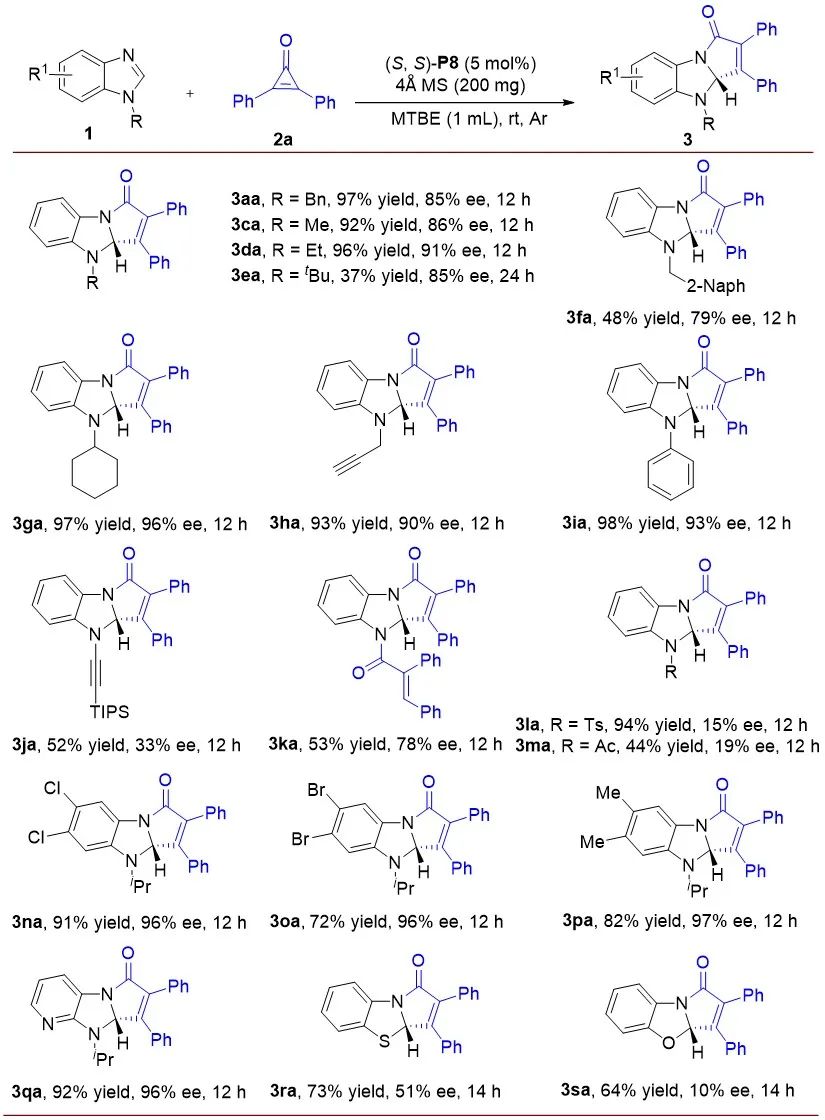 图3. 苯并咪唑底物拓展
图3. 苯并咪唑底物拓展完成底物拓展后,为了验证该方法的实用性,作者对该反应进行了克级规模放大和产物转化实验 (图4)。在标准条件下,将模板底物1b和2a的反应规模放大至3 毫摩尔,可以取得与小反应相当的结果,即以91%的收率和96% ee得到1.0 克目标产物3ba。接下来对手性产物3ba进行产物转化,产物3ba (96% ee) 在DCM中与劳森试剂作用,室温反应2小时能以95%的收率顺利转化为产物4且对映选择性得以保持。此外,炔丙基取代的产物3ha (90% ee)与BnN3通过铜催化的Click反应,以78%收率和86% ee合成三氮唑产物5。
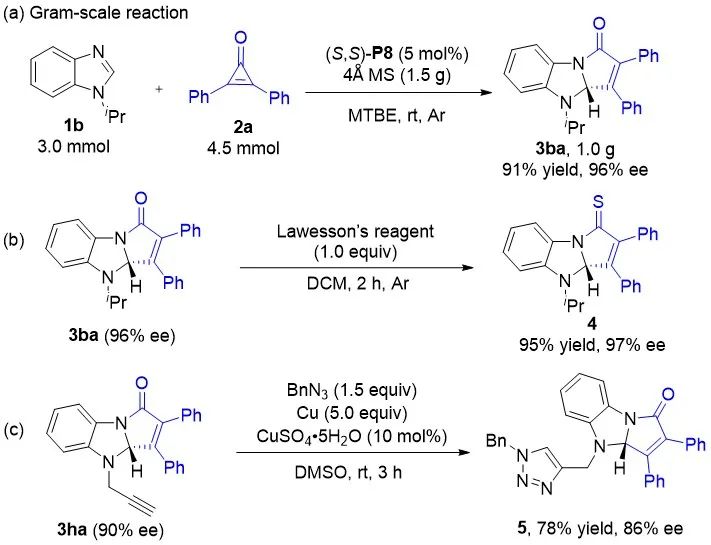 图4. 克级规模与产物转化
图4. 克级规模与产物转化根据上述实验结果和以往的工作,作者对该反应也提出了一个可能的催化循环和立体控制模型 (图式5)。首先,环丙烯酮2a被手性膦催化剂PR3活化,形成两性离子中间体I;紧接着中间体I的C−C键断裂,生成联烯酮中间体II;中间体II受到苯并咪唑底物1b的亲核进攻,生成中间体III;随后,中间体III在苯并咪唑的Re-face的C2位置发生分子内亲核加成形成中间体IV,最后消去一分子催化剂PR3,生成产物3ba,完成催化循环。
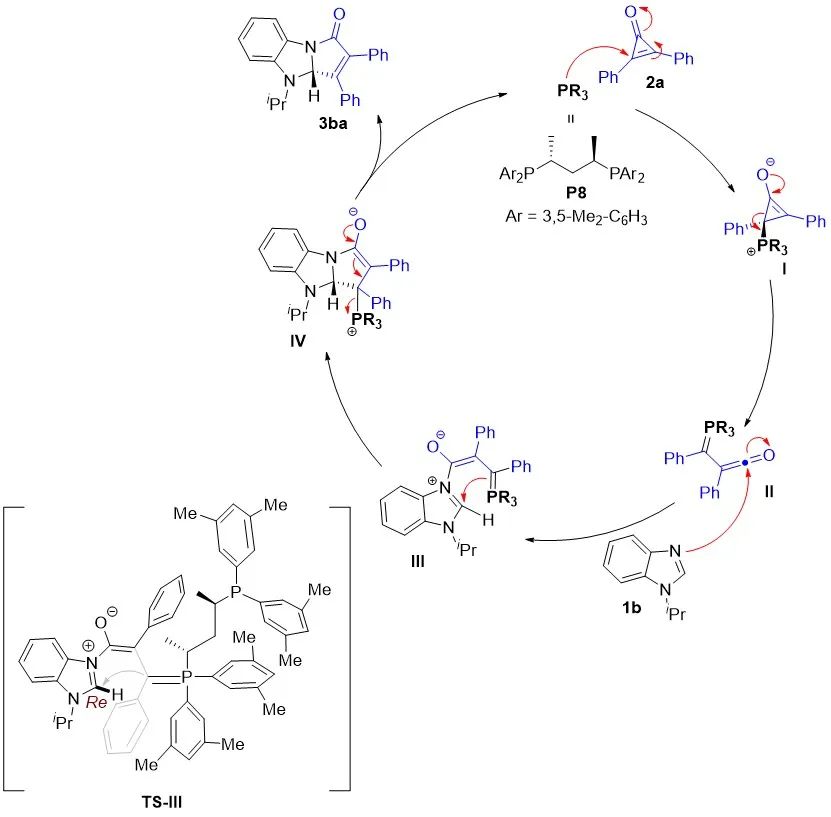 图5. 可能的催化循环和立体控制模型
图5. 可能的催化循环和立体控制模型总结与展望:
综上所述,作者基于手性小分子催化体系,利用商业可得的手性膦催化剂作为路易斯碱,在温和条件下实现了苯并咪唑化合物与环丙烯酮的不对称[3+2]环加成去芳构化反应。反应以优秀的收率 (up to 98% yield) 和优异的对映选择性 (> 99% ee) 合成了一系列含氮杂环化合物。作者也给出了可能的催化循环和立体控制模型,克级规模反应和产物转化实验验证了该方法的实用性。
该工作以Research Article的形式发表在CCS Chemistry。中国科学院上海有机化学研究所游书力研究员为通讯作者,华东师范大学与上海有机所联合培养博士生张闪闪为第一作者。特别感谢国家重点研发计划、国家自然科学基金、上海市科学技术委员会、新基石科学基金会的大力支持。
文章详情:
Phosphine-Catalyzed Asymmetric Dearomative [3+2] Annulation Reaction of Benzimidazoles with Cyclopropenones
Shan-Shan Zhang, Rui-Xiang Wang, Qing Gu and Shu-Li You*
Cite this by DOI:10.31635/ccschem.024.202403981文章链接:https://doi.org/10.31635/ccschem.024.202403981
扫码在线阅读
扫描或长按左侧二维码,
在线阅读全文
 中国化学会
中国化学会Chemsoc
原标题:《CCS Chemistry | 膦催化苯并咪唑与环丙烯酮的不对称 [3+2]环加成去芳构化反应》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




