- +1
Nat Commun丨饥饿状态下大脑如何调节进食行为
2024年6月27日,德国马克斯·普朗克代谢研究所Henning Fenselau团队在Nature communications发表了“NPY-mediated synaptic plasticity in the extended amygdala prioritizes feeding during starvation”,揭示了促食欲神经肽Y(Neuropeptide Y, NPY)介导的杏仁核突触可塑性在饥饿期间优先保障进食,强调了NPY在调节饥饿状态下进食行为中的作用机制。
 高效控制摄食行为需要对复杂的动机和情感神经回路进行协调调整。来自能量感应下丘脑神经元的神经肽是强有力的摄食调节因子,但这些内源性信号如何塑造相关神经回路的具体机制尚不清晰。本文中探讨了NPY如何调整至终纹床核(BNST)的GABA能输入。作者发现,禁食增加了表达AgRP(Agouti-related protein,AgRP,也称为刺鼠关联肽,是由AgRP / NPY神经元在大脑中产生的神经肽。它仅在位于下丘脑弓状核腹侧部分的含有神经肽Y的细胞体中合成)的“饥饿”神经元与BNST神经元之间的突触连接性,该回路与促进摄食相关。相比之下,来自中央杏仁核(CeA)的GABA能输入(一个减少摄食的杏仁核回路)则减少。激活表达NPY的AgRP神经元能诱发这些突触适应性变化,而这些变化在缺乏NPY的小鼠中则不存在。此外,禁食减弱了CeA到BNST投射抑制食物摄入的能力,而NPY缺乏的小鼠也无法降低焦虑以促进摄食。因此,AgRP神经元驱动了输入特异性的突触可塑性,通过NPY在饥饿期间实现了对饥饿和焦虑信号选择性转变的能力,从而高效调节摄食行为。
高效控制摄食行为需要对复杂的动机和情感神经回路进行协调调整。来自能量感应下丘脑神经元的神经肽是强有力的摄食调节因子,但这些内源性信号如何塑造相关神经回路的具体机制尚不清晰。本文中探讨了NPY如何调整至终纹床核(BNST)的GABA能输入。作者发现,禁食增加了表达AgRP(Agouti-related protein,AgRP,也称为刺鼠关联肽,是由AgRP / NPY神经元在大脑中产生的神经肽。它仅在位于下丘脑弓状核腹侧部分的含有神经肽Y的细胞体中合成)的“饥饿”神经元与BNST神经元之间的突触连接性,该回路与促进摄食相关。相比之下,来自中央杏仁核(CeA)的GABA能输入(一个减少摄食的杏仁核回路)则减少。激活表达NPY的AgRP神经元能诱发这些突触适应性变化,而这些变化在缺乏NPY的小鼠中则不存在。此外,禁食减弱了CeA到BNST投射抑制食物摄入的能力,而NPY缺乏的小鼠也无法降低焦虑以促进摄食。因此,AgRP神经元驱动了输入特异性的突触可塑性,通过NPY在饥饿期间实现了对饥饿和焦虑信号选择性转变的能力,从而高效调节摄食行为。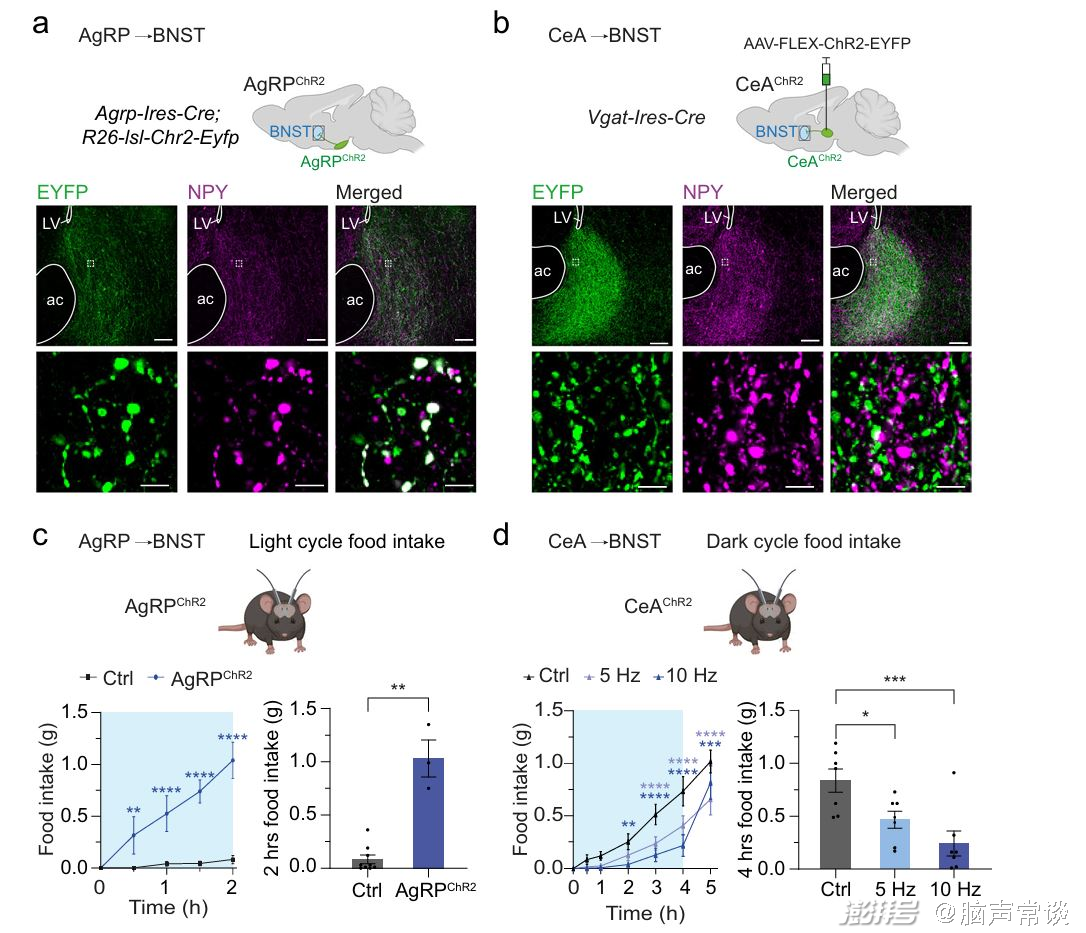
1. 不同GABA能输入至BNST对摄食行为具有不同的调控作用
作者运用光遗传学比较和对比由AgRP神经元和CeA神经元向BNST投射的GABA能输入在调节摄食行为上的特定输入特性。为了评估源自CeA的GABA能输入,在Vgat-Ires-Cre小鼠的CeA中双侧注射了表达Cre依赖性腺相关病毒,同时在BNST上方双侧植入光纤。免疫组化结果表明AgRPChR2和CeAChR2神经元都向BNST的背侧和腹侧亚区发送投射,但不投射到附近的伏隔核。重要的是,这两个传入神经元群体的投射领域广泛重叠,表明AgRP和CeA神经元可能与BNST中的相同或相似的下游神经元相联系。对AgRPChR2神经元在BNST的光刺激在光照周期开始时迅速且明显地增加了饱食小鼠的食物摄入量。2小时的光刺激(20Hz;1秒开,3秒关)使AgRPChR2小鼠的食物摄入量约为1克,但在对照组小鼠中没有此效果。相反,对CeAChR2在BNST的终端进行光刺激,在黑暗周期开始时(此时小鼠自然感到饥饿)显著降低了食物摄入。用5Hz或更高频率的连续光刺激(该刺激方案已被发现能引发焦虑和摄食行为)显著减少了食物摄入,而2.5Hz的刺激则无影响,表明CeA→BNST回路对食物摄入抑制的刺激强度依赖性调节。当光刺激在4小时后关闭时,小鼠迅速增加了食物摄入,这表明该GABA能回路的持续稳定激活对于减少摄食至关重要。在光照周期中,对饱食小鼠的BNST中的CeAChR2终端进行光刺激也轻微减少了食物摄入。总之,通过光遗传学方法揭示了AgRP神经元和CeA神经元到BNST的不同GABA能输入在调节摄食行为上的特异性和复杂性,强调了这些输入在不同生理状态下对食物摄入控制的精细调节作用。
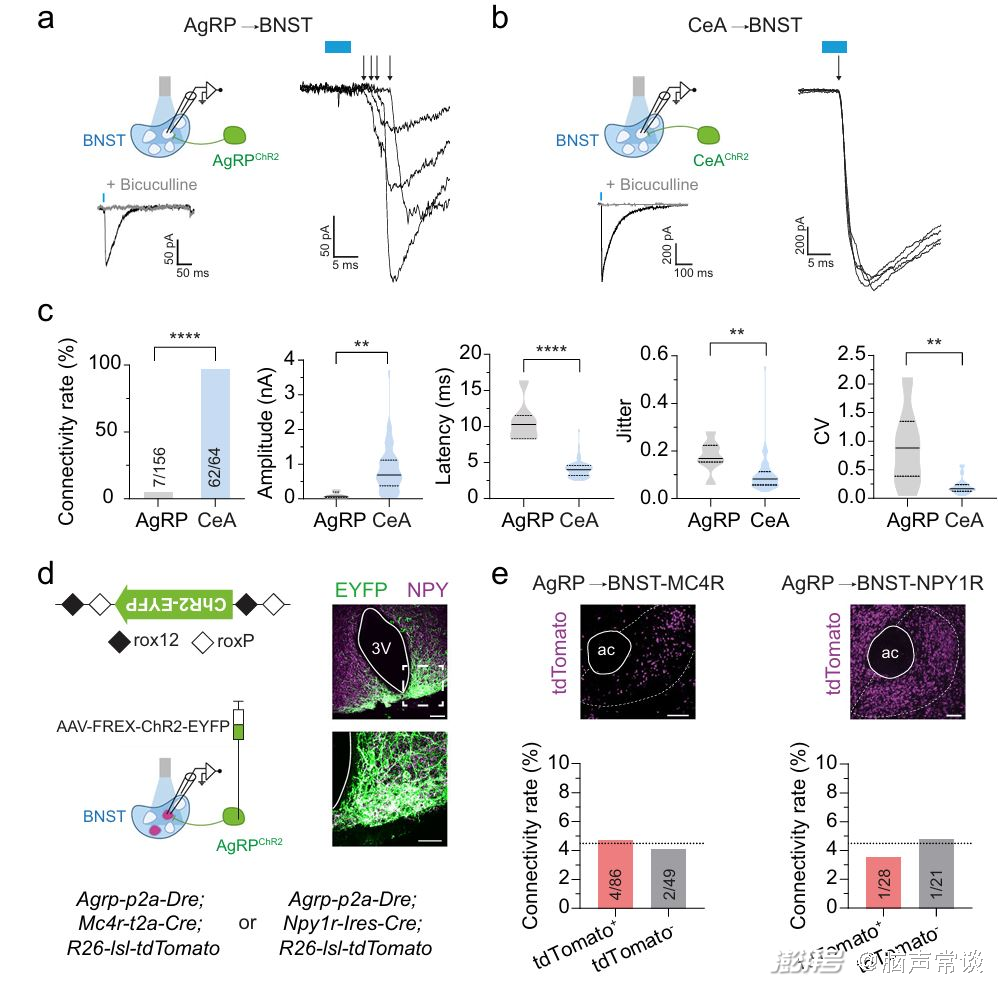
2. GABA能AgRP→BNST和CeA→BNST突触具有不同的特性
在光刺激AgRPChR2和CeAChR2小鼠的BNST投射时,摄食行为出现了相反的变化,这提示GABA能AgRP→BNST和CeA→BNST输入在控制下游BNST神经元活动的机制上具有本质上的不同特征。作者采用了光遗传学与电生理学结合的方法从AgRPChR2和CeAChR2小鼠中制备了急性脑片,并对投射区域内的BNST神经元进行了全细胞膜片钳记录。记录到的抑制性突触后电流(eIPSCs)完全被GABAA受体拮抗剂荷包牡丹碱所阻断,证实了两种输入是GABA能。记录分析揭示了AgRP→BNST和CeA→BNST突触间传递的显著差异,AgRP→BNST回路的响应率低于CeA→BNST回路。此外,AgRPChR2小鼠记录到的eIPSC幅度较小,而潜伏期较长。作者从突触前功能的特性参数发现AgRP→BNST和CeA→BNST回路之间存在明显差异。这些发现表明,AgRP→BNST突触的GABA能传递弱且不可靠,而CeA→BNST突触的传递则强大而高效。
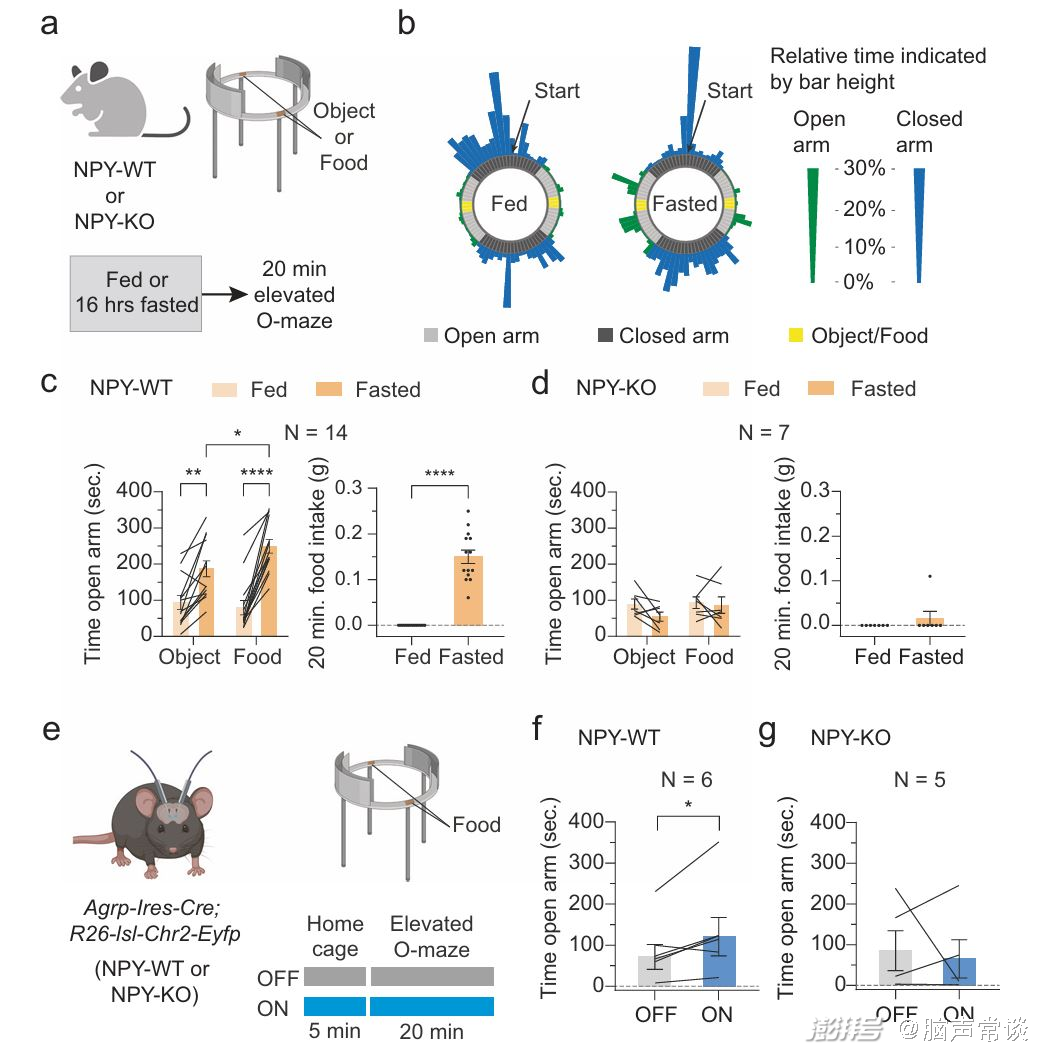
3. NPY缺失消除了焦虑环境下对摄食行为的调整
AgRP神经元和CeA神经元向BNST的投射调节了与焦虑相关行为的环境依赖性适应,即在禁食状态下NPY对于触发这两个回路突触可塑性的必要性,作者接下来运用高架O迷宫(Elevated O-maze, EOM)测试探索NPY缺乏如何影响能量状态依赖的行为变化。在开放臂的中间区域放置物体或食物颗粒,与热量限制能够减少焦虑样行为一致,禁食状态下的NPY-WT小鼠在开放臂上花费的时间明显增多,同时伴随食物获取和消耗的增加。尽管禁食的NPY-WT小鼠在总运动距离上没有变化,但它们在进入开放区域之前的封闭臂停留时间更长(潜伏期增加)。NPY-KO小鼠在EOM中的行为结果表明禁食诱导的开放臂停留时间和食物获取增加完全消失。此外,禁食的NPY-KO小鼠在EOM中也没有表现出食物摄入的增加,这证明了NPY的作用对于在饥饿引起的焦虑环境中增加觅食行为以获取和消耗食物是必要的。在家笼中重新提供食物后的前20分钟内,NPY-WT和NPY-KO小鼠的食物摄入量没有显著差异,但60分钟后,NPY-KO小鼠的食物摄入量明显较低。此外,光遗传学激活NPY-KO小鼠BNST中的AgRPChR2神经元引起的摄食反应明显减弱,禁食引起的焦虑信号减少是由AgRP神经元释放的NPY介导的。作者在表达ChR2的AgRP神经元的NPY-WT和NPY-KO小鼠的BNST双侧植入光纤研究AgRP神经元来源的NPY通过BNST调节焦虑相关行为调整的作用。结果表明由激活的AgRP神经元增加释放的NPY通过BNST调整了与焦虑相关的行为。
综上所述,该研究揭示了一种突触可塑性机制,该机制根据能量状态调整控制饥饿和焦虑信号的关键神经回路。研究强调了NPY在整合饥饿感知、焦虑反应及相应行为调整中的核心作用,特别是在能量缺乏时,通过AgRP神经元介导的NPY释放,能够精细调节涉及摄食和情绪的关键神经回路,从而影响动物对环境的适应性行为。这一成果不仅增进了对大脑如何根据身体能量状态调整行为策略的理解,也为开发针对饮食障碍和相关精神健康问题的新疗法提供了理论依据和潜在的干预靶标。
文章来源:https://doi.org/10.1038/s41467-024-49766-0
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




