- +1
【前沿进展】PNAS | 陈扬、黄超揭示Rab10-CAV1介导迁移体内纳米囊泡转运的机制
2024-07-19 19:35
来源:澎湃新闻·澎湃号·政务
字号
细胞采用多种途径进行细胞间以及细胞与外部环境之间的通信。迁移体是清华大学俞立教授于2015年报道的细胞器结构。迁移体细胞迁移过程中,尾部留下的收缩丝的尖端或分叉点上形成的囊泡状结构,是细胞间通讯的重要介质。
电子显微镜发现迁移体内部含有许多纳米囊泡(图1),这些囊泡也是迁移体区别于其他细胞器的重要结构特征,也是迁移体内容物的关键组成部分。这些纳米囊泡运输到迁移体的机制仍然是个谜题,这些囊泡的性质和功能也仍未被解析。
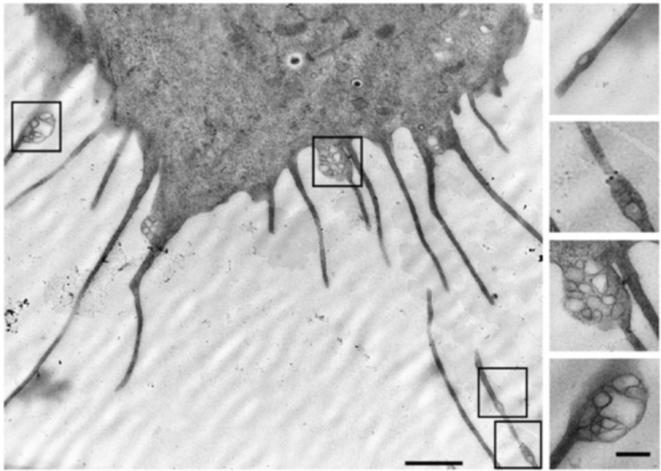 图1 细胞原位电镜图片展示收缩丝、迁移体和迁移体内部的纳米囊泡(发表文章内图片)。
图1 细胞原位电镜图片展示收缩丝、迁移体和迁移体内部的纳米囊泡(发表文章内图片)。2024年7月16日,北京大学临床医学高等研究院陈扬团队、协和医院黄超兰教授在PNAS期刊发表了题为:Rab10-CAV1 mediated intraluminal vesicle transport to migrasomes的研究论文。该研究阐述了迁移体内特征性纳米囊泡的性质和运输途径,揭示了细胞通过迁移体进行蛋白质分选和细胞外释放的机制。
 在本研究中,通过对细胞内介导囊泡转运的核心蛋白Rab GTPase家族的36个蛋白的定位筛选,发现Rab10特异性定位在迁移体的内部。通过蛋白质谱方法鉴定Rab10和Caveolin-1 (CAV1) 标记了迁移体内的纳米囊泡。同时,Rab10-CAV1囊泡转运到迁移体需要动力蛋白Myosin Va和接头蛋白RILPL2。同时,LRRK2激酶对Rab10的磷酸化调节了这一转运机制(图2)。研究明确了功能蛋白CSF-1是通过迁移体内纳米囊泡这一途径释放,在皮肤创面愈合过程中促进单核-巨噬细胞分化。该研究揭示了细胞通过迁移体中纳米囊泡进行蛋白质分选和细胞外释放的机制,建立了细胞在Rab GTP酶、接头蛋白、动力蛋白的介导下,依赖细胞骨架,转运纳米囊泡的到迁移体的新运输模式,从而促进了对迁移体的功能作用及其对细胞间通讯的影响的理解。
在本研究中,通过对细胞内介导囊泡转运的核心蛋白Rab GTPase家族的36个蛋白的定位筛选,发现Rab10特异性定位在迁移体的内部。通过蛋白质谱方法鉴定Rab10和Caveolin-1 (CAV1) 标记了迁移体内的纳米囊泡。同时,Rab10-CAV1囊泡转运到迁移体需要动力蛋白Myosin Va和接头蛋白RILPL2。同时,LRRK2激酶对Rab10的磷酸化调节了这一转运机制(图2)。研究明确了功能蛋白CSF-1是通过迁移体内纳米囊泡这一途径释放,在皮肤创面愈合过程中促进单核-巨噬细胞分化。该研究揭示了细胞通过迁移体中纳米囊泡进行蛋白质分选和细胞外释放的机制,建立了细胞在Rab GTP酶、接头蛋白、动力蛋白的介导下,依赖细胞骨架,转运纳米囊泡的到迁移体的新运输模式,从而促进了对迁移体的功能作用及其对细胞间通讯的影响的理解。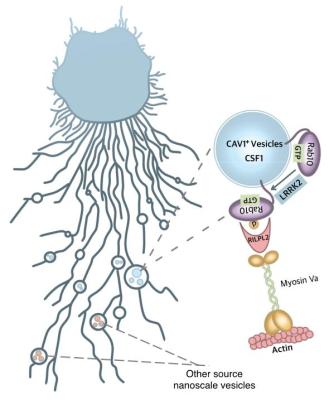 图2. Rab10-CAV1纳米囊泡转运到迁移体的过程和调控机制(发表文章内图片)。
图2. Rab10-CAV1纳米囊泡转运到迁移体的过程和调控机制(发表文章内图片)。北京大学临床医学高等研究院陈扬副研究员、协和医院黄超兰教授为本文的共同通讯作者。北京大学生命科学联合中心博士研究生黎勇、北京大学医学部基础医学院博士研究生文艺玲为本文共同第一作者。
原文链接:
https://www.pnas.org/doi/10.1073/pnas.2319267121
原标题:《【前沿进展】PNAS | 陈扬、黄超揭示Rab10-CAV1介导迁移体内纳米囊泡转运的机制》
特别声明
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。
+1
收藏
我要举报





查看更多
澎湃矩阵
新闻报料
- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司
反馈




