- +1
【前沿进展】JMCB丨朱学良和鄢秀敏团队发现支撑动纤毛中央微管的亚结构-中央微管基座
动纤毛是一种突出于细胞表面的富含微管的毛发状细胞器,通过摆动驱动细胞运动和胞外液体流动。动纤毛大多以多纤毛的形式分布于气管、脑室和输卵管等器官,参与呼吸道清洁、脑脊液循环和生殖细胞运输等,而精子鞭毛以单根形式存在,驱动精子的运动【1-3】。动纤毛结构和功能异常会引发原发性纤毛运动障碍综合征(primary ciliary dyskinesia,PCD),主要病征为反复呼吸道感染、脑积水和不育等【4】。动纤毛由基体、转接区、纤毛膜和轴丝等部分组成,大部分的动纤毛轴丝由9组外周二联体微管(peripheral microtubles doublets)和2根中央微管(C1和C2)构成。中央微管及其附属物对于调控纤毛的摆动模式至关重要【5-8】。然而,这对中心微管的末端是如何固定在转接区之上,从而维持动纤毛中央器的正常功能,尚不清楚。
近日,中国细胞生物学学会监事、中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)朱学良研究组联合上海交通大学医学院附属新华医院鄢秀敏团队在Journal of Molecular Cell Biology上在线发表了题为A polarized multicomponent foundation upholds ciliary central microtubules的研究论文。该研究发现并解析了支撑动纤毛中央微管的亚结构-中央微管基座(CP-foundation , CPF)。
 该团队前期研究发现哺乳动物多纤毛细胞特有的纤维状颗粒物(fibrogranular materials,FGMs)富集大量的中心粒和纤毛蛋白,保证了动纤毛精细结构的有序组装。在研究中,研究人员首次发现FGMs富集的Cep131 和Centrin共定位于动纤毛基部的中央腔区域,而且随着纤毛成熟,该结构的长度可达到2 µm。由于这一结构特异性分布于中央微管的基部,于是在该工作中将其命名为中央微管足(CP-foot)【9】。
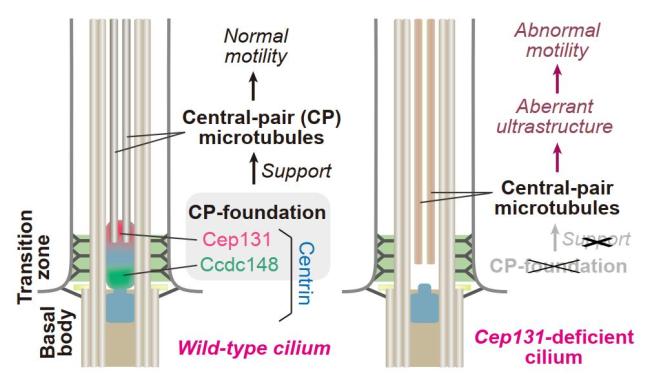
该团队前期研究发现哺乳动物多纤毛细胞特有的纤维状颗粒物(fibrogranular materials,FGMs)富集大量的中心粒和纤毛蛋白,保证了动纤毛精细结构的有序组装。在研究中,研究人员首次发现FGMs富集的Cep131 和Centrin共定位于动纤毛基部的中央腔区域,而且随着纤毛成熟,该结构的长度可达到2 µm。由于这一结构特异性分布于中央微管的基部,于是在该工作中将其命名为中央微管足(CP-foot)【9】。在近日发表的研究中,该研究团队对这一结构进行了更为深入细致的观察和功能分析。为了能更好的区分它与另一纤毛相关超微结构基足(basal foot),研究人员将其重新命名为中央微管基座(CP-foundation; CPF)。为了进一步明确CPF在动纤毛中的空间位置,研究人员利用结构照明显微镜(3D-SIM)观察分析了CPF与动纤毛其他超微结构(包括转接区、基体远端和中央微管等)的空间位置关系,发现CPF从基体远端伸出并穿过转接区包裹住中央微管的负端。随后,研究人员利用中央微管缺失小鼠(Wdr47-/-)发现CPF的组装并不依赖于中央微管。通过APEX2邻近标记技术,该团队鉴定出26个CPF候选蛋白,其中Ccdc148定位于CPF近端,与Cep131富集在远端的分布互补,提示可能由多个蛋白复合物共同构筑了这个中央微管支撑平台。进化分析表明CPF组分Centrin、Ccdc131和Ccdc148从原生动物到哺乳动物都较为保守,提示CPF是一个进化保守的多组分超微结构。
为了探究CPF的生理功能,研究团队构建了Cep131敲除小鼠,发现Cep131缺失并不影响纤毛形成,但是会导致CPF结构的消失,进而造成中央微管落入转接区并影响纤毛的运动能力,最终引发Cep131缺失小鼠出现晚发性脑积水。
 综上所述,这项研究首次系统阐明了哺乳动物纤毛中央微管的支撑机制,为理解纤毛的组装和功能提供了新的视角,有助于进一步揭示原发性纤毛运动障碍综合征的致病机理。
综上所述,这项研究首次系统阐明了哺乳动物纤毛中央微管的支撑机制,为理解纤毛的组装和功能提供了新的视角,有助于进一步揭示原发性纤毛运动障碍综合征的致病机理。上海交通大学医学院附属新华医院助理研究员陈青霞和山东师范大学赵惠杰教授为本文第一作者,分子细胞科学卓越创新中心朱学良研究员和上海交通大学医学院附属新华医院鄢秀敏研究员为本文通讯作者。
原文链接:
https://academic.oup.com/jmcb/advance-article/doi/10.1093/jmcb/mjae031/7737774?searchresult=1
来源:BioArtMED
参考文献
1. Breslow, D.K. and A.J. Holland, Mechanism and Regulation of Centriole and Cilium Biogenesis. Annu Rev Biochem, 2019. 88: p. 691-724.
2. Nigg, E.A. and J.W. Raff, Centrioles, centrosomes, and cilia in health and disease. Cell, 2009. 139(4): p. 663-78.
3. Bettencourt-Dias, M., et al., Centrosomes and cilia in human disease. Trends Genet, 2011. 27(8): p. 307-15.
4. Fliegauf, M., T. Benzing, and H. Omran, When cilia go bad: cilia defects and ciliopathies. Nat Rev Mol Cell Biol, 2007. 8(11): p. 880-93.
5. Reiter, J.F. and M.R. Leroux, Genes and molecular pathways underpinning ciliopathies. Nat Rev Mol Cell Biol, 2017. 18(9): p. 533-547.
6. Lyu, Q., et al., Formation and function of multiciliated cells. J Cell Biol, 2024. 223(1).
7. Liu, H., et al., Wdr47, Camsaps, and Katanin cooperate to generate ciliary central microtubules. Nat Commun, 2021. 12(1): p. 5796.
8. Zhao, L., et al., The unity and diversity of the ciliary central apparatus. Philos Trans R Soc Lond B Biol Sci, 2020. 375(1792): p. 20190164.
9. Zhao, H., et al., Fibrogranular materials function as organizers to ensure the fidelity of multiciliary assembly. Nat Commun, 2021. 12(1): p. 1273.
原标题:《【前沿进展】JMCB丨朱学良和鄢秀敏团队发现支撑动纤毛中央微管的亚结构-中央微管基座》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




