- +1
Cell子刊:激活肠道IL-22通路,治疗肥胖及非酒精性脂肪肝
原创 生物世界 生物世界
编辑丨王多鱼
排版丨水成文
代谢功能障碍相关脂肪性肝病(MASLD,也就是之前的非酒精性脂肪性肝病)的发病率呈指数级上升,这与人们越来越多地食用高能量饮食(高糖高脂饮食)有关,因此迫切需要有效的MASLD治疗药物。
2024年9月23日,加州大学圣地亚哥分校 Michael Karin 团队在 Cell 子刊 Cell Metabolism 上发表了题为:IL-22 resolves MASLD via enterocyte STAT3 restoration of diet-perturbed intestinal homeostasis 的研究论文。该研究表明,肠道特异性激活IL-22通路,可治疗肥胖和MASLD/MASH。

代谢功能障碍相关脂肪性肝病(MASLD)的发病率在最近20-30年里急剧上升,这与饮食中糖和脂肪摄入量的指数级增长同步,使其成为最常见的代谢紊乱之一。MASLD与脂毒性、胰岛素抵抗、2型糖尿病(T2D)、肝脏应激性炎症和免疫途径的代谢激活以及微生物菌群失调有关,是克罗恩病(CD)的常见共病。“肠道-肝脏轴”被提出为MASLD发病的关键因素之一,通过门静脉将肠道微生物代谢物和炎症介质输送到肝脏,包括过度摄入高能量密度和高度加工食品的行为和饮食因素。尽管进行了大量研究,但目前只有一种MASLD治疗药物获准临床使用,此外,GLP-1受体激动剂可以缓解脂肪变性,但不能缓解肝脏纤维化。
白细胞介素-22(IL-22)是由固有淋巴细胞和Th17/22细胞产生的一种屏障保护性、抗微生物细胞因子,其向肠道上皮细胞(IEC)的信号传递会受到破坏屏障的高果糖和高脂肪饮食的抑制。
内源性IL-22被认为可以预防由饮食引起的代谢紊乱,并抑制脂质代谢,同时塑造肠道微生物群。重组IL-22Fc融合蛋白在动物模型中改善了2型糖尿病、MASLD及其相关代谢疾病,并正在2期临床试验中进行剂量递增安全性和有效性研究,以评估其在酒精性肝炎中的作用,尽管其作用机制尚不清楚。
由于IL-22Fc在急性肝炎和高脂肪饮食诱导的肝脏脂肪变性模型中具有保护作用,并降低了脂质合成酶的表达,因此推测它可以直接影响肝细胞。然而,IL-22还可以加强肠道上皮屏障并恢复肠道菌群失调,这些作用也可能有助于解决肝脏脂肪变性和与代谢紊乱相关脂肪性肝炎(MASH)。
该研究发现,诱导MASH的高果糖饮食(HFrD)会抑制结肠IL-22信号通路。因此,研究团队使用了其他由饮食诱导的MASLD模型,并通过条件性敲除小鼠肝脏或小肠上皮细胞中的IL-22受体α1亚基(IL-22Ra1),进一步研究饮食对IL-22信号通路的影响,并确定IL-22Fc在何处以及如何发挥其治疗作用。
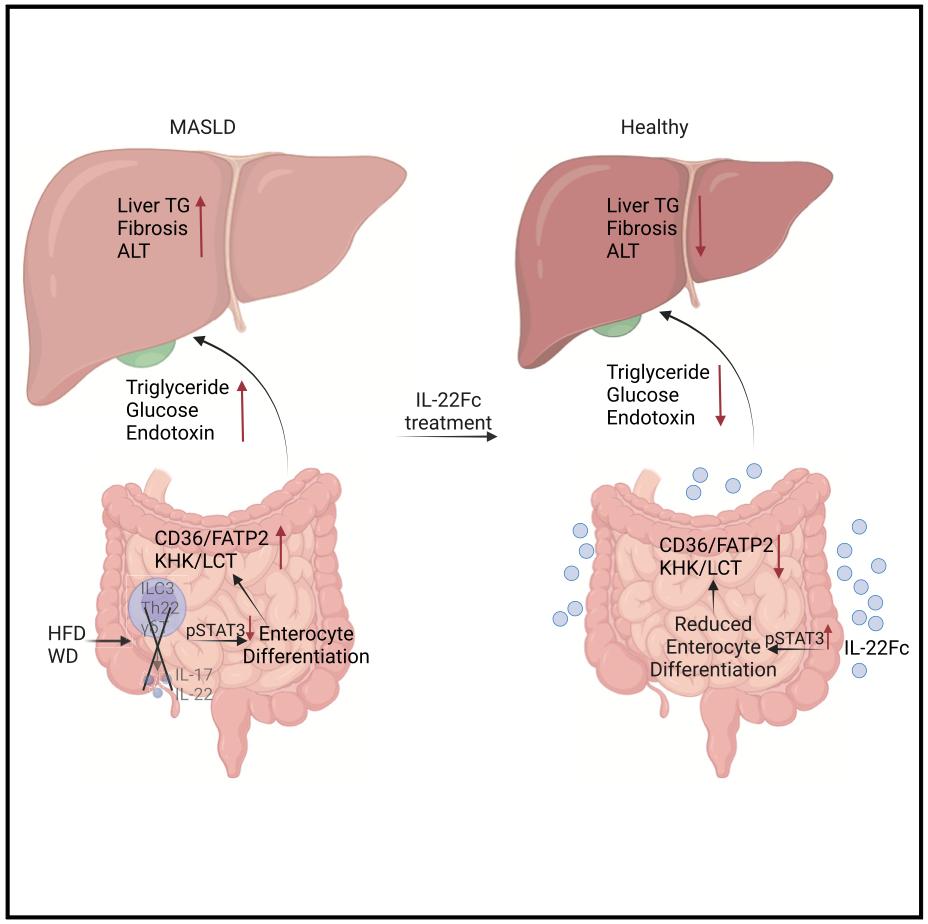
在这项最新研究中,研究团队描述了一个恶性循环:长期摄入高能量密度饮食会抑制小肠固有淋巴样细胞3型细胞(ILC3)中的IL-22表达,并改变肠道上皮细胞(IEC)的分化和成熟,以增加脂肪和糖的吸收。而这些效应可通过外源性的IL-22Fc逆转,从而导致MASLD的缓解。
具体来说,MASLD的发病机制与肥胖、糖尿病、“肠道-肝脏轴”功能紊乱以及缺陷性白细胞介素-22(IL-22)信号通路有关。尽管IL-22能够保护屏障功能,抑制代谢紊乱、脂肪摄入以及微生物失调,但肥胖诱导饮食会迅速抑制小肠内固有淋巴细胞产生的IL-22。这导致肠道上皮细胞(IEC)中的STAT3抑制,并扩大吸收性肠上皮细胞的数量。这些可维持MASLD的异常现象可通过注射重组IL-22得到逆转,从而解决肝脂肪变性、炎症、纤维化和胰岛素抵抗等问题。
外源性IL-22通过IEC受体发挥治疗作用,而不是通过肝脏细胞,激活STAT3并抑制WNT-β-catenin信号通路,从而缩小吸收性肠上皮细胞的数量。通过逆转饮食强化的宏量营养素吸收,即肝脏脂质的主要来源,恢复IL-22信号通路,代表了一种可能有效的预防饮食性肥胖和MASLD的方法。
论文链接:
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(24)00364-4
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




