- +1
Cell Rep:少突胶质细胞引风霜!浙大徐贞仲团队揭示少突胶质细胞炎症关键通路
帕金森病(PD)是一种常见的神经退行性疾病,由于其发病机制不清治疗颇具难度。近期研究发现,少突胶质细胞与帕金森病进展之间存在显著关联,但少突胶质细胞如何调控帕金森病的发病机制仍不明确。
基于此,2025年2月4日浙江大学医学院附属第一医院麻醉科徐贞仲研究团队在Cell Reports杂志发表了“Oligodendrocytes drive neuroinflammation and neurodegeneration in Parkinson’s disease via the prosaposin-GPR37-IL-6 axis”揭示了少突胶质细胞通过PSAP-GPR37-IL-6轴,在帕金森病中引发神经炎症和神经退行性变。

作者发现黑质少突胶质细胞中G蛋白偶联受体37(GPR37)表达上调,且帕金森病小鼠体内鞘脂激活蛋白原(PSAP)的分泌增加。释放的PSAP可通过GPR37依赖的途径诱导少突胶质细胞中白细胞介素(IL)-6表达上调并分泌,进而加剧神经炎症、多巴胺能神经元变性以及行为缺陷。少突胶质细胞中GPR37缺失可在多种帕金森病模型中预防神经退行性变。最后,在帕金森病患者中也观察到了PSAP - GPR37 - IL - 6轴的特征。因此,研究结果表明,多巴胺能神经元通过分泌的PSAP与少突胶质细胞相互作用,同时确定了PSAP-GPR37- IL-6轴是帕金森病发病机制的驱动因素,也是一个潜在的治疗靶点,或许能够减缓帕金森病患者的病情进展。
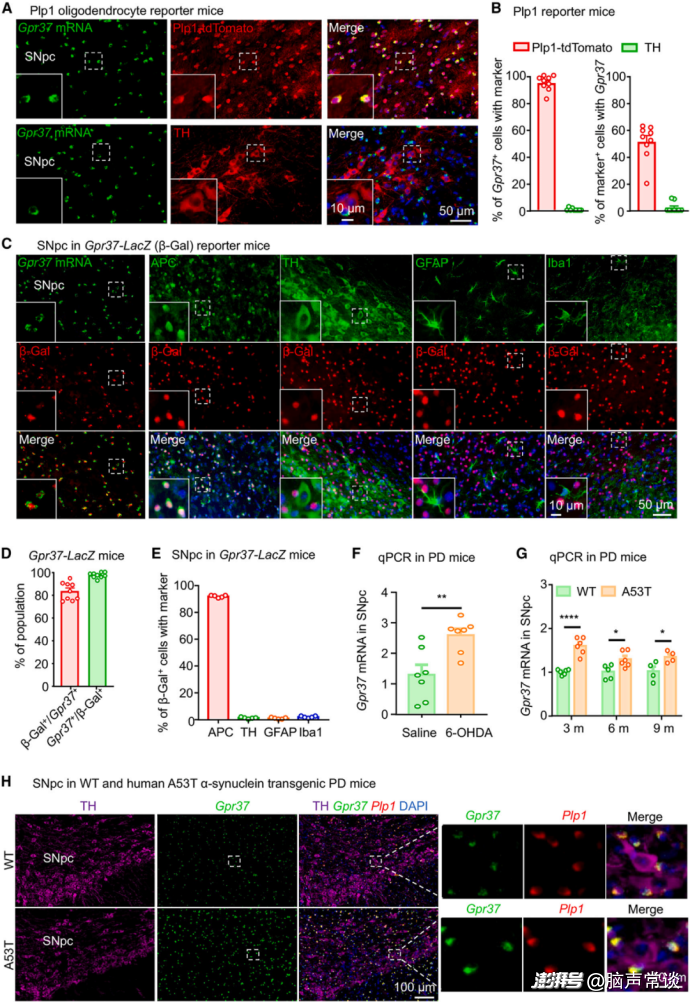
图一 GPR37特异性地在少突胶质细胞中表达,且在帕金森病模型的SNpc上调
为了探究GPR37在中脑黑质致密部(SNpc)的表达模式,作者首先采用原位杂交技术在Plp1-Cre/ER;Ai14少突胶质细胞报告基因小鼠的SNpc中探测Gpr37 mRNA。Gpr37在tdTomato阳性的少突胶质细胞中特异性表达,而在酪氨酸羟化酶(TH,一种多巴胺能神经元标志物)阳性的多巴胺能神经元中不表达。还利用Gpr37 - LacZ报告基因小鼠(其Gpr37基因座中含有细菌β -半乳糖苷酶(β - gal)报告基因)来评估Gpr37 mRNA在SNpc中的表达情况。发现表达Gpr37的细胞核(由β - gal标记)主要出现在腺瘤性结肠息肉病蛋白(APC)阳性的少突胶质细胞中,并且未发现β - gal标记的细胞核与TH、Iba1或GFAP共定位。为了探究GPR37在PD发展中的潜在作用,作者评估了Gpr37 mRNA在6 - 羟基多巴胺(6-OHDA)中毒诱导的PD小鼠、人A53T α - 突触核蛋白转基因PD小鼠以及腺相关病毒介导的hA53T - αSyn过表达PD小鼠的SNpc中的表达情况。6 - OHDA注射1周后,SNpc中的Gpr37 mRNA明显增加。同样,在A53T转基因小鼠和AAV - αSyn注射的PD小鼠中,尤其是在早期,Gpr37 mRNA也上调。此外,在hA53T转基因小鼠和AAV - αSyn注射的PD小鼠的SNpc中,Gpr37 mRNA仍局限于Plp1阳性的少突胶质细胞中。这些结果表明,GPR37在少突胶质细胞中选择性表达,并且在PD模型的SNpc中显著上调。
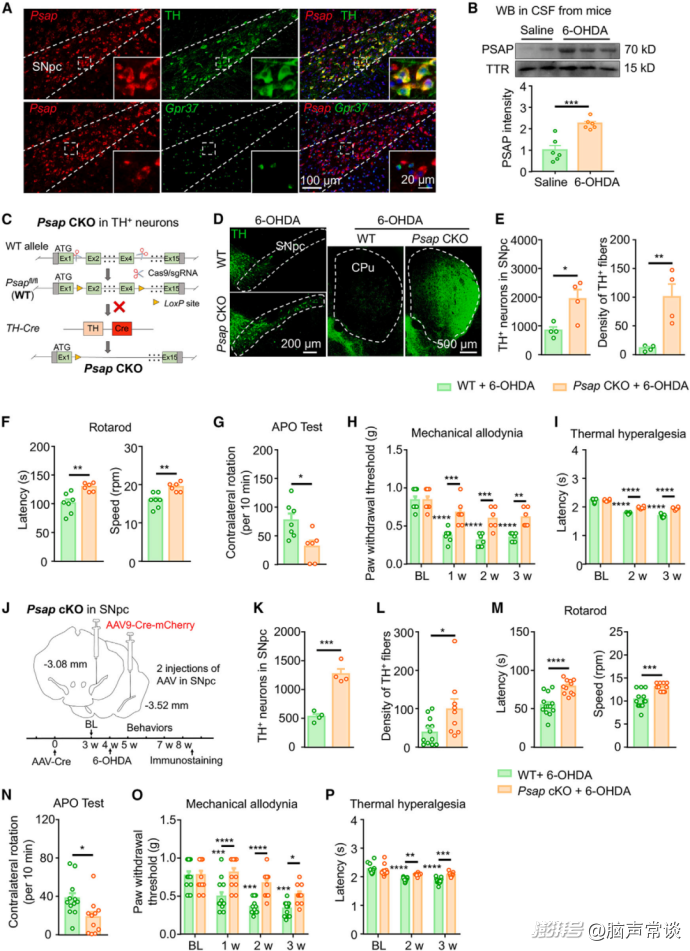
图二 PSAP在多巴胺能神经元中富集,PSAP缺失可缓解PD相关的神经退行性病变
作者进一步探究PSAP对PD进展的潜在影响。发现PSAP在中脑黑质致密部(SNpc)的TH阳性多巴胺能神经元中选择性富集。此外,在注射6-OHDA的帕金森病小鼠的脑脊液中,PSAP蛋白水平明显升高。为了研究PSAP在帕金森病发展中的作用,作者通过将PSAPfl/fl小鼠(野生型,WT)与TH - Cre小鼠杂交培育出PSAP条件性敲除(CKO)小鼠。与野生型小鼠相比,PSAP CKO小鼠的DA神经元中PSAP的表达基本消失。PSAP CKO小鼠的黑质DA神经元数量和纹状体DA纤维密度与野生型小鼠相当。PSAP CKO小鼠的运动功能和基础痛觉水平也表现正常。注射6 - OHDA后,PSAP CKO小鼠的DA神经元损失明显减少。与野生型小鼠相比,注射6 - OHDA的PSAP CKO小鼠对行为异常表现出显著的抗性。同样,PSAP CKO小鼠的病理性α - 突触核蛋白(αSyn)积累和DA神经元变性得到缓解。注射AAV - αSyn的PSAP CKO小鼠对运动障碍也表现出显著的抗性。为了进一步证实帕金森病相关的神经变性是否依赖于SNpc中PSAP的局部表达,通过立体定向将AAV - Cre - mCherry注射到PSAPfl/fl小鼠的SNpc中条件性敲除SNpc中的PSAP。PSAP cKO小鼠的SNpc中PSAP表达被有效消除。然而,PSAP cKO小鼠在基础运动功能或基础痛觉感受方面没有缺陷。重要的是,6 - OHDA诱导的DA神经元变性在PSAP cKO小鼠中基本被消除。此外,PSAP缺失的小鼠在伴随的行为缺陷方面有显著改善。这些结果表明PSAP主要在黑质的DA神经元中表达,且帕金森病相关的DA神经元变性依赖于PSAP。
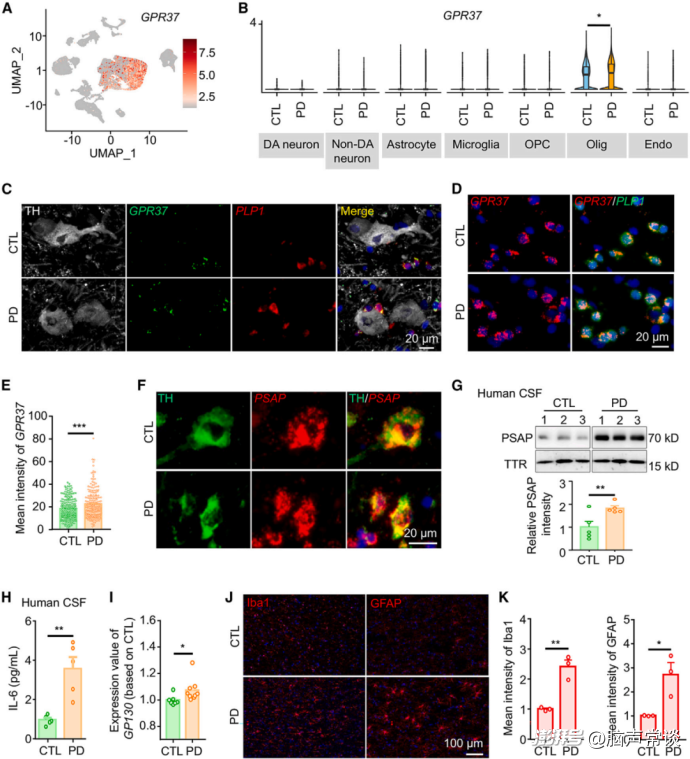
图三 在帕金森病患者中观察到PSAP - GPR37 - IL - 6轴的特征
作者最后探究了研究结果对PD临床治疗是否具有转化应用的潜力。为了探寻GPR37在人类帕金森病中的潜在关联,利用了帕金森病患者死后SNpc的单细胞核糖核酸测序数据集。通过对特定细胞类型标记基因的聚类分析,识别出了SNpc内的七个不同细胞群,其中包括少突胶质细胞和多巴胺能神经元。发现在帕金森病患者和健康对照者的SNpc中,GPR37都特异性地在少突胶质细胞中表达。帕金森病患者SNpc内少突胶质细胞中的GPR37表达显著升高。此外,在另一组独立的帕金森病患者队列中,GPR37的表达水平也显著增加。这些发现表明,少突胶质细胞中的GPR37与人类帕金森病可能存在潜在联系。此外,在人类脑切片中,PSAP mRNA在DA神经元中富集,并且帕金森病患者脑脊液中的PSAP蛋白显著增加。随后,通过酶联免疫吸附测定(ELISA)比较了脑脊液样本中的白细胞介素 - 6(IL - 6)水平,发现与对照组相比,帕金森病患者脑脊液中的IL - 6蛋白明显升高。还发现散发性帕金森病患者SNpc中gp130 mRNA的表达显著增加。此外,在帕金森病患者的SNpc切片中检测到了小胶质细胞和星形胶质细胞的异常激活。因此,作者证实了PSAP和GPR37在人类死后SNpc中的表达,以及帕金森病患者脑脊液中PSAP和IL - 6水平的升高,这表明PSAP - GPR37 - IL - 6信号轴与帕金森病的临床表现可能存在潜在关联。
总结
少突胶质细胞通过PSAP-GPR37-IL-6 信号轴驱动类似帕金森病的神经退化。在帕金森病小鼠中,GPR37 在少突胶质细胞中上调,且PSAP的分泌增加。释放的PSAP可以通过 GPR37 信号诱导少突胶质细胞中 IL-6 的上调和分泌,从而增强神经炎症、导致多巴胺神经元退化及行为缺陷。多巴胺能神经元通过分泌PSAP与少突胶质细胞相互作用,PSAP- GPR37 - IL - 6轴驱动PD发病,有望成为减缓PD进展的潜在治疗靶点。
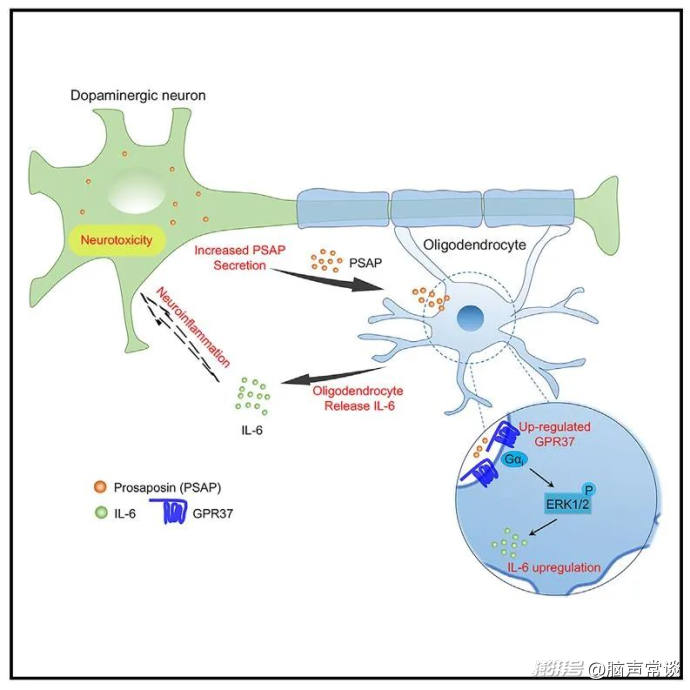
图四 全文摘要总结
文章来源:https://doi.org/10.1016/j.celrep.2025.115266
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




