- +1
哈佛医学院研究发现:激活B细胞,可提升TIL细胞疗法成功率2倍
在癌症治疗领域,TIL(肿瘤浸润性淋巴细胞)疗法曾被誉为最有希望的个体化免疫疗法之一。
然而,如何稳定高效地扩增TIL细胞,始终是制约其普及和疗效提升的关键难题。
近日,哈佛医学院附属达纳-法伯癌症研究院团队发布重磅研究:通过激活肿瘤局部的B细胞,仅仅一个环节的改进,就能将TIL扩增成功率提高近2倍,从33%跃升至67%。
这一发现不仅刷新了对肿瘤免疫微环境的理解,也为提升TIL疗法的治疗效果、加速其应用普及,打开了新的突破口。
细胞战争的战局,正在被悄悄改写。
01 TIL疗法:曾被寄予厚望,也面临现实难题
TIL疗法,即肿瘤浸润性淋巴细胞治疗(Tumor-Infiltrating Lymphocyte Therapy),是一种高度个体化的免疫疗法。
它的基本逻辑简单而有力:从患者自身肿瘤组织中提取已经自然渗透进去的T细胞,这些T细胞本身具备识别并攻击肿瘤细胞的潜力。经过体外扩增和激活后,再大剂量回输体内,强化免疫攻击力,从而清除癌细胞。
TIL疗法的临床效果令人振奋。在黑色素瘤、宫颈癌、非小细胞肺癌等实体瘤中,部分患者实现了深度缓解,甚至完全缓解。
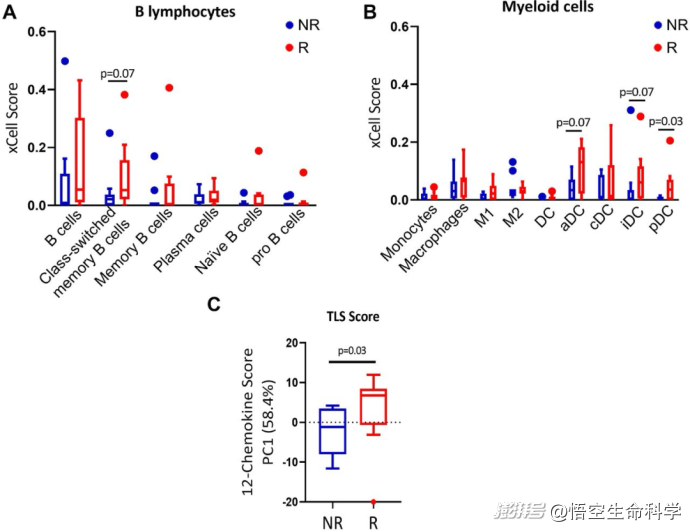
黑色素瘤TIL治疗的反应者(R)和非反应者(NR)的免疫细胞含量分析
美国FDA也于2024年批准了首款TIL疗法(Lifileucel)用于晚期黑色素瘤患者,标志着这一疗法正式进入主流癌症治疗体系。
然而,TIL疗法的推广并不容易,最大的问题在于:
扩增难度高:并非每个患者的TIL都能在体外顺利扩增到治疗所需数量;
扩增失败率高:传统流程下,TIL扩增成功率仅约30%-40%;
细胞质量参差不齐:即便扩增成功,不同患者TIL中抗肿瘤活性的T细胞比例差异巨大,影响治疗效果。
换句话说,TIL疗法就像一场赌博,很多时候并不是医生技术不到位,而是患者肿瘤组织内本身缺乏足够有战斗力的细胞种子。
因此,如何提升TIL扩增成功率、提高细胞质量,成为制约这一疗法全面普及的核心瓶颈。
哈佛医学院附属达纳-法伯癌症研究院团队,正是瞄准了这个“扩增困局”,提出了一个出人意料又极具说服力的解法:激活肿瘤微环境中的B细胞。
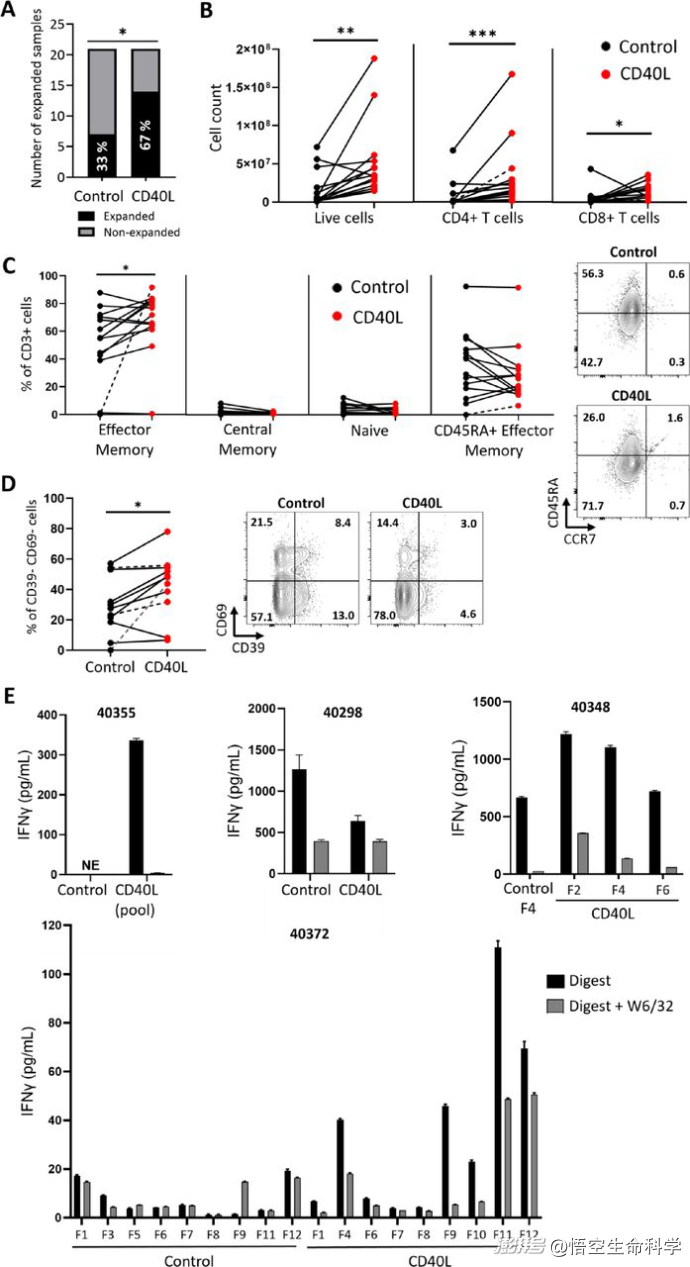
CD40L增强了黑色素瘤TIL的扩张。黑色素瘤单细胞悬浮液在标准TIL膨胀培养基(对照)或补充CD40(CD40L)激动剂的培养基中培养3-4周
02 哈佛团队新发现:激活B细胞,TIL扩增成功率翻倍
在这项由哈佛医学院附属达纳-法伯癌症研究院主导的研究中,科学家们提出了一个颠覆传统的假设:肿瘤组织中的B细胞,不是旁观者,而是TIL扩增成功与否的重要推手。
通过对黑色素瘤患者样本的系统分析,研究团队发现:
TIL扩增成功的患者肿瘤组织中,B细胞尤其是“类切换记忆B细胞(class-switched memory B-cells)”的比例显著更高(p=0.007)。
三次淋巴结构(TLS,类似小型淋巴结的微环境结构)评分也更高(p=0.03),而TLS往往富含活跃的B细胞群体。
进一步的实验验证了B细胞在TIL扩增过程中的重要性。
研究者在传统TIL扩增体系中,加入了CD40配体(CD40L)——一种能强烈激活B细胞的分子信号。
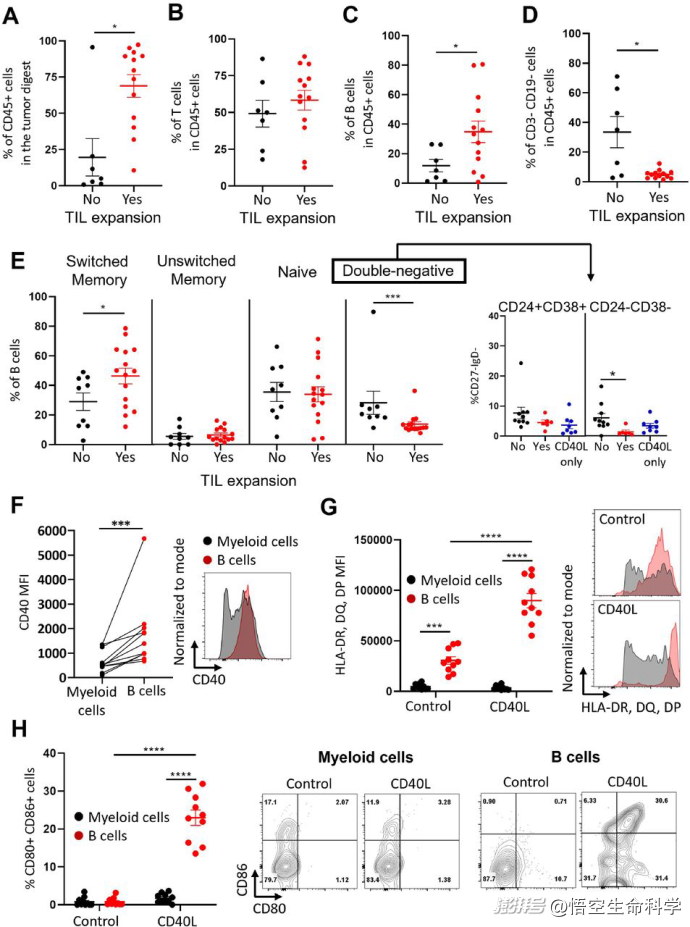
浸润的黑色素瘤B细胞对CD40L的反应对配体进行上调
结果非常惊人:加入CD40L后,TIL扩增成功率从原本的33%跃升至67%(p=0.03),接近翻倍;扩增出来的TIL中,具有更年轻表型(CD39- CD69-)的T细胞比例更高;新抗原特异性的T细胞克隆数量明显增加,提示抗肿瘤活性更强。
不仅在黑色素瘤中,在非小细胞肺癌(NSCLC)样本中,CD40L激活策略同样有效——TIL扩增速度加快(节省一周培养时间);新抗原反应性T细胞数量增加(p≤0.01)。
更深入的单细胞转录组分析揭示,CD40L几乎专门刺激了肿瘤B细胞,诱导它们上调共刺激分子(如CD83、CD58)和趋化因子(如CCL22、CCL17),从而为T细胞扩增创造了更有利的局部免疫环境。
简而言之,CD40L激活B细胞,就像在肿瘤微环境中点燃了一场“细胞动员令”,让沉睡的T细胞得到更好支持、迅速成长为可以用于治疗的免疫大军。
03 激活B细胞:一场改变TIL疗法未来格局的微创新
在以往的癌症免疫治疗研究中,B细胞往往被忽略。
人们习惯将注意力集中在T细胞,尤其是杀伤性T细胞(CD8+ T细胞)上,认为它们是对抗肿瘤的主力军。
但哈佛医学院附属达纳-法伯团队的这项研究颠覆了这一传统认知:B细胞不仅是“配角”,在TIL扩增乃至疗效提升中,可能是关键的“助推器”。
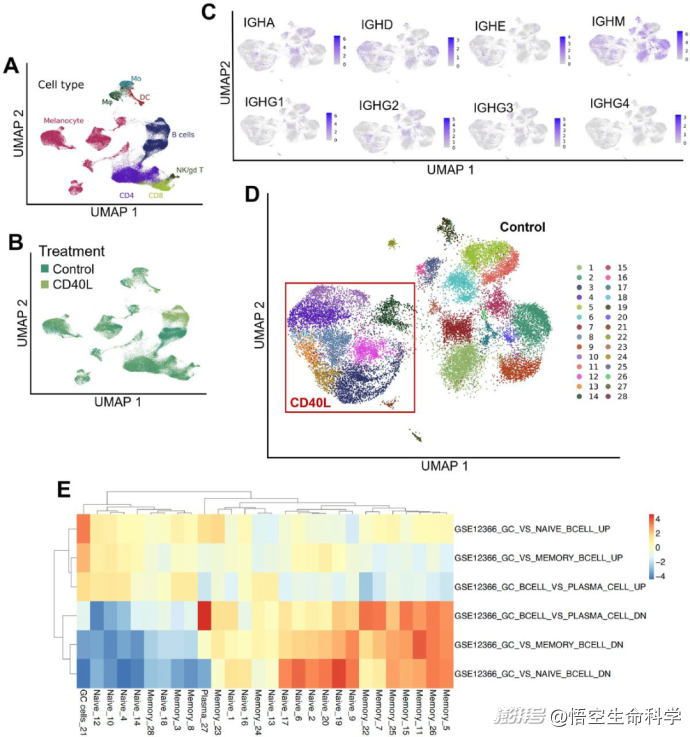
(A)肿瘤消化中识别的不同细胞群的UMAP投影。(B)基于培养条件(CD40L与对照)的肿瘤消化的UMAP投影。(C)B细胞的UMAP投影,显示IgA、IgD、IgE、IgG1、IgG2、IgG3、IgG4和IgM抗体/BCR同型的表达。(D)B细胞的UMAP投影显示由Seurat算法识别的子聚类。与CD40L处理样品对应的集群用红方表示。(E)将B细胞集群与之前描述的基因集与原始、记忆、胚胎中心(GC)和浆细胞相对应的基因集交叉引用
具体来说,B细胞在CD40L刺激下扮演了两重角色:
增强T细胞扩增的局部环境:B细胞被CD40L激活后,大量上调共刺激分子(如CD58、CD83),这些分子与T细胞表面受体结合,为T细胞提供必需的“第二信号”,促进其增殖与存活。
同时,B细胞释放出一系列趋化因子(如CCL17、CCL22),进一步吸引并聚集潜在的抗肿瘤T细胞。
提升TIL细胞产品的质量:研究显示,经过B细胞激活辅助扩增的TIL细胞,具有更多年轻表型(CD39- CD69-),这类T细胞被证明在体内更具持久性和抗肿瘤活性。
更重要的是,TCR测序发现,新抗原特异性克隆频次明显增加,意味着治疗后能更精准识别和杀伤肿瘤细胞。
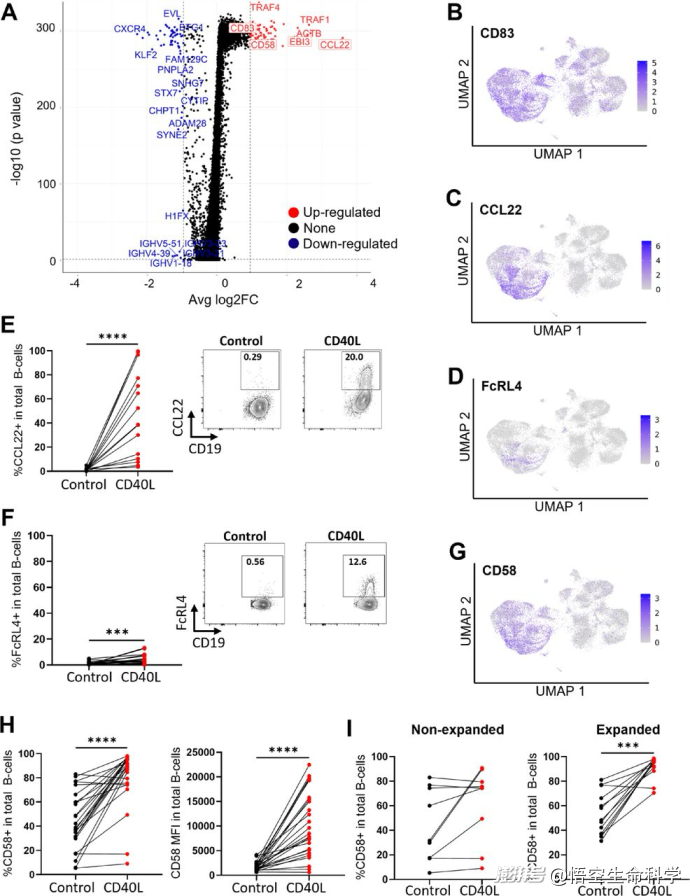
CD40L诱导黑色素瘤浸润B细胞的基因表达变化。黑色素瘤消化液在标准TIL(对照)或CD40L补充培养基中培养48小时(n=14个样本,7名患者)
这一切意味着什么?
不仅TIL扩增成功率翻倍,治疗所用细胞的质量也更好,治疗后的持久反应率、完全缓解率有望进一步提升。
对于过去TIL扩增失败、无缘接受治疗的患者,这一技术改进也可能打破门槛,让更多人受益。
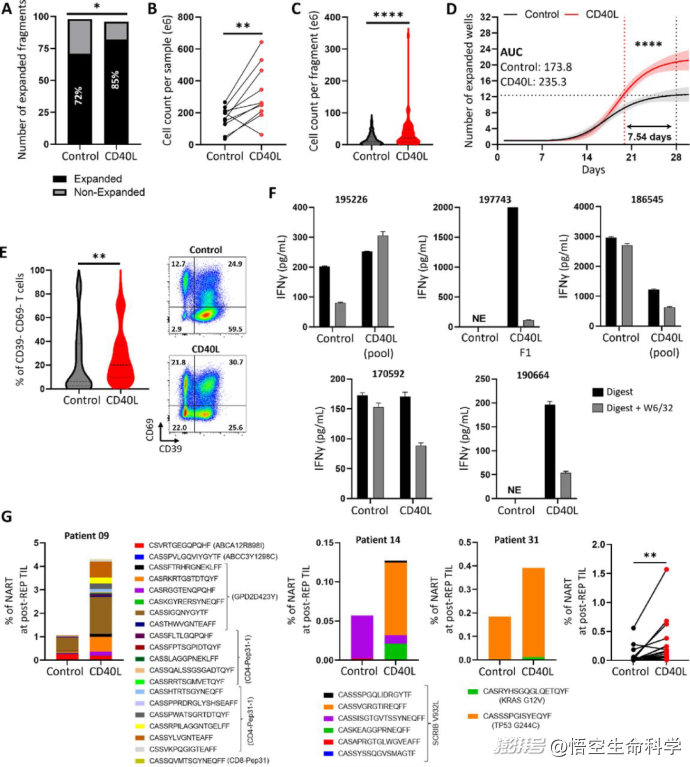
CD40L增强了NSCLC TIL的扩张,并增加了新抗原反应性T细胞的频率
05 未来免疫疗法:不止是强化单兵,而是激活全军
在免疫治疗的战场上,单打独斗的时代正在过去。
哈佛医学院附属达纳-法伯癌症研究院的这项研究提醒我们,真正高效持久的抗癌力量,来自细胞与细胞之间的协作与动员。
B细胞不再是边缘角色,而是TIL扩增成功、疗效增强的关键助力。
通过精准激活B细胞这条新通路,科学家不仅提升了治疗成功率,更重新绘制了免疫疗法的战略版图。
未来,当更多类似的微创新被不断发现与应用,癌症免疫治疗或许将迎来一场真正意义上的质变——
不只是延长生命,更是赋予更多患者彻底逆转命运的可能。
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




