- +1
当“快效”遭遇“耐药”,应该如何选择?玛巴洛沙韦 Vs 奥司他韦
玛巴洛沙韦(速福达),因“全病程仅需一次服药”的依从性优势,成为很多流感吃药困难户的首选。
不过,它“相对容易诱发流感病毒耐药突变”的特点,也一直引起很多医生和家长的担忧。
2023年4月,在本公众号首篇相关文章《关于速福达的12个答疑》里就讨论过这个问题(第4个答疑)。
玛巴洛沙韦诱导的流感病毒耐药突变率确实高于奥司他韦,但众多研究发现:服用玛巴洛沙韦的患者往往退热更快,其整体疗效并不逊色于奥司他韦——乍一看,像是个“悖论”。
接下来,我就来解释这一现象背后的机制。
01
作用机制差异
简单对比这两个药的抗病毒机制,就能理解其中缘由了。
玛巴洛沙韦——源头阻断。靶点是Cap依赖性核酸内切酶。
作用:切断源头(上游),直接阻断流感病毒复制起始。
结果:病毒载量断崖式下跌 → 病毒引起的免疫反应迅速平息 → 体温快速下降
奥司他韦——封锁出口。靶点是神经氨酸酶 (NA)。
作用:阻止病毒从被感染的细胞中释放(下游),但无法阻止细胞内病毒复制。此时,细胞内病毒还在复制,仅仅是被“困在”细胞里。
结果:病毒载量下降相对缓慢 → 病毒引起的免疫反应慢慢平息 → 退热相对偏慢。
也许有读者要问:被奥司他韦“困在”细胞里的流感病毒将会面临怎样的结局?今天不展开,有空再聊。
02
退热时间差异
作用机制的差异,导致了用药物后病毒动力学的显著不同:治疗开始后24小时内,玛巴洛沙韦可使病毒载量降低约84%,奥司他韦降低约56%。
流感患者反复高热,主要由病毒诱导的细胞因子驱动。而流感病毒载量在第1天就被玛巴洛沙韦“断崖式”压制,病毒引发的炎症反应随之消退,于是退热较快——通常比奥司他韦缩短12~24小时左右。
这意味着,流感患者如果在出现流感样症状的48小时内服用玛巴洛沙韦,那么,往往会在服药后1~2天内退烧;如果服用奥司他韦,则需2~3天 。



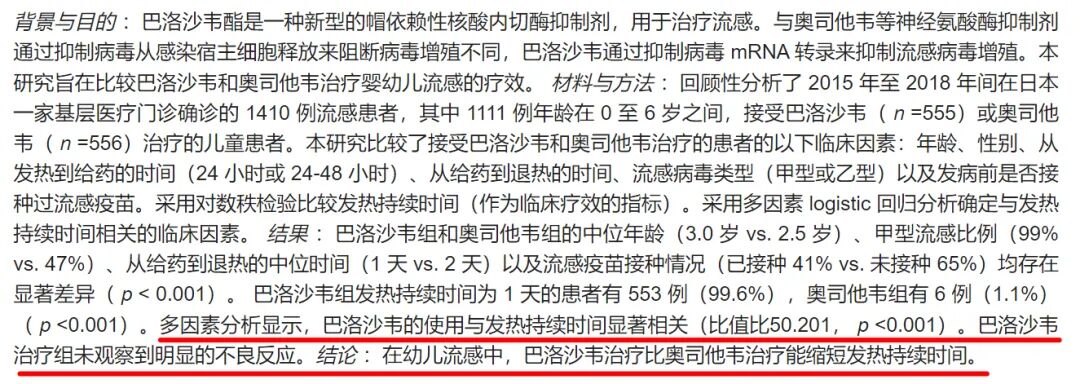
两种药物的安全性相似,不良事件发生率无显著差别,但玛巴洛沙韦的胃肠道不良反应(恶心、呕吐)发生率更低。
许多临床研究观察到这些现象,结果得到重复验证,不再一一列举。
03
阻止病毒播散
流感患者的病毒脱落会引起病毒播散。
与奥司他韦相比,玛巴洛沙韦治疗的患者,病毒脱落停止时间提前48~144小时,这意味着病毒播散也随之减少。
2025年4月,《新英格兰医学杂志》发表的一篇研究显示:家庭内的首个流感患者确诊流感后,如果立即服用玛巴洛沙韦,那么家庭接触者感染流感的风险降低了29%~32%


2024年5月,日本一对照研究发现:在预防家庭内流感病毒传播方面,玛巴洛沙韦优于奥司他韦。


服用一次就能快速抑制病毒复制,退热快,减少传播,不良反应更少,看似完美的玛巴洛沙韦却有一个隐患——容易诱导流感病毒出现耐药突变。
04
耐药机制差异
玛巴洛沙韦耐药机制
玛巴洛沙韦的作用靶点是病毒PA蛋白的帽依赖核酸内切酶。
其耐药核心在于PA基因I38位点的单点突变(最常见 I38T,其次 I38M、I38F)。I38位于酶活性中心的金属离子结合口袋,突变会降低药物与PA的结合亲和力,使内切酶抑制失效,病毒复制恢复。
耐药特点:
1、仅需单一核苷酸突变,即可导致敏感性下降。所以,容易发生耐药。
2、儿童中更易出现耐药。
3、虽然玛巴洛沙韦诱导的耐药流感病毒检出率相对偏高,但携带这些突变的病毒复制能力差,传播力弱。
奥司他韦耐药机制
奥司他韦结合病毒表面神经氨酸酶(NA),阻断宿主细胞内新生病毒颗粒释放。
其耐药主要由NA基因结构性突变导致,如 H275Y(H1N1最典型)、R292K 和 E119V(H3N2)。这些突变会改变NA活性位点和空间构象,使药物难以有效进入酶的结合口袋,导致药效下降。
耐药特点:
1、需要多个氨基酸改变,才能导致敏感性下降。因此临床耐药率低于玛巴洛沙韦。
2、奥司他韦诱导的流感耐药病毒株传播力,稍强于玛巴洛沙韦诱导的耐药毒株。
05
时间差
服用玛巴洛沙韦的患者,如果体内出现药物引起的耐药毒株,那么时间线大概如下:
Day 1(给药日):药物发挥作用,野生型病毒载量迅速下降。
何为“野生型病毒”?
野生型病毒,是病毒学的常用术语,指在自然界中存在、未经人工改造或未发生重大突变的病毒原形态。
野生型病毒对应的是“突变毒株”。
突变,既可能是自然突变,或是两种病毒在宿主体内重组,也可能是药物、免疫系统的压力下筛选出来的突变。
Day 2–3(症状改善期):野生型病毒基本被清除,绝大多数患儿在服药的24-48小时退热,临床症状恢复明显。
Day 3–5(耐药筛选期):在药物选择压力下,少量携带I38T突变的病毒株开始复制。
你看,玛巴洛沙韦诱导耐药突变的形成和扩增需要时间,而此时它已完成了“退热”的目标。
尽管在研究发现患儿体内出现耐药毒株的病毒学反弹,但临床症状反弹极少见。大多数耐药患儿的恢复过程与未耐药者基本一致,少数仅延长了症状恢复时间。
为何体内出现耐药病毒,却很少出现“症状反弹”?
06
适应性免疫
这是因为在感染进入第4~5天后,人体的“第二道防线”——适应性免疫(又称获得性免疫)开始接力清理病毒。
适应性免疫维系人类生存的核心免疫机制,其由两部分组成:抗体(B 细胞)和细胞毒性T细胞(CTL)。
抗体负责“中和”病毒:识别并黏附其表面结构,阻断其进入细胞,并促进清除。大多数人在感染的第3~5天,抗体开始明显升高。
CTL则是“定点清除的杀伤部队”,专门识别并摧毁已被病毒感染的细胞,相当于直接摧毁病毒复制的“生产车间”。CTL通常在感染的第4~5天后逐渐活跃。
因此,当药物效应减弱,甚至体内出现耐药突变株时,患者体内逐步产生的抗体和CTL可以接力,继续压制病毒复制。
适应性免疫是感染后期维持病情稳定、清除耐药病毒的关键。
与人体的“第一道防线”——与生俱来的先天性免疫(又称固有免疫,如皮肤屏障、白细胞吞噬)不同,适应性免疫需要人体在后天接触特定病原体(如,病毒、细菌)或接种疫苗后,通过“学习”与“记忆”逐步建立。
正因为具备这套机制,对免疫功能正常的大多数人而言,流感也是一种自限性疾病——在没有抗病毒药的年代,人类就是依靠自身免疫系统战胜流感的。不过,接种流感疫苗和及时抗病毒治疗可以显著减少并发症、重症和死亡风险。
另外,至今许多呼吸道病毒也无特效药,人体仍然需要依靠适应性免疫对抗感染,逐渐康复。
综上,玛巴洛沙韦的“退热快”与其“较高的诱导耐药率”看似矛盾,实则发生在不同的时间点。正是这段时间差,让患者的适应性免疫得以发挥作用,最终完成对耐药病毒的清除。
07
耐药毒株传播力
玛巴洛沙韦治疗过程中较易出现耐药突变的现象,早就引起流感监控部门和医生的关注。
个体层面,流感患儿服用玛巴洛沙韦后出现的耐药毒株相对常见。临床研究显示,PA I38X替换在儿童中的发生率达19~23%,以2~4岁、H3N2感染者较为突出。
然而,目前仅记录到耐药病毒引起的零星家庭传播事件,并未造成明显的社区传播。
基础研究显示:
雪貂实验(研究流感传播的经典模型)显示耐药株具备接触传播和部分空气传播的能力,但传播效率不及野生型:耐药毒株复制效率较低,当耐药病毒和野生型病毒混在一起传播时,耐药病毒的比例逐渐下降,甚至消失。
另有研究发现,某些耐药突变(如 A(H3N2) 的 I38F)流感病毒无法通过空气(气溶胶)传播。这意味着通过呼吸道远距离传染他人的能力大打折扣。
是否存在社会层面耐玛巴洛沙韦流感毒株的流行?这需要关注主要国际机构和各国疾控部门的监测数据。
WHO的全球监测数据:2018~ 2025年间季节性流感病毒对玛巴洛沙韦的耐药突变总体维持在极低水平。A(H3N2) 的敏感性降低比例为0.3~0.7%,A(H1N1)pdm09为0~0.6%。
中国国家流感中心每周发布的流感周报数据:所有A(H1N1)pdm09、A(H3N2)亚型和B型流感病毒毒株均对聚合酶抑制剂敏感,意味着中国大陆迄今没有检测到对玛巴洛沙韦的耐药毒株。
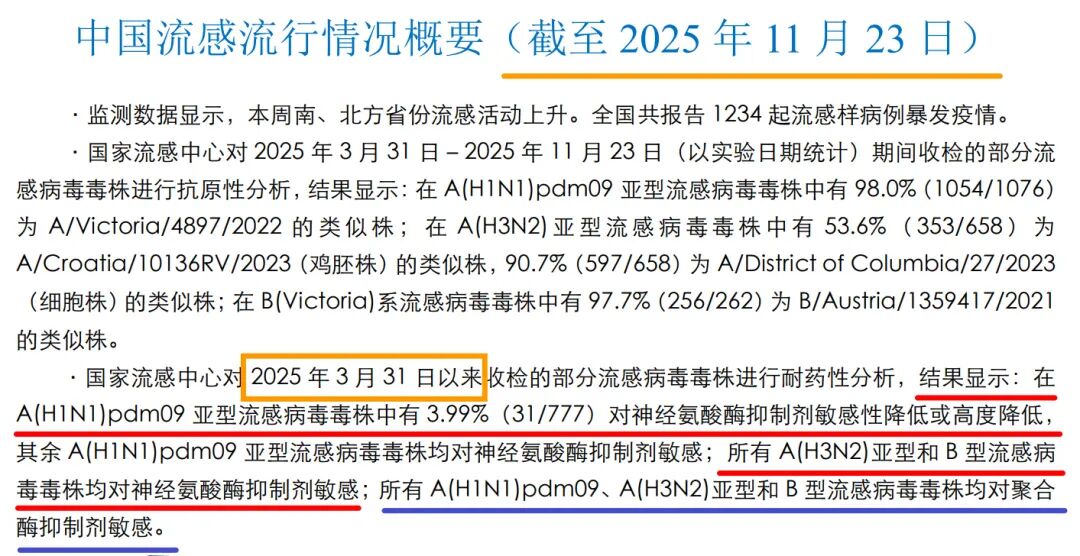
相比他国,日本流感患者中玛巴洛沙韦处方量最高,所以日本的耐药监测数据最值得关注。
日本国家传染病研究所的监测数据显示,从2019/2020到2024/2025流感季,未治疗患者中流感病毒对玛巴洛沙韦的耐药率保持在0.90%以下。更早的2018/2019季节,为0.97%。
2023/2024流感季,仅报告一个A(H1N1)pdm09耐药病例,未见社区集群或进一步传播。
美国2024/2025流行季,仅报告1株耐药H1N1pdm09病毒。
关于耐药话题,我曾写过文章分析,《玛巴洛沙韦在中国处于耐药性“空白期”?奥司他韦耐药率真的在上升?》,有兴趣者可点击了解。
综合来看,虽然文献中频繁讨论玛巴洛沙韦的耐药问题,但迄今的全球监测与临床研究显示:玛巴洛沙韦相关的耐药流感病毒,在社区层面的传播极为有限,检出率长期处于极低稳定水平,未出现上升趋势。
08
总 结
从作用机制 → 临床转归 → 耐药机制 → 适应性免疫 → 耐药毒株传播力,一直看下来,应该很费神吧。我来总结一下:
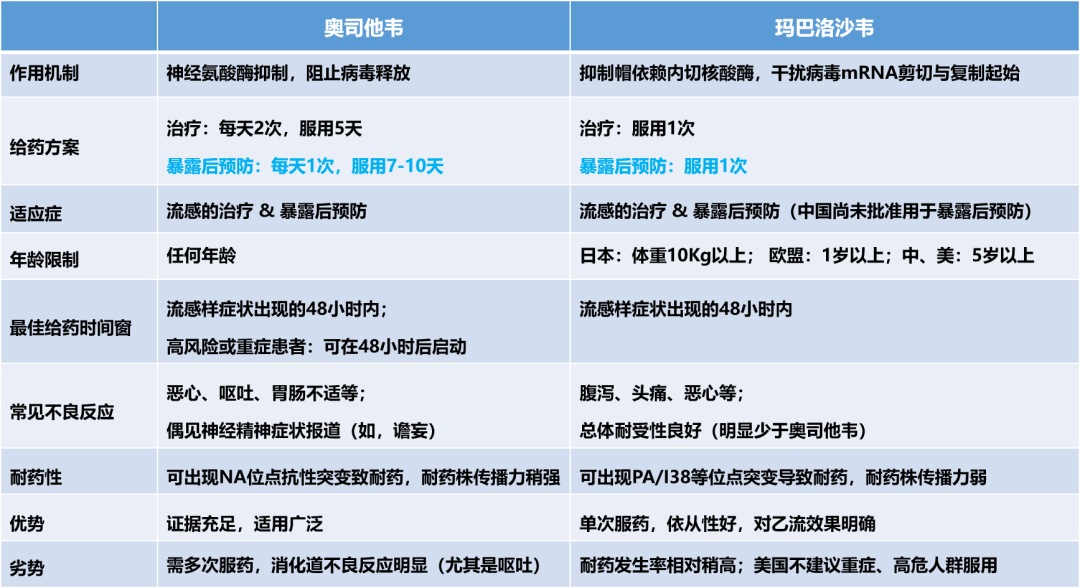
相比奥司他韦,玛巴洛沙韦的优势是:单次服药、依从性好、病毒载量下降更快、体温更早恢复正常、不良反应小、可阻止家庭传播,但其耐药风险不可忽略,我们需要密切观察用药者的症状转归。
免疫功能正常的适龄患者,如果平时服药困难,玛巴洛沙韦是不错的选择。
免疫功能受损的人群,或其他重症高风险患者,考虑到耐药风险以及自身适应性免疫不健全,奥司他韦则是更稳妥的选择。
参考来源
https://pmc.ncbi.nlm.nih.gov/articles/PMC11993522/
https://academic.oup.com/cid/article/71/4/971/5571979?login=false
https://pmc.ncbi.nlm.nih.gov/articles/PMC7360097/
https://www.nejm.org/doi/full/10.1056/NEJMoa1716197
https://pubmed.ncbi.nlm.nih.gov/32526195/
https://pmc.ncbi.nlm.nih.gov/articles/PMC7360097/
https://d-nb.info/1369324405/34
https://journals.plos.o
rg/plosone/article?id=10.1371%2Fjournal.pone.0326777
https://pmc.ncbi.nlm.nih.gov/articles/PMC9012239/
https://www.nejm.org/doi/full/10.1056/NEJMoa2413156
https://pubmed.ncbi.nlm.nih.gov/38706384/
https://link.springer.com/article/10.1007/s40121-025-01203-5
https://wwwnc.cdc.gov/eid/article/31/5/24-1123_article
https://www.nature.com/articles/s41564-019-0609-0
https://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1009527
https://www.isrv.global/wp-content/uploads/2025/06/nisn_options_report_dec2010.pdf
https://www.pnas.org/content/117/15/8593.short
声明:本文作者和奥司他韦和玛巴洛沙韦生产商、经销商无任何利益关系。

本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




