- +1
Science子刊:王荣福团队开发新型CAR-T细胞,更安全、更有效、更持久
撰文丨王聪
编辑丨王多鱼
排版丨水成文
CAR-T 细胞疗法在血液类癌症中已产生令人瞩目的临床疗效,证明了这种合成 T 细胞信号受体是产生治疗性抗肿瘤免疫的一种有前景的方法。尽管 CAR-T 细胞疗法在血液类癌症中取得了巨大成功,但约 30%-50% 的患者在 CAR-T 细胞治疗后 1 年会出现疾病复发。此外,CAR-T 细胞疗法常引起严重毒性,主要包括由血清中高浓度炎症细胞因子触发的细胞因子释放综合征和神经毒性。
鉴于 T 细胞的持久性与 CAR-T 细胞疗法的疗效和长期癌症消退密切相关,开发改善或延长 T 细胞持久性的策略,对于 T 细胞免疫疗法至关重要。T 细胞的持久性依赖于几个关键因素——包括干细胞样记忆 T 细胞的百分比、T 细胞的体内增殖能力以及对抗 T 细胞耗竭的能力。
2025 年 12 月 10 日,南加州大学王荣福教授团队(柳鑫博士为论文第一作者)在 Science 子刊 Science Translational Medicine 上发表了题为:ZAP327 signaling domain–driven chimeric antigen receptor generates robust and long-term antitumor immunity in mouse models 的研究论文。
该研究开发了一种 ZAP327 信号结构域驱动的新型 CAR 结构,基于这种 CAR 结构的 CAR-T 细胞疗法显著降低了细胞因子释放、减少了 T 细胞耗竭,在小鼠模型中产生强大且持久的抗肿瘤免疫反应。这代表了 CAR-T 细胞疗法的有前景的改进方向。

当前的 CAR 结构通常包含四个主要组成部分:一个抗原结合域、一个铰链区和跨膜结构域、一个胞内共刺激结构域、以及一个 T 细胞信号转导结构域。
CAR 的抗肿瘤免疫活性可通过其信号转导结构域进行调控,这些结构域包括共刺激结构域和核心的 T 细胞受体信号转导结构域。在源自不同蛋白(例如 CD28、4-1BB、OX40、CD40、ICOS 和 CD27)的众多共刺激信号结构域中,CD28 和 4-1BB 是 CAR 结构中最常用的两种。尽管多种含有 CD28 和 4-1BB 的 CAR-T 细胞产品具有治疗效果,但它们在细胞增殖、杀伤能力、代谢状态和持久性方面表现出显著差异。
最近的几项研究表明,通过筛选源自其他信号分子的信号结构域库,可以识别出先前未知的共刺激组合(用以替换 CD28 和/或 4-1BB 信号结构域),从而能够生成具有更强细胞毒性作用和更长 T 细胞持久性的下一代 CAR 结构。
在这项新研究中,研究团队报道了构建具有 ZAP70 来源信号结构域(ZAP70 激酶域的截短形式——ZAP327)的 CAR 结构,该结构域通过增强体内 T 细胞持久性来提升治疗性抗肿瘤活性。
与传统 CAR-T 细胞相比,ZAP327 驱动的 CAR-T 细胞减少了细胞因子释放和 T 细胞耗竭标志物的表达,但保持相似或更好的对肿瘤细胞的细胞溶解活性。
ZAP327 CAR 结构中的共刺激结构域是必需的,它们提供了跨膜结构域和 ZAP327 激酶结构域之间的间隔,以实现最佳的激酶结构折叠和功能以及共刺激信号传导。此外,ZAP327 驱动的 CAR-T 细胞在治疗性抗肿瘤免疫方面优于传统及几种近期改进的 CAR-T 细胞,特别是在抗原低表达肿瘤模型中。在小鼠实验中,其显著延长了生存期,并在实体瘤模型中表现出色。这不仅为 CAR-T 细胞治疗后血液类癌症的复发提供解决方案,更为实体瘤的 CAR-T 细胞疗法铺平了道路。
从机制上来说,研究团队发现,ZAP327 结构域能够调低 TCR 信号,增加干细胞样记忆 T 细胞(Tscm)库,并通过利用氧化磷酸化途径表现出与记忆 T 细胞相关的代谢特征。
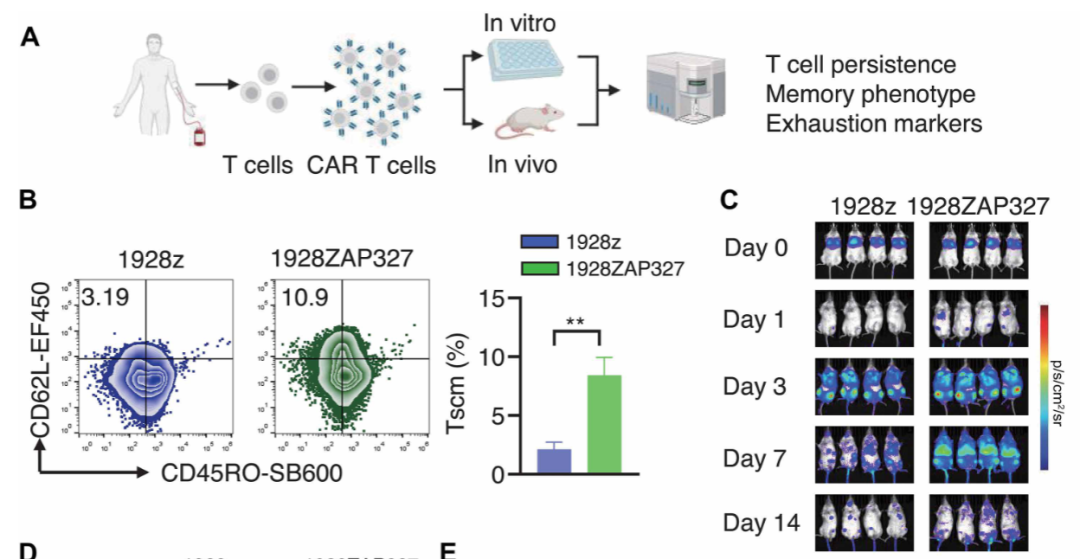
这些结果突显了 ZAP327 驱动的 CAR-T 细胞的治疗潜力,可克服当前 CAR-T 细胞疗法的局限性,并增强抗肿瘤 T 细胞反应在实体瘤中的效力和持久性。
论文链接:
https://www.science.org/doi/10.1126/scitranslmed.adz0529
原标题:《Science子刊:王荣福团队开发新型CAR-T细胞,更安全、更有效、更持久》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




