- +1
【科技前沿】Adv Sci综述 | 王红艳团队总结单细胞视角下肺部感染中巨噬细胞亚群的研究进展
巨噬细胞是肺部感染中关键的先天免疫效应细胞,广泛参与病原体识别、炎症调控及组织修复过程。然而,长期以来,巨噬细胞被简单分为促炎与抑炎两类,这种二元模式逐渐显露局限,难以解释其在真实感染过程中呈现出的高度异质性与动态可塑性。近年来,单细胞测序、空间组学和谱系追踪技术的发展,为解析巨噬细胞在不同感染阶段、不同空间微环境中的状态变化提供了前所未有的分辨率。随着细胞注释类别急剧增加,目前研究高度依赖个别基因标记进行定义,命名体系分散、标准不统一、跨研究比较困难,也在一定程度上阻碍了生物学意义的整合。基于不断累积的单细胞证据,一个更贴近生理过程、以功能状态为核心的巨噬细胞分类框架逐渐形成,并推动研究从“静态标签式分类”向“理解动态连续谱系变化”转变。
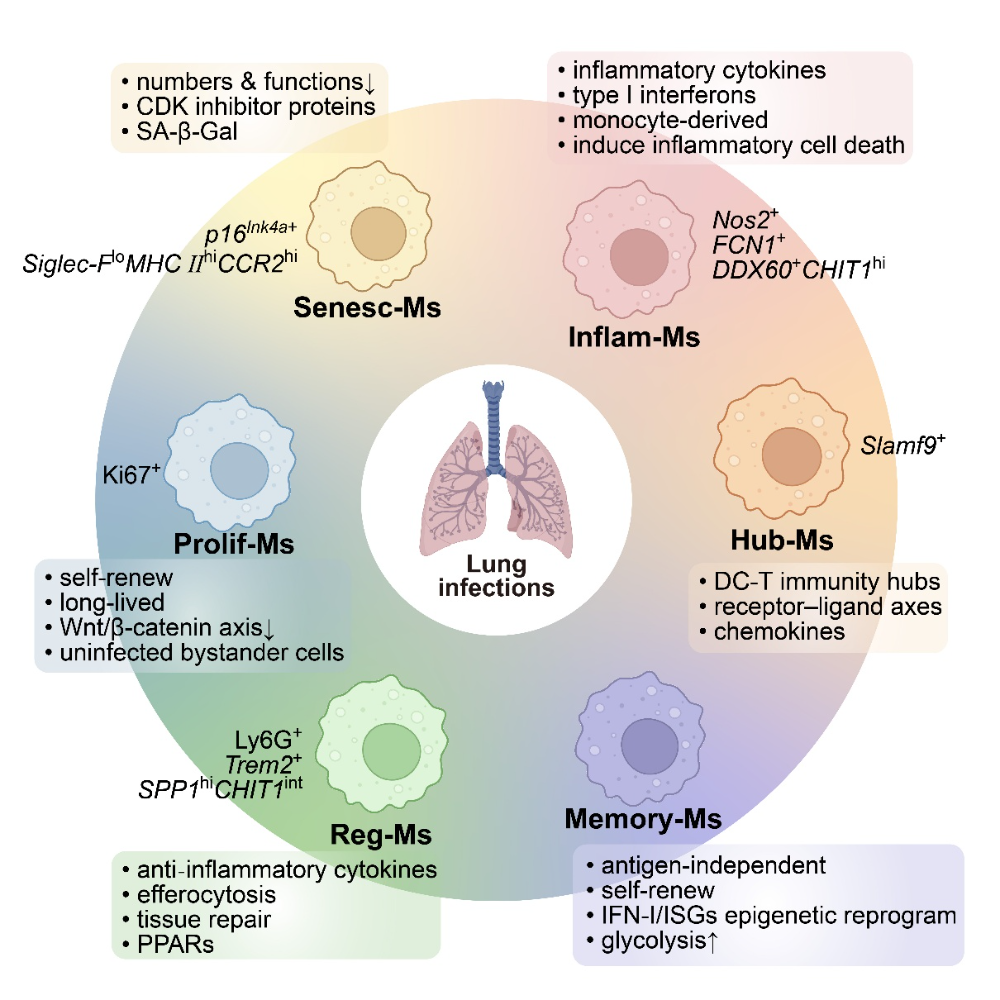
图1. 肺部感染过程中巨噬细胞亚群的动态可塑性与分类框架
中国科学院分子细胞科学卓越创新中心王红艳团队近期受邀在Advanced Science 发表综述文章Single-Cell Insights Into Macrophage Subtypes in Pulmonary Infections,系统整合了近年来单细胞研究关于肺感染中巨噬细胞的关键发现,并提出一个更加贴近生理过程的功能性理解框架。文章通过比较病毒感染(如 SARS-CoV-2 与流感)、细菌感染、以及慢性感染或损伤性炎症模型,梳理出六类功能倾向明确的巨噬细胞亚型,包括以强烈炎症应答为特征的炎症因子富集型 (Inflammatory cytokine-enriched macrophages)、在特定微环境承担免疫通讯与细胞招募的免疫枢纽型 (Immunity hubs-associated macrophages)、负责免疫调节与组织修复的免疫调节型 (Immune regulatory macrophages)、在感染和修复过程中维持巨噬细胞数量的增殖型 (Proliferating macrophages)、具备训练免疫特征的记忆型 (Memory macrophages),以及可能在慢性炎症与年龄相关损伤中累积的衰老型 (Senescent macrophages)。巨噬细胞具有高度动态性和可塑性,在感染过程中能持续适应微环境的变化。这些巨噬细胞亚群并非严格互斥的“离散群体”,而是代表了连续激活谱系中具有功能偏向性的“状态节点”。

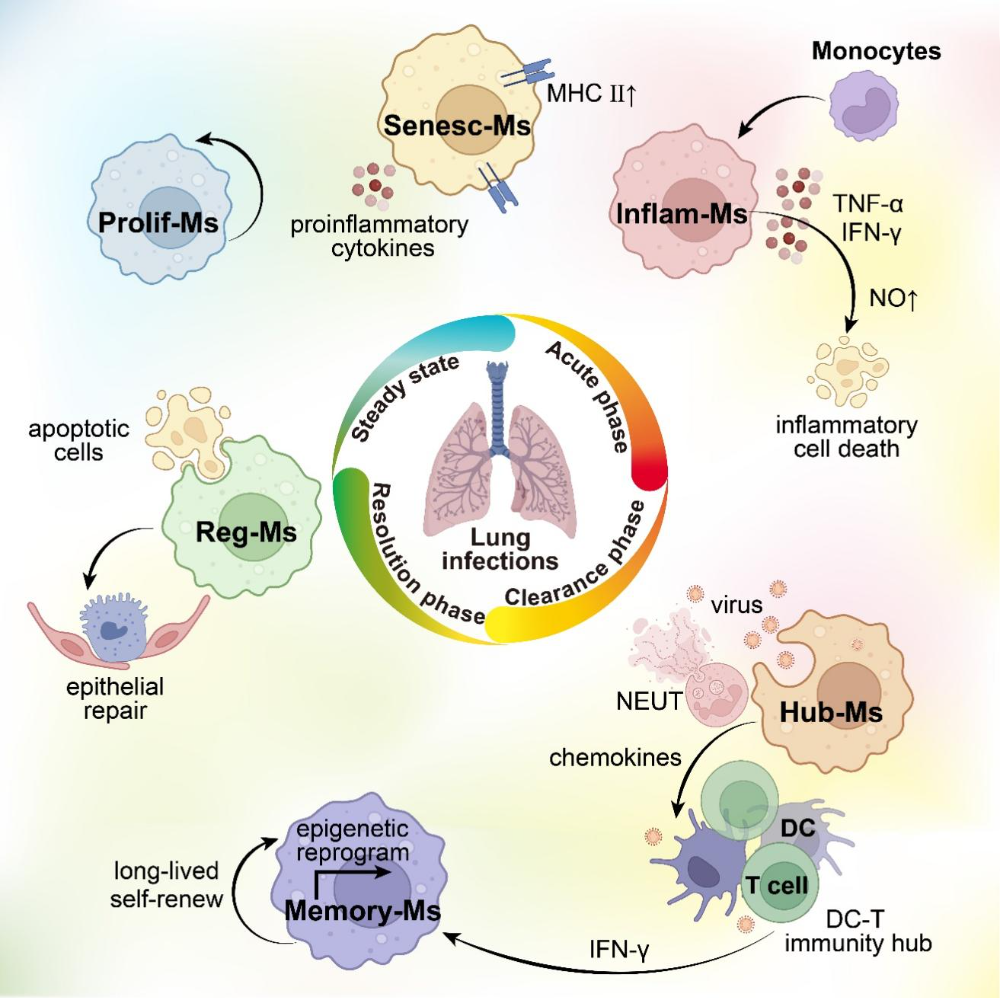
图2. 肺部感染不同阶段中巨噬细胞亚群的功能角色与动态变化
巨噬细胞功能状态受到病原类型、宿主免疫背景、代谢微环境以及空间定位等因素共同调控。在肺部感染的早期阶段,I型干扰素与TNF相关通路驱动炎症因子富集型巨噬细胞 (Inflam-Ms) 迅速激活,承担病原感应与初始免疫反应。尽管这一阶段对抑制病原扩增至关重要,但炎症是一把“双刃剑”,持续或过度激活会引发免疫级联放大,促进炎症扩散。多项冠状病毒病 (COVID-19) 患者单细胞分析显示,炎症因子富集型巨噬细胞过量积累与急性呼吸功能障碍、组织损伤和细胞因子风暴密切相关,这也提示其保护与损伤并存的特性。
随着感染从急性应答阶段过渡到病原清除阶段,免疫细胞之间的互作显现出更组织化的特征,其中免疫枢纽型巨噬细胞 (Hub-Ms) 处于关键位置。该亚群通常富集于由树突状细胞 (DC) 与T细胞构建的免疫微环境 (DC–T immunity hubs),这一跨细胞通讯枢纽结构是近年来通过单细胞与空间组学技术识别的重要免疫组织特征,介导免疫细胞聚集与效应应答的放大。在新冠病毒 (SARS-CoV-2) 感染中,免疫枢纽型巨噬细胞中具有代表性的Slamf9+亚群表现出显著扩增趋势,并与病毒清除密切相关。随着感染逐步控制,该亚群出现向两类功能状态分化的趋势:一部分分化为Trem2+免疫调节型巨噬细胞 (Reg-Ms),承担凋亡细胞清除、炎症消退与组织修复相关功能;另一部分则分化为Fbp1+增殖型巨噬细胞 (Prolif-Ms),通过维持细胞数量与更新能力,参与组织重建与微环境稳态重塑。
在炎症消退阶段,免疫调节型巨噬细胞 (Reg-Ms) 通过多层次机制协调炎症消退与组织修复。免疫调节型巨噬细胞识别并清除凋亡细胞,同时在抑炎细胞因子等信号协同下,启动特征性的转录与代谢重编程,上调修复相关基因、促进胶原合成和细胞外基质重塑。在肺泡微环境中,Ly6G+免疫调节型巨噬细胞通过分泌骨桥蛋白 (OPN),促进肺泡II型上皮细胞 (AT2) 向AT1细胞分化,支持肺泡重建和功能恢复。与此同时,一部分巨噬细胞在经历表观遗传与代谢层面的深度重塑后进入具有“训练免疫”特征的记忆型状态 (Memory-Ms)。与抗原特异性的适应性免疫记忆不同,记忆型巨噬细胞形成的免疫“记忆”具有抗原非依赖性 (antigen-independent) 与异源免疫性 (heterologous protection)。例如,既往新冠病毒感染可能减轻后续流感感染的严重程度;卡介苗接种可在肺部诱导记忆型肺泡巨噬细胞,不仅能够预防目标病原体,也可降低婴幼儿及老年人的全因死亡率及呼吸道感染风险,提示训练免疫能够为肺组织提供更快速的天然免疫动员。这种能力源于干扰素相关区域染色质可及性增强,代谢状态改变以及长期自我更新能力,使记忆型巨噬细胞即便在缺乏适应性免疫细胞参与的情况下仍能维持。然而,训练免疫并非始终显示出更强的反应性——在败血症等背景下,记忆型巨噬细胞可能进入免疫抑制或耐受模式。
随着感染接近尾声,巨噬细胞并未完全回归静息,在某些条件下会呈现出另一类功能特征,即衰老型巨噬细胞 (Senesc-Ms)。这一亚群多见于慢性炎症、组织慢性损伤或与年龄相关的肺部微环境变化。与具有可逆激活特征的其他亚群不同,衰老型巨噬细胞显示出增殖潜能下降、转录调控紊乱以及持续性促炎信号表达等特征,提示其在局部免疫调节中的作用既非完全抑制,也并非经典炎症应答,而更偏向一种难以关闭的炎症状态。值得注意的是,尽管 p16INK4a 或 SA-β-gal 等指标常被用于检测细胞衰老,但这些标志在巨噬细胞中具有环境依赖性和潜在可逆性。因此,在界定巨噬细胞衰老时,需谨慎解读单一指标,应结合其增殖停滞、功能紊乱及分泌表型等多维度证据进行综合判断。衰老型巨噬细胞的来源、稳定性及可逆性仍需进一步研究。
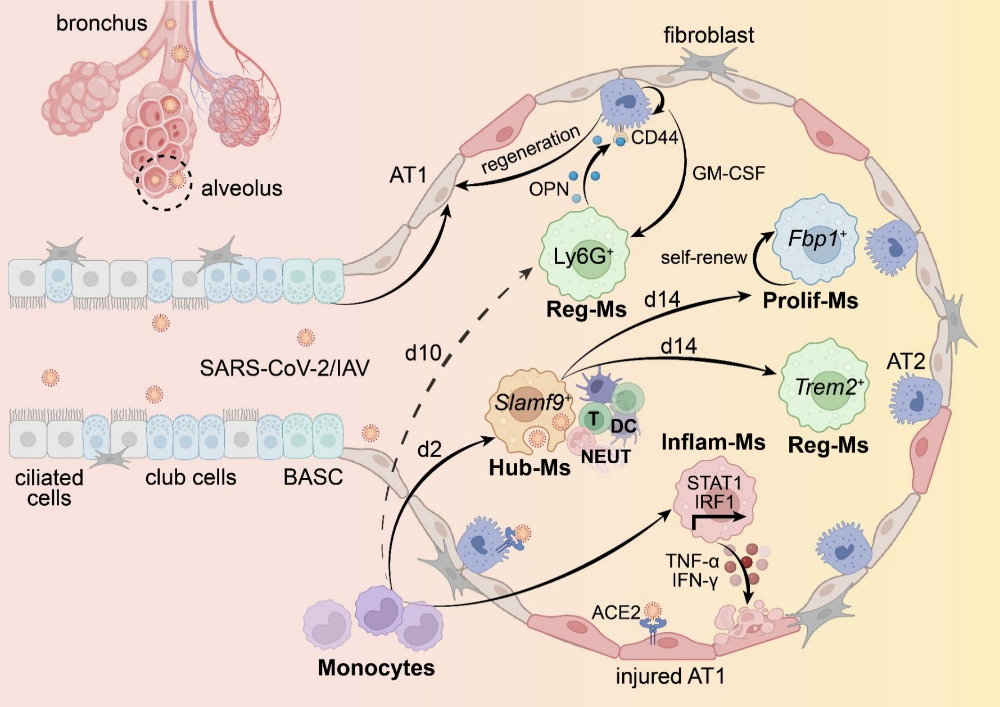
图3. SARS-CoV-2或流感病毒感染中肺泡微环境内巨噬细胞亚群的动态变化
综上,单细胞组学技术正在重塑我们对肺部感染后巨噬细胞谱系的理解。文章提出的功能性理解框架揭示,巨噬细胞在炎症启动、免疫协调、组织修复及长期稳态过程中动态转换,形成具有不同功能偏向的细胞状态节点。这一认识不仅为解析不同病原体、疾病阶段和宿主因素下的免疫差异提供了更接近生理现实的解释,也为未来开发针对特定巨噬细胞状态的精准干预策略奠定了理论基础。随着空间组学、多组学整合及功能验证的推进,靶向巨噬细胞可塑性的治疗策略或将逐渐成为可能。
中国科学院大学杭州高等研究院硕士研究生林兆亨、博士后郑雨骁、硕士研究生钟雨为本文共同第一作者,中国科学院分子细胞科学卓越创新中心王红艳研究员为本文通讯作者。
原文链接:https://doi.org/10.1002/advs.202510758
文章来源于:BioArt
相关推荐:
【科技前沿】Nat Cell Biol | 自噬调节线粒体不对称遗传并控制早期CD8⁺ T细胞命运
【科技前沿】Nature | 线粒体靶向序列在应激信号传递中的直接作用
中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】Adv Sci综述 | 王红艳团队总结单细胞视角下肺部感染中巨噬细胞亚群的研究进展》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




