- +1
脑声常谈|防御环路:威胁反应中的脑-体回路

大多数动物长期生活在捕食者的持续威胁之下,而捕食行为已成为塑造动物行为的主要选择压力。然而,针对捕食威胁的防御反应需要与其他适应性行为(如觅食、交配和感染后恢复)相平衡。这种在行为学相关情境下的行为平衡,需要大脑与身体通过复杂的相互作用,充分整合内部和外部信号。尽管存在这种复杂性,以往研究往往认为防御行为完全由大脑介导:大脑通过感知外部环境获取与威胁相关的信息并对其进行处理。但越来越多的证据表明,内分泌系统、免疫系统、胃肠道系统和生殖系统在调节威胁相关行为反应中发挥着重要作用。
引言
大多数动物长期处于被捕食的威胁之下,而捕食者本身也常是更高阶捕食者的猎物。因此,自然选择塑造了多种先天、自动激活的防御行为,以在危险中快速规避伤害或死亡。
1970年,Bolles提出突破性观点:捕食威胁会触发特定的先天防御反应(如僵直、逃跑、假死),而非依赖后天学习的任意行为。后者在致命威胁下往往来不及习得。这一思想随后由Fanselow等人发展为“捕食逼近连续体”(predatory imminence continuum)模型:动物根据捕食者在时空上的逼近程度,选择最有效的防御策略。从风险评估、回避,到僵直、逃跑、防御性攻击乃至假死,这些行为已在从昆虫到人类的多个物种中被系统刻画。
重要的是,某些压力可扭曲该连续体,导致防御反应侵入本应执行其他适应性行为(如社交、进食)的情境,这正是焦虑症、PTSD等恐惧相关障碍的核心特征。
传统观点将防御行为视为纯脑内过程的输出,但越来越多证据表明,外周系统(如免疫、内分泌、生殖、消化系统及肠道菌群)通过调节防御反应的激活阈值与强度,深刻影响行为选择。例如,感染或饥饿状态下,促炎因子或代谢信号可增强警觉;性激素亦能调制对威胁的反应。
长期的捕食压力不仅塑造了大脑中的防御回路,也可能优化了外周器官与神经系统的整合机制。防御行为必须与觅食、繁殖、疾病恢复等需求动态平衡,而这依赖于大脑与身体之间的双向信号整合。
在现代社会,慢性压力、不良饮食等因素可扰乱这种整合如引发炎症、菌群失调或代谢紊乱,进而非适应性地降低防御阈值,增加神经精神疾病风险。因此,全面理解防御行为,必须将其视为脑–体协同调控的系统性过程。
威胁逼近连续体三个阶段中的防御反应及其潜在的脑神经回路
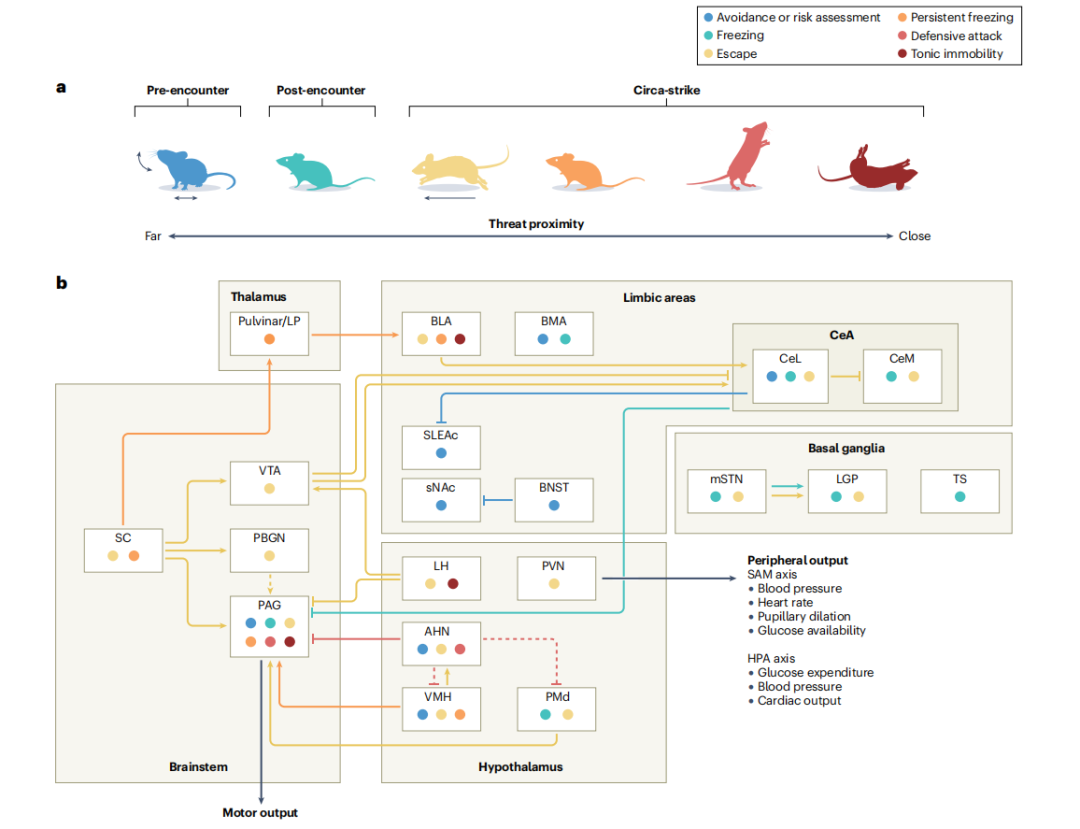
捕食威胁下的防御行为阶段和介导这些行为的神经回路与外周调控:
防御行为的“威胁紧迫性阶段”
动物(以小鼠为例)随捕食者距离(威胁 proximity)变化的防御行为,分为3个阶段:
1. 相遇前(Pre-encounter):威胁距离远,行为是回避/风险评估(蓝色小鼠的转向动作);
2. 相遇后(Post-encounter):威胁接近,行为是僵直(青色、黄色小鼠的静止姿态);
3. 攻击周边(Circa-strike):威胁极近,行为升级为逃逸、持续僵直、防御性攻击、强直不动(红色小鼠的逃跑、站立攻击、躺倒僵硬姿态)。
防御行为的神经回路与外周输出
当动物面临捕食性威胁时,上丘(SC)作为初级感觉整合中枢,首先检测视觉或听觉等威胁线索并将信号迅速传递至丘脑、中脑导水管周围灰质(PAG)以及杏仁核(包括基底外侧核BLA和中央核CeA)。杏仁核与终纹床核(BNST)共同构成边缘系统的核心节点,负责对威胁进行情绪赋值、评估其紧迫性并在“遭遇前”阶段驱动风险评估或回避行为。随着威胁逼近,信息进一步汇聚至下丘脑多个核团如调控应激反应的室旁核(PVN)和介导攻击/逃跑决策的腹内侧核(VMH),这些区域整合来自皮层、边缘系统及体内稳态信号,形成对当前情境的综合判断。
最终,PAG作为关键的运动输出枢纽,接收来自杏仁核、下丘脑等上游结构的输入,并通过直接投射至脑干运动中心,触发特定的防御动作:远距离威胁引发僵直或警戒,近距离则触发逃跑、防御性攻击甚至强直不动。这一行为梯度严格遵循“捕食逼近连续体”原则:威胁越近,行为越激烈、自动化程度越高。
与此同时,该神经网络并非孤立运作而是通过交感-肾上腺髓质轴(SAM轴)和下丘脑-垂体-肾上腺轴(HPA轴)与外周系统紧密耦合。例如,PVN激活HPA轴释放皮质醇,而PAG和下丘脑也驱动SAM轴,快速提升心率、血压、血糖和肌肉供氧,为“战或逃”提供生理支持。反过来,外周信号(如炎症因子、瘦素、睾酮或肠道代谢物)亦可通过迷走神经或血液循环反馈至杏仁核、下丘脑和PAG,动态调节防御反应的阈值与强度。
感染信号向大脑的传递途径
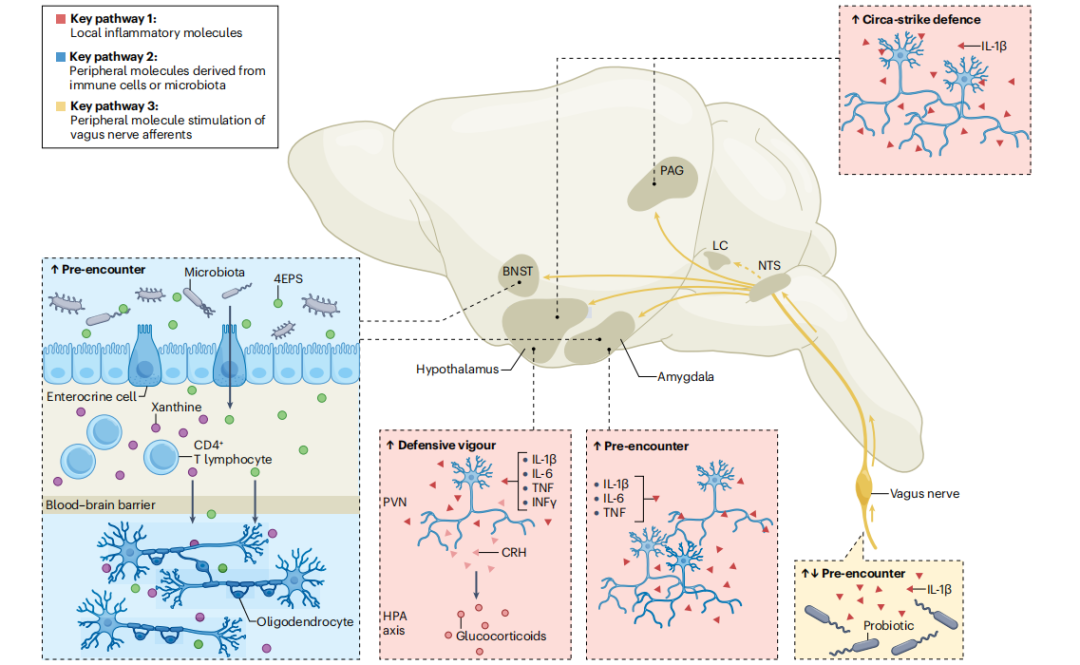
除了捕食者,传染性病原体也是动物进化中最强的选择压力之一。为应对感染,动物演化出一套免疫-行为协同系统:一方面将能量优先用于抗感染,另一方面仍保持对环境威胁的警觉以在不同威胁阶段(如风险评估、逃跑或僵直)灵活调整防御策略。
外周炎症信号如何影响防御行为?
1. 细胞因子是关键媒介
在啮齿类中,外周促炎细胞因子(如IL-1β、IL-6、TNF)可减少探索、增强回避。表现为“遭遇前”阶段防御强度的提升。人类研究也发现,焦虑症、PTSD等患者体内TNF和IL-1β水平升高,提示炎症与防御失调密切相关。
2. 三条主要通路将外周信号传入大脑:
(1)体液通路:细胞因子或微生物代谢物穿越血脑屏障
LPS虽不能入脑,但可诱导杏仁核局部合成IL-1β等,增强神经元活性与焦虑样行为。
肠道菌群代谢物4EPS可穿过血脑屏障,损害少突胶质细胞功能,激活杏仁核与BNST,诱发“遭遇前”防御反应。
外周CD4⁺ T细胞分泌的黄嘌呤进入脑内,促进少突胶质细胞增殖,间接导致杏仁核过度兴奋。
(2)神经通路:迷走神经介导快速信号传递
外周炎症激活迷走传入纤维,信号经孤束核(NTS)上传至PAG、杏仁核、BNST、PVN等防御相关脑区。
迷走神经切断可阻断LPS诱导的HPA轴激活和焦虑行为;益生菌的抗焦虑作用也依赖此通路。
NTS本身调控“遭遇前”行为:其神经元激活可诱发焦虑,而糖皮质激素受体拮抗则减少探索。
(3)HPA轴通路:炎症-应激-行为的系统整合
IL-1β等激活下丘脑PVN–CRH神经元,启动HPA轴,释放糖皮质激素(如皮质醇),既抑制炎症,又增强防御强度。
在高架十字迷宫(EPM)中,皮质酮水平与风险评估正相关;
高皮质醇的猴幼崽或儿童在“近身攻击”情境中表现出更持久的僵直,提示HPA轴可能放大高紧迫性防御反应。
肠–免疫–脑轴的整合作用:
肠道不仅是免疫前线,也是行为调节枢纽:
肠道感染诱发典型“遭遇前”防御行为,伴随菌群失调与迷走神经激活;
益生菌干预可减轻感染或应激后的焦虑,该效应被迷走神经切断所阻断;
无菌小鼠HPA轴反应过度,定植特定菌株可恢复正常;
微生物代谢物(如4EPS)直接作用于脑内情绪回路,改变行为输出。
身体状态动态调制威胁应对:
原标题:《脑声常谈|防御环路:威胁反应中的脑-体回路》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




