- +1
Neuron|戒烟会焦虑?南医大卢应梅/韩峰等揭示内侧缰核神经元放电变化介导尼古丁戒断诱发的焦虑
为什么很多人想戒烟却屡屡失败,戒断时的焦虑、烦躁总能让人半途而废?
这种难以忍受的戒断反应,或许并不是你意志力不够,而是大脑里一群神经元的放电模式改变了。

2026年3月27日,南京医科大学卢应梅、韩峰团队及美国芝加哥大学徐宇君(Eugene Yujun Xu)教授团队合作在《Neuron》上发表的研究《 Molecular brake on firing pattern transitions in MHbChAT neurons to mediate nicotine-withdrawalinduced anxiety 》,第一次把这个戒断焦虑的神经机制解析清楚了:
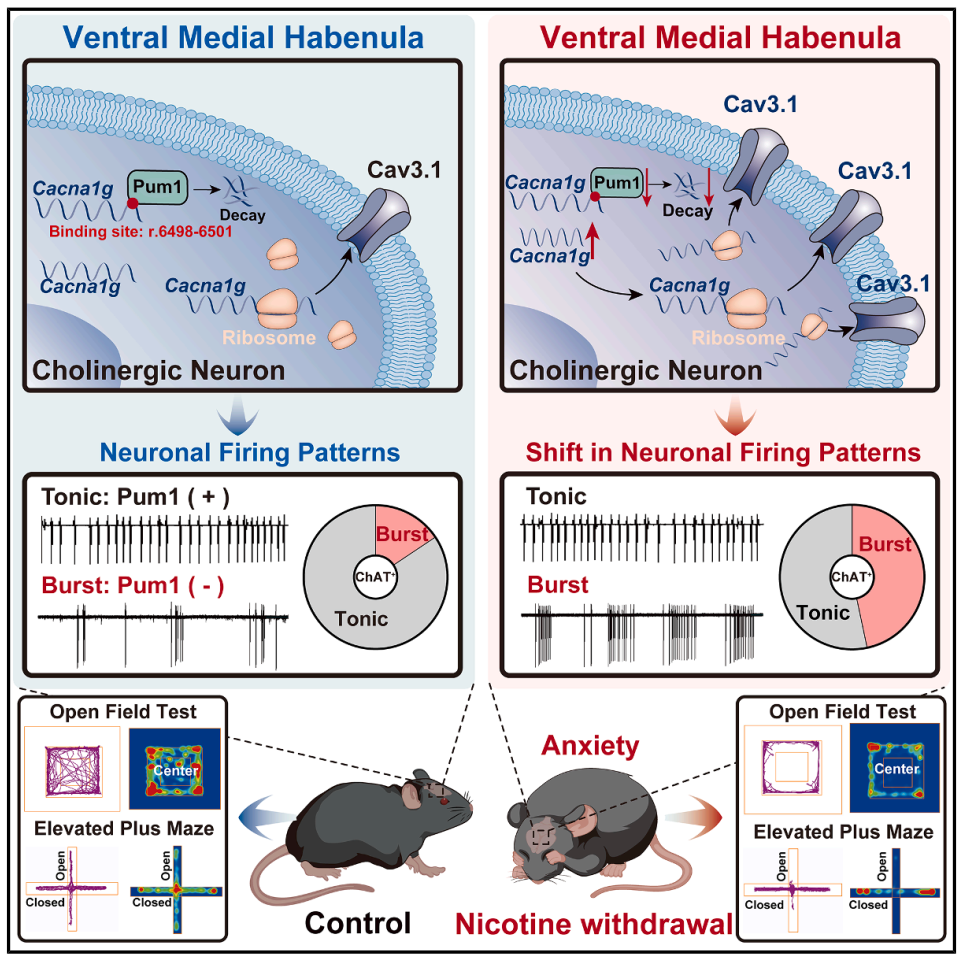
尼古丁戒断会引发内侧缰核胆碱能神经元从紧张性放电转为爆发性放电,这种放电模式的变化,直接导致焦虑。
这一变化由 Cav3.1 通道上调驱动,而 RNA 结合蛋白 Pum1 是调控该过程的分子刹车,其通过降解 Cav3.1 的 mRNA ,抑制通道表达。恢复 Pum1 功能或抑制 Cav3.1 能逆转戒断引发的神经元异常放电和焦虑样行为,为胆碱能功能障碍相关疾病提供了靶向治疗策略。
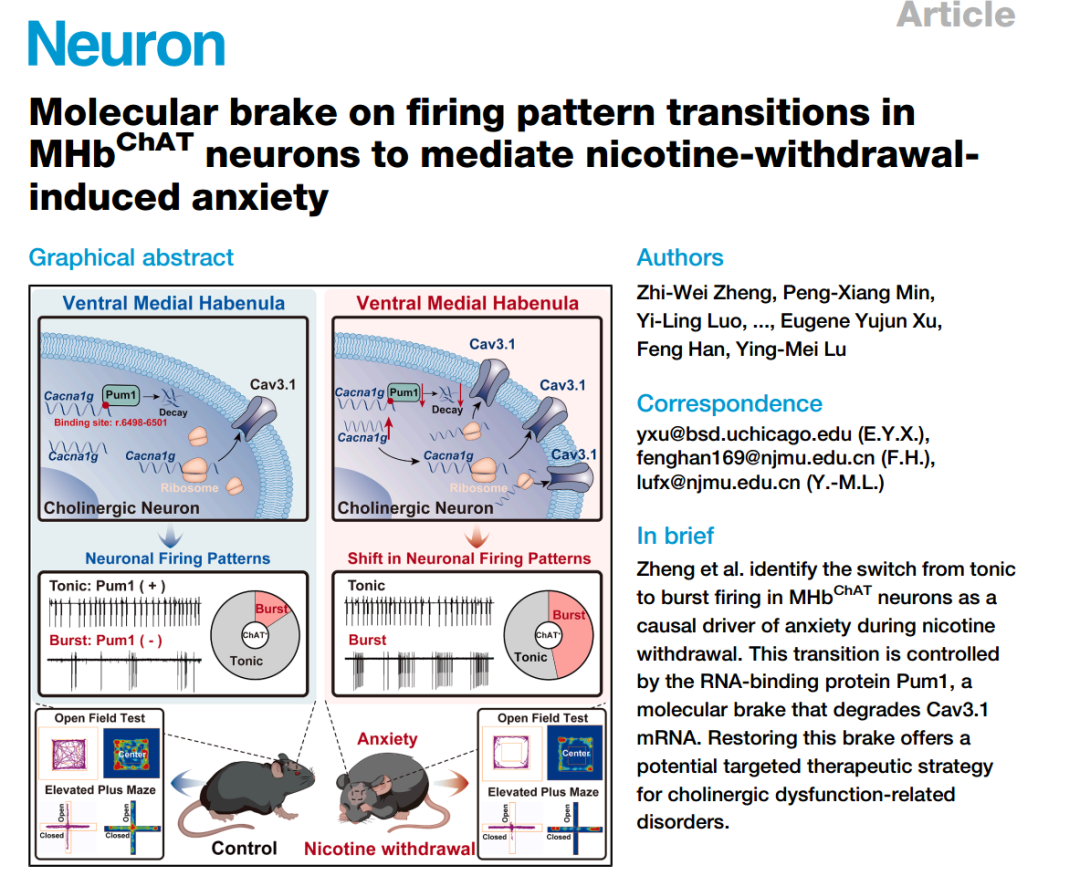
谁在制造戒断焦虑?
研究者聚焦内侧缰核(MHb)脑区(与尼古丁依赖密切相关)。
正常小鼠的胆碱能神经元,放电模式是规律的紧张性放电,但尼古丁戒断后,这些神经元开始爆发性放电,而且,爆发性放电的比例越高,小鼠的焦虑程度越严重。用光遗传学直接模拟这种爆发性放电,不需要戒断,小鼠就出现了焦虑样行为。
因此,戒断焦虑是神经元放电模式变了。
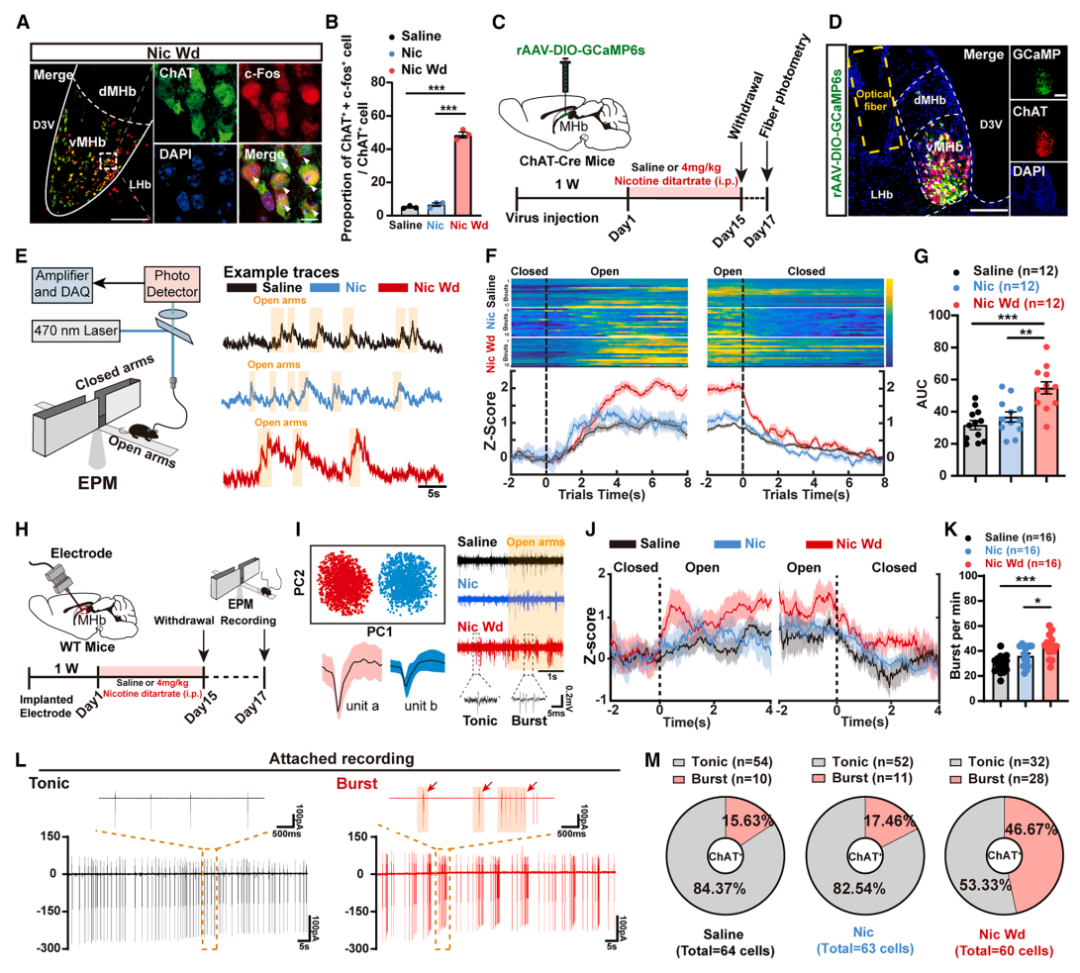
谁在驱动这种放电模式切换?
转录组测序分析戒断后MHb脑区的基因变化,发现Cacna1g基因显著上调(编码Cav3.1钙通道)。
用膜片钳记录,证实Cav3.1通道介导的钙电流增强,正是爆发性放电的核心原因。基因敲低或药理学抑制(米贝拉地尔)阻断Cav3.1 → 神经元恢复正常放电 → 戒断焦虑显著缓解。
因此,Cav3.1通道介导的钙电流增强,就是神经元放电模式改变的关键。
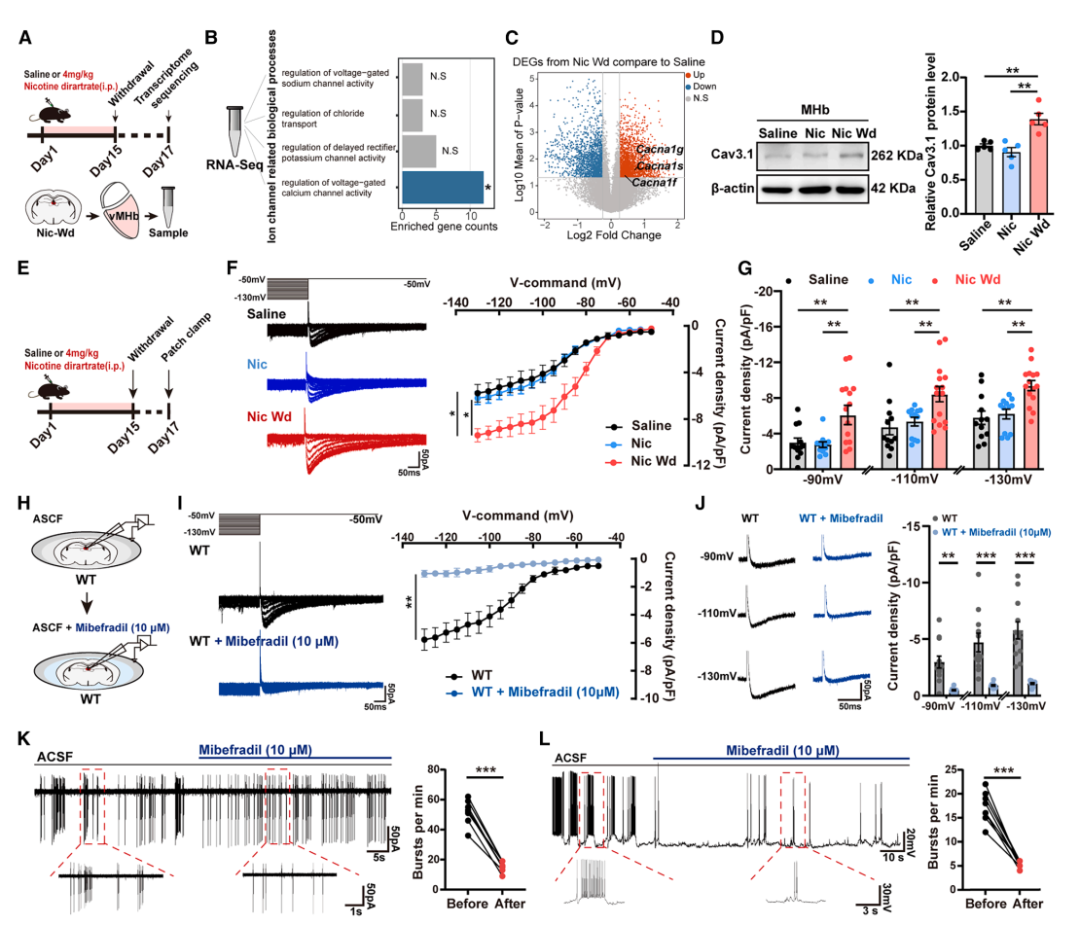
Pum1是调控该过程的分子刹车
转录组分析和蛋白检测发现,尼古丁戒断会下调 RNA 结合蛋白 Pum1,而 Pum1 与 Cav3.1 的表达负相关。
Pum1 可直接结合 Cacna1g mRNA并促进其降解,敲除 Pum1 会导致 Cav3.1 上调并诱发神经元爆发性放电和焦虑;反之,在该脑区过表达 Pum1,能通过抑制 Cav3.1 逆转尼古丁戒断引发的异常放电和焦虑,且不影响尼古丁的奖赏效应。
因此,Pum1 是调控该过程的分子刹车,刹车坏了,Cav3.1 上调,就会引发神经元爆发性放电。
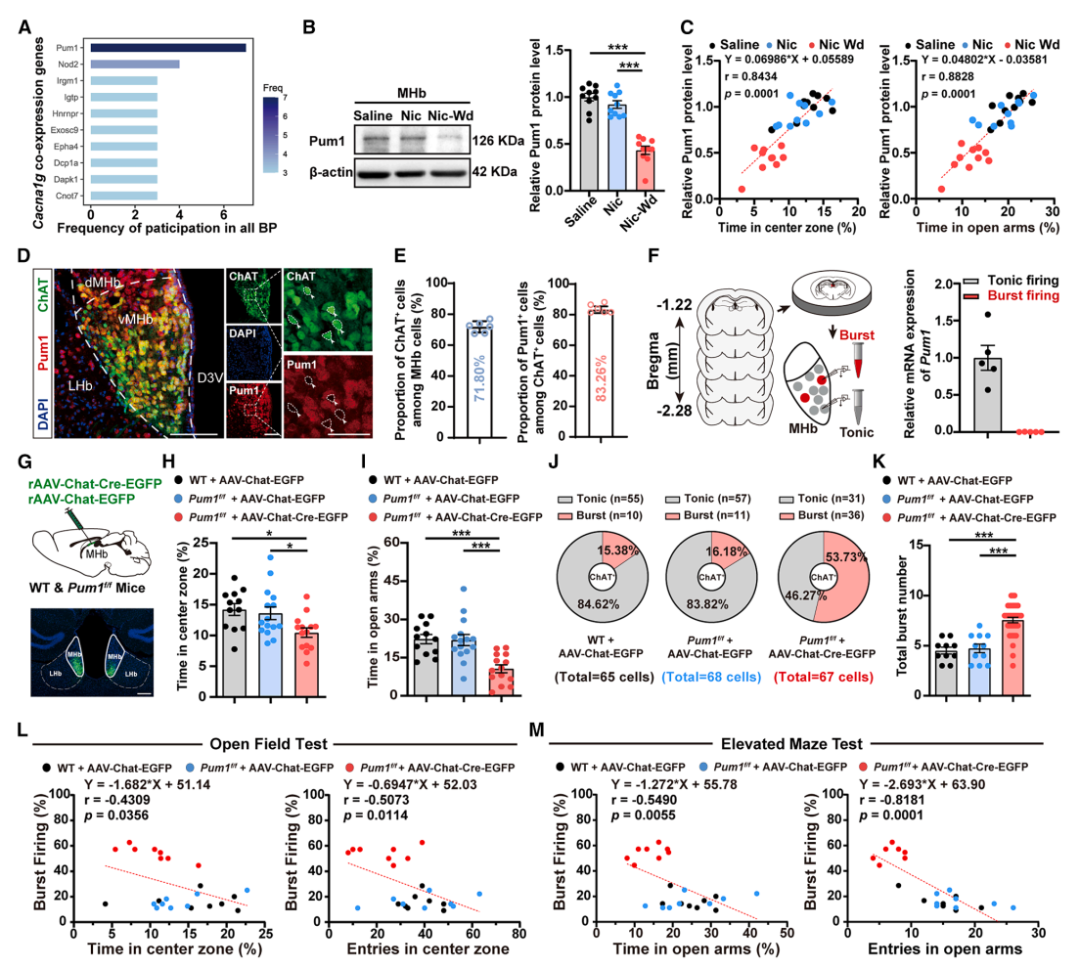
全文总结
该研究明确了尼古丁戒断焦虑的核心神经机制。腹侧内侧缰核胆碱能神经元的 Pum1-Cav3.1 轴失衡,导致神经元放电模式从紧张性转为爆发性,是驱动焦虑样行为的关键机制。Pum1 作为分子刹车,通过降解 Cav3.1 的 mRNA 抑制其表达。
恢复 Pum1 功能或靶向抑制 Cav3.1,能精准逆转神经元异常和戒断焦虑,为戒烟及相关胆碱能功能障碍疾病的治疗提供了全新的分子靶点和研究思路。
小编寄语:
尼古丁戒断焦虑,是戒烟失败的头号原因。无数人想戒烟,却败给戒断后的烦躁、焦虑、坐立不安。
以前,我们把这归为意志力问题,但南京医科大学卢应梅、韩峰团队的这项研究,把它变成了神经科学问题。
他们发现,尼古丁戒断后,内侧缰核的胆碱能神经元从规律的紧张性放电,变成了簇状的爆发性放电。这种放电模式的切换,直接驱动了焦虑。而背后的分子机制,是RNA结合蛋白Pum1的刹车失灵,导致Cav3.1通道上调。更关键的是,恢复Pum1功能或抑制Cav3.1,能精准逆转戒断焦虑,且不影响尼古丁的奖赏效应。这意味着,未来的戒烟辅助治疗,也许可以直接靶向这条分子通路。
那些想戒烟却屡屡失败的人,终于有了一个新的希望。

原文链接:
https://doi.org/10.1016/j.neuron.2026.02.020
原标题:《Neuron|戒烟会焦虑?南医大卢应梅/韩峰等揭示内侧缰核神经元放电变化介导尼古丁戒断诱发的焦虑》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




