- +1
Neuron | 石溪大学葛少宇/熊巧婕发现星形胶质细胞-新生神经元的糖代谢协作通路

我们平时能背书、刷题、吸收新知识,靠的就是大脑里不断新生的神经细胞。可这些刚长出来的脑细胞特别娇气,能不能活下来,关键就看能量够不够。就像人要学习、要靠吃饭补充糖分一样,大脑里的星形胶质细胞,会把葡萄糖转化成能量,专门给这些新生神经元供能打气。

2026年4月7日,纽约州立大学石溪分校葛少宇(Shaoyu Ge)、熊巧婕(Qiaojie Xiong)在《Neuron》发表题为:“Astrocytic glucose metabolism regulates the survival of newborn hippocampal neurons in the adult brain”的研究工作。
核心聚焦:本研究聚焦星形胶质细胞葡萄糖代谢对成年海马新生神经元存活的调控机制,通过多种体内外实验技术,系统解析了新生神经元与星形胶质细胞的代谢协作关系,明确了乳酸作为关键代谢物的核心作用。这一发现揭示了星形胶质细胞-新生神经元的代谢协作通路,为衰老和疾病中的成年神经发生研究提供了新视角。
新生海马神经元自身很难恢复胞内葡萄糖平衡
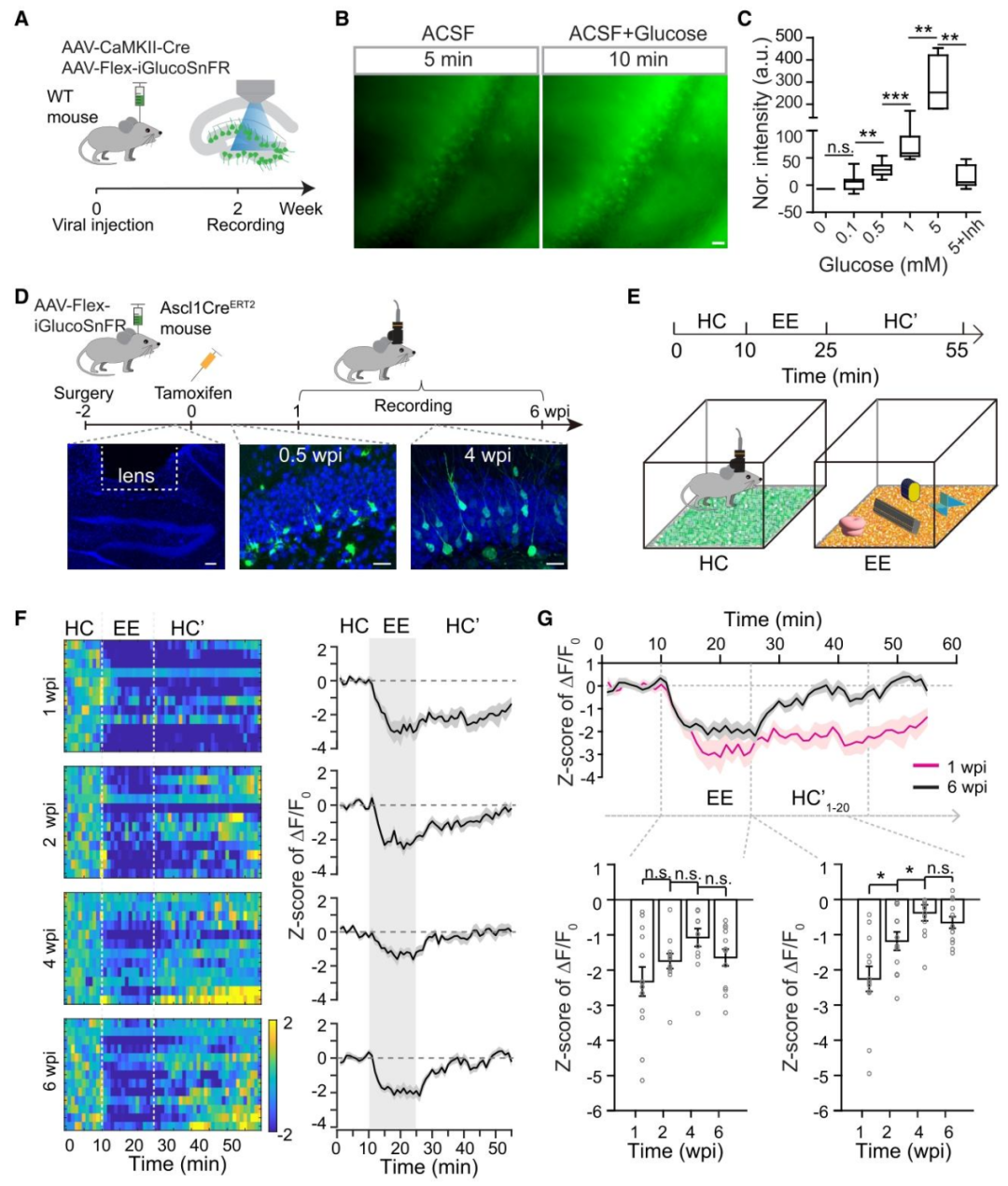
为研究葡萄糖是否影响新生齿状回颗粒细胞的存活,作者用葡萄糖生物传感器iGlucoSnFR做了验证:先在脑切片中测试,确认该传感器能精准反映细胞内葡萄糖变化,葡萄糖浓度越高荧光越强,抑制葡萄糖转运后荧光则会下降。
随后作者用转基因小鼠特异性标记新生齿状回颗粒细胞,结合活体成像,观察小鼠在普通环境、富集探索环境及恢复后,不同发育阶段新生细胞的葡萄糖变化。发现诱导标记后1周的新生细胞,在探索时胞内葡萄糖会持续下降,回到普通环境30分钟仍低于正常水平;且细胞越成熟,葡萄糖恢复速度越快,4-6周时就和成熟细胞的恢复模式一致了。这说明新生细胞在探索后,胞内葡萄糖恢复到正常水平的时间会显著变长。
另外作者还测试了新生细胞的葡萄糖摄取能力,诱导标记1.5周的新生细胞,在葡萄糖液中孵育后胞内葡萄糖无明显升高,而成熟细胞的胞内葡萄糖会显著上升,可见新生细胞的葡萄糖摄取能力很差。
同时作者发现,这些新生细胞周围,存在大量高表达糖酵解相关基因的星形胶质细胞。
星形胶质细胞摄糖影响新生神经元存活
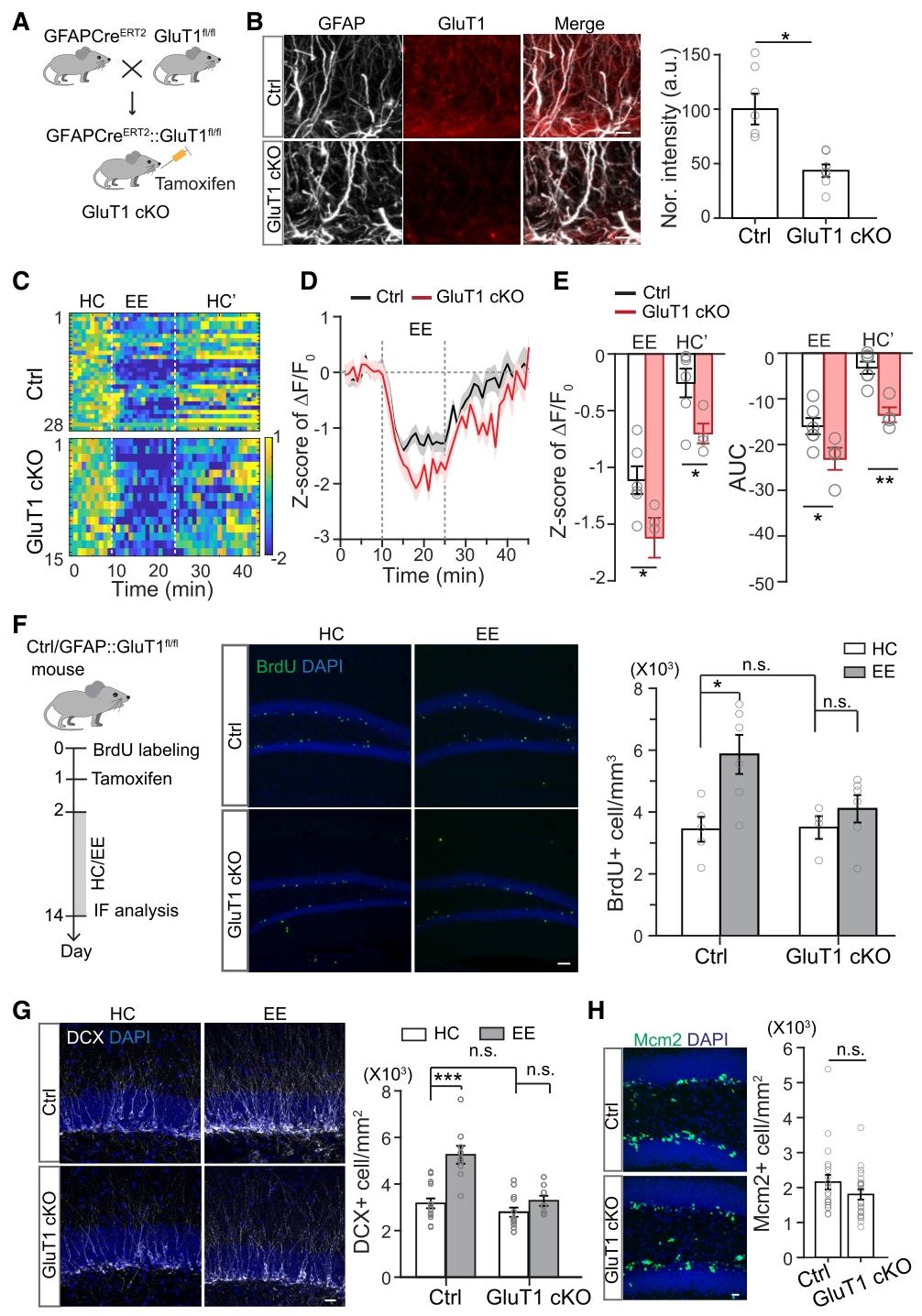
作者先通过分析发现,小鼠在富集环境中探索时,星形胶质细胞的葡萄糖摄取能力会增强。于是构建了星形胶质细胞特异性敲除葡萄糖转运体GluT1的小鼠,发现敲除后星形胶质细胞内葡萄糖下降得更明显,恢复也更慢。
随后用标记物追踪新生细胞,发现对照组小鼠在富集环境中,新生存活的细胞数量会比普通环境高约70%,但GluT1敲除的小鼠,这种存活促进效应几乎消失了。同时敲除小鼠的神经前体细胞增殖未受影响,说明仅抑制了新生细胞存活,而非增殖。
用药物阻断星形胶质细胞的GluT1,也得到了相同的结果。这说明不管是基因敲除还是药物抑制,只要阻断星形胶质细胞摄取葡萄糖,都会破坏其在探索时的葡萄糖代谢变化,进而大幅削弱新生齿状回颗粒细胞的存活。
自由活动小鼠海马区的细胞外乳酸动态变化
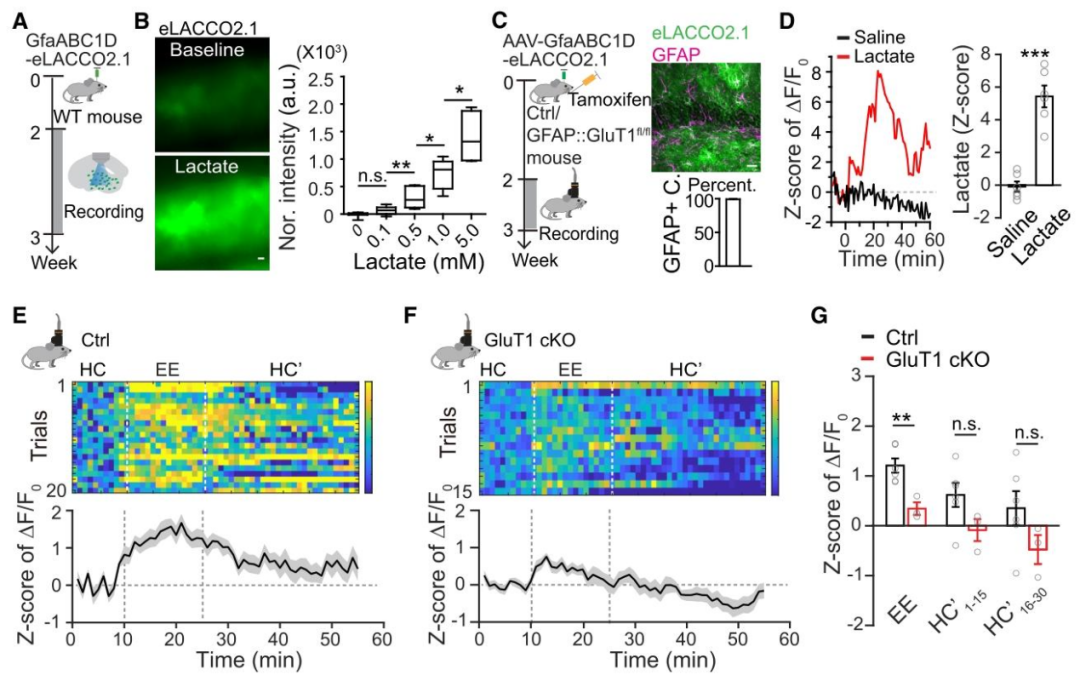
作者先为小鼠齿状回的星形胶质细胞,专门表达了能检测细胞外乳酸的生物传感器,同时设置了对乳酸无响应的突变传感器作为对照,验证后确认该传感器能精准、特异性地反映乳酸的动态变化,且对星形胶质细胞形态无影响;
后续还发现给小鼠补充葡萄糖后,齿状回的细胞外乳酸水平也会升高,说明葡萄糖能在该区域转化为乳酸。随后作者检测了小鼠在普通环境和富集探索环境下的细胞外乳酸变化,发现小鼠在富集环境中时,细胞外乳酸会明显上升,待返回普通环境后,乳酸水平能在20分钟内恢复至正常基线。而当特异性敲除星形胶质细胞中的GluT1后,富集环境本应引发的细胞外乳酸升高效应会被显著削弱;
同时还观察到,这些GluT1缺陷的星形胶质细胞,其葡萄糖的代谢变化和乳酸生成过程不再同步,二者出现了分离。
研究意义
理论意义:首次阐明了葡萄糖代谢在成年海马新生神经元活性依赖性存活中的调控机制,发现了星形胶质细胞的全新代谢功能,补充了成年神经发生的调控理论。
技术意义:利用基因编码的葡萄糖/乳酸生物传感器实现了自由活动小鼠海马细胞特异性的代谢物动态监测,为脑代谢研究提供了新的技术手段。
应用意义:为衰老、阿尔茨海默病、糖尿病等伴随海马神经发生受损的疾病,提供了以星形胶质细胞葡萄糖代谢/乳酸转运为靶点的潜在治疗方向。
文章来源:
https://www.cell.com/neuron/abstract/S0896-6273(26)00212-6
原标题:《Neuron | 石溪大学葛少宇/熊巧婕发现星形胶质细胞-新生神经元的糖代谢协作通路》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




