- +1
同济大学李永勇/李艳Cell Biomaterials: 纳米颗粒弹性调控巨噬细胞来源外泌体分泌以实现肿瘤免疫调节

物质科学
Physical science
近日,同济大学研究团队在Cell Press细胞出版社旗下期刊Cell Biomaterials上发表了题为“Piezo1-mediated regulation of macrophage-derived exosome secretion via nanoparticle elasticity for tumor immunomodulation”的研究论文。本研究建立了一种“纳米力学工程化外泌体”新范式,为力学调控外泌体免疫生物学提供了基础性见解,并为精准外泌体治疗提供了蓝图。
文章亮点
本研究揭示了纳米力学刺激可激活机械敏感性离子通道Piezo1,从而触发Ca²⁺内流。该Ca²⁺信号进而由CAMK2A介导,促使Rab8转变为GTP结合的活化状态,最终精确调控外泌体的分泌过程。
外泌体蛋白质组学表明,纳米力学工程化外泌体通过调控TCR信号通路,在体外促进T细胞活化,并在体内引发系统性抗肿瘤免疫(如脾脏CD8+T细胞扩增、肿瘤微环境免疫抑制细胞减少等),直接将机械刺激与高效的抗肿瘤免疫应答相关联。
本研究建立了一种“纳米力学工程化外泌体”新范式,为力学调控外泌体免疫生物学提供了基础性见解,并为精准外泌体治疗提供了蓝图。
文章简介
外泌体的生物调控机制对其生物合成、分泌及货物分选过程具有关键调控作用,在细胞间通讯、疾病发病机制及精准医学中发挥核心作用。力学因素作为细胞行为的关键调控者,其重要性日益凸显。然而,纳米力学信号如何调控外泌体分泌机制及其生物学效应仍鲜有研究。本研究系统揭示了纳米颗粒弹性对巨噬细胞外泌体分泌及其免疫功能的调控机制。
研究团队利用杨氏模量可调(103.2–1064.7 MPa)的纳米颗粒,创新性地提出低模量机械刺激可通过“Piezo1-Ca2+-CAMK2A/GTP-Rab8”轴促进巨噬细胞产生外泌体;这些外泌体通过协同放大TCR信号引发强效促炎反应,最终在体内表现出优越的肿瘤生长抑制及免疫抑制微环境重塑能力(图1)。
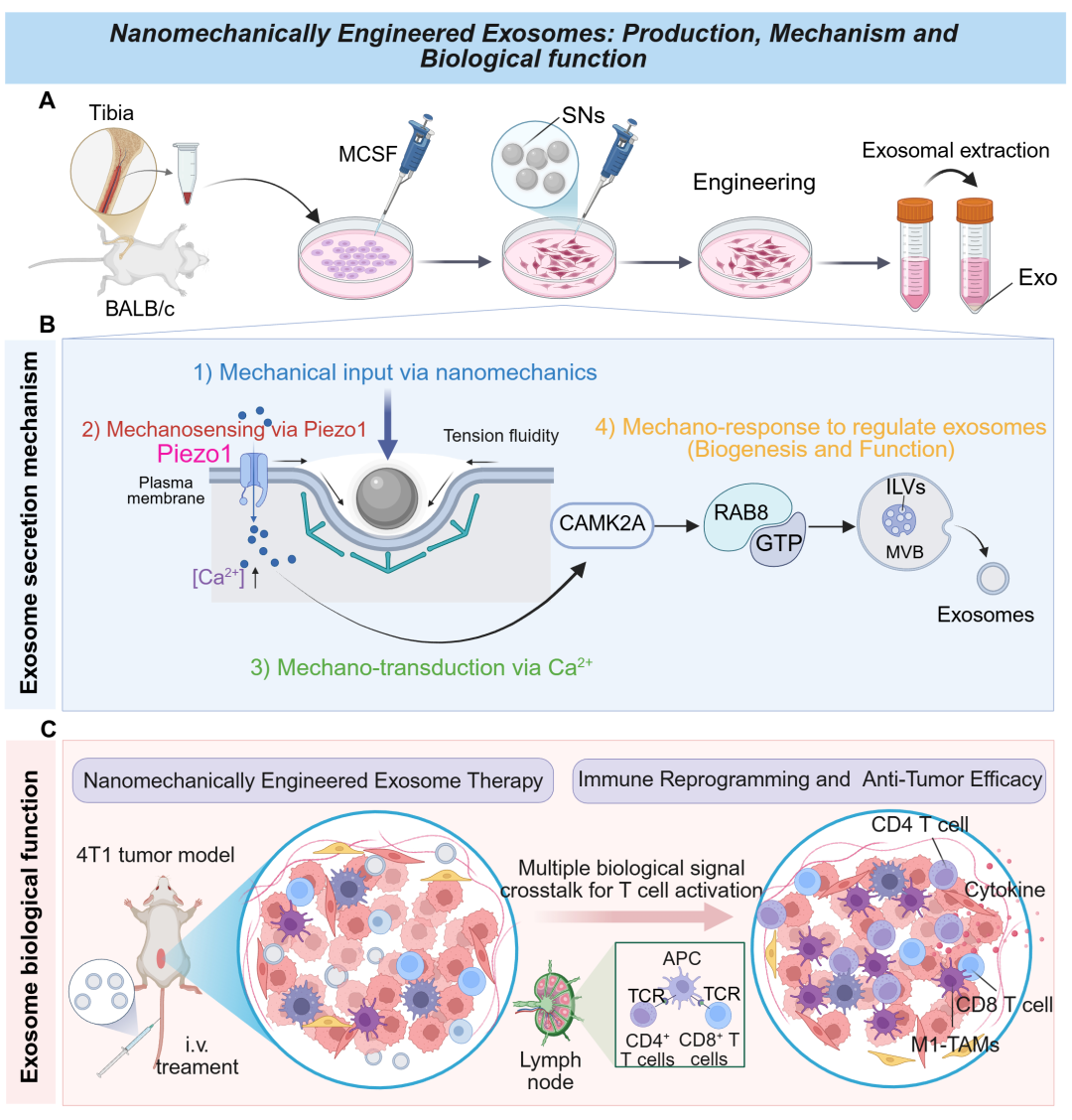
图1:巨噬细胞来源外泌体纳米力学工程策略示意图
本研究首先探讨了纳米力学刺激对骨髓来源巨噬细胞(BMDMs)外泌体生成的影响。并对外泌体大小、形态及外泌体标志物(CD63、TSG101和ALIX)进行表征分析。结果表明分离获得的外泌体呈现典型的碟状形态,平均直径约为100 nm。纳米颗粒追踪分析显示,在不同纳米力学刺激条件下,外泌体分泌量存在显著差异。BMDMs与低模量纳米颗粒共培养产生的外泌体数量约为对照组的3倍(图2)。
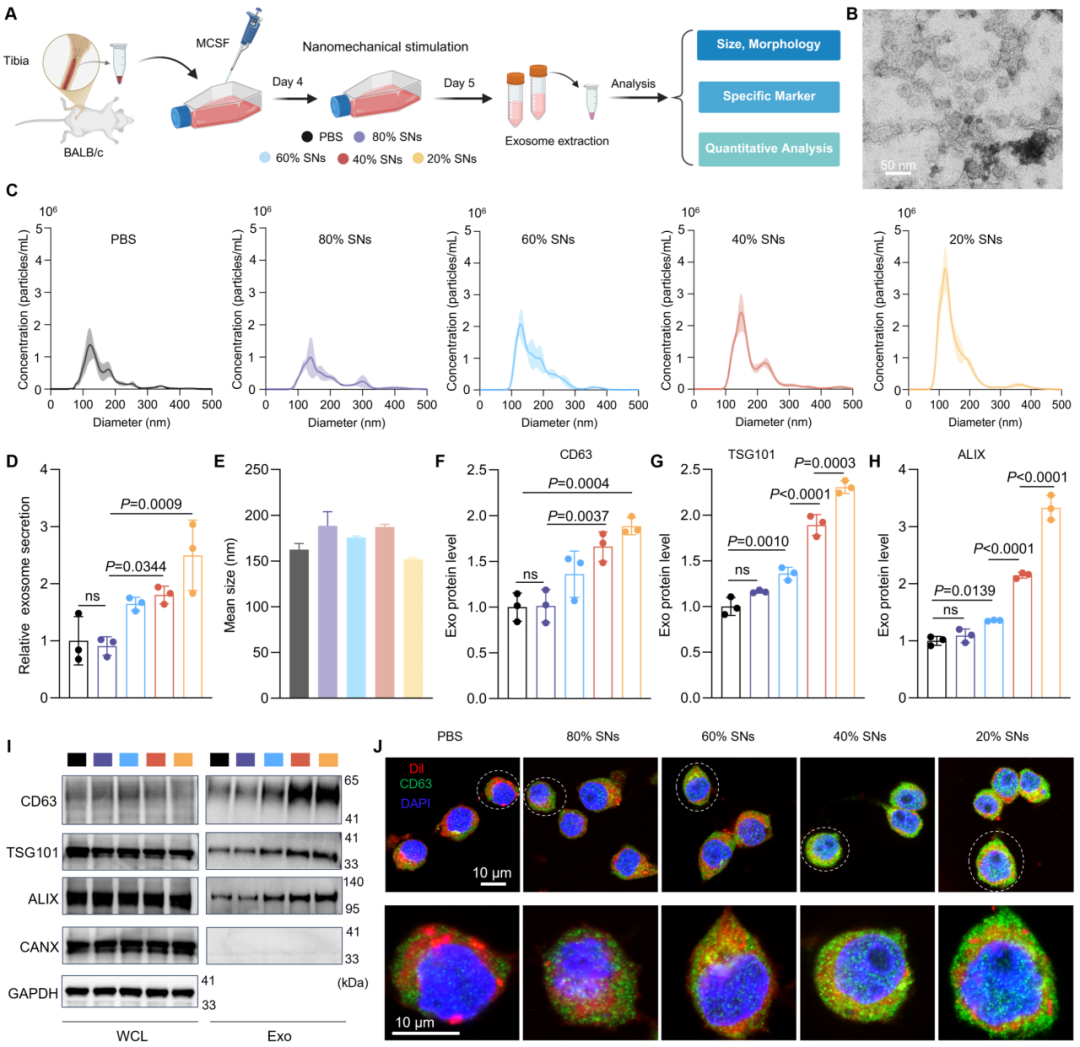
图2:纳米颗粒弹性调控巨噬细胞外泌体分泌。
随后,进一步研究表明纳米力学激活Piezo1蛋白,进而引发Ca²⁺内流及CAMK2A依赖性Rab8蛋白激活。该级联反应最终促进外泌体生物合成与分泌,外泌体标志物(CD63、TSG101和ALIX)表达水平升高即为证据(图3)。反之,抑制Piezo1或CAMK2A会破坏GTP-Rab8活性并阻碍外泌体分泌,由此证实Piezo1-CAMK2A-GTP/Rab8轴是纳米力学驱动外泌体释放的核心调控机制。
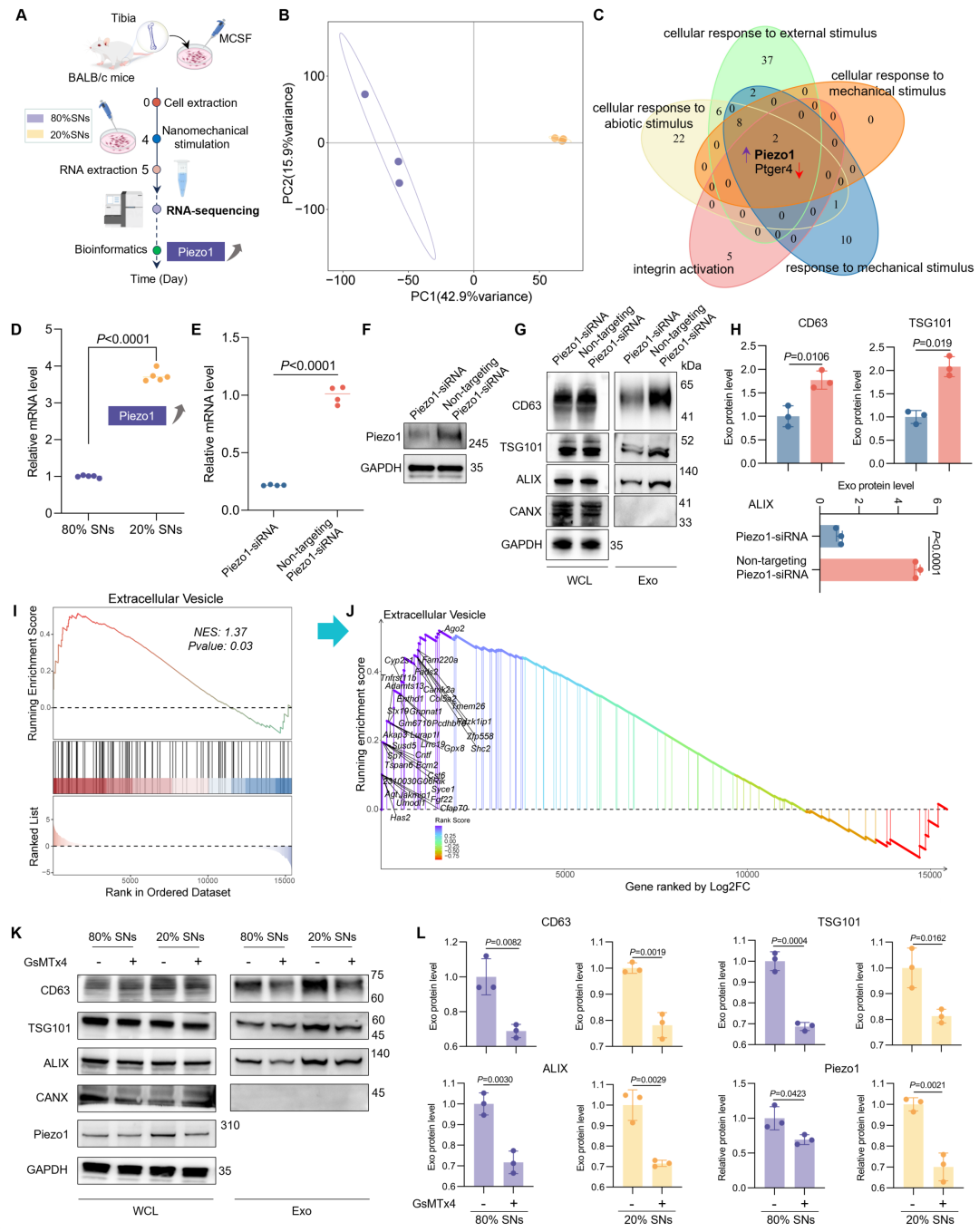
图3:Piezo1介导的纳米力学诱导外泌体分泌。
最后,体内4T1乳腺癌模型实验研究表明,低模量纳米颗粒处理后来源外泌体不仅表现出显著的肿瘤抑制活性,还为传统LPS诱导的外泌体疗法提供了一种更安全且更具生理相关性的替代方案(图4)。本研究凸显了纳米力学调控外泌体在重塑抗肿瘤免疫中的卓越疗效,为基于纳米力学诱导外泌体的免疫治疗提供了具有前景的策略。
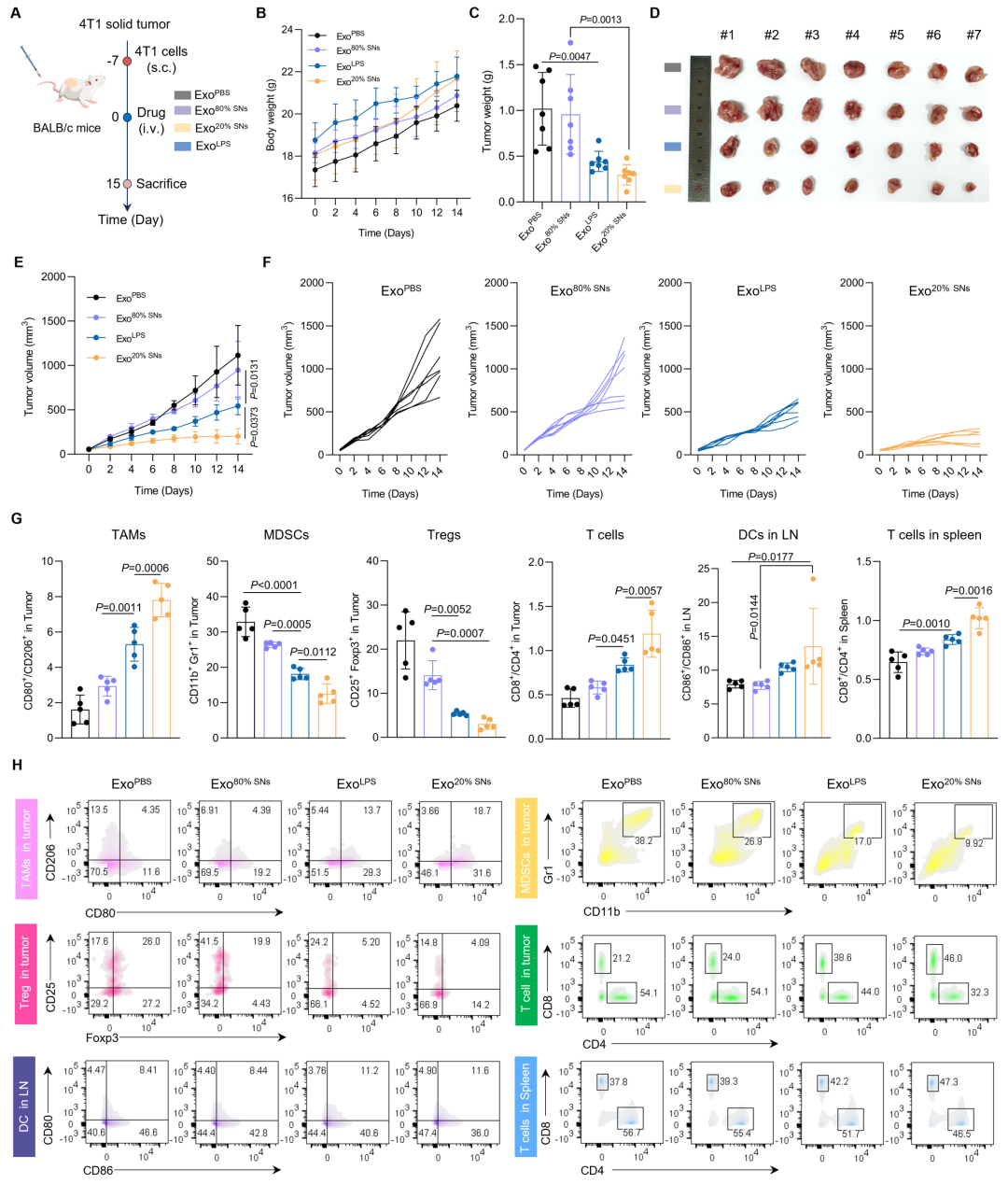
图4:纳米力学诱导外泌体的抗肿瘤治疗效应及免疫反应分析。
综上所述,本研究建立了纳米力学工程化外泌体的范式,为精准免疫治疗提供了新策略。
作者专访
Cell Press细胞出版社特别邀请研究团队进行了专访,为大家进一步详细解读。
CellPress:
请简要概述这项工作的亮点。
研究团队:
在细胞行为调控中,力学因素不仅是基本的物理信号,更是驱动特定生物学功能的核心要素。然而,纳米尺度的力学信号如何精确调控外泌体分泌及其下游免疫应答,仍是该领域未被揭示的关键瓶颈。本研究首次系统阐明了纳米颗粒弹性(杨氏模量)作为核心力学变量,对巨噬细胞外泌体分泌及其免疫调节功能的决定性作用,为力学免疫调控提供了新的见解。
CellPress:
研究过程中是否遇到了困难?团队是如何克服并顺利解决的?或是有任何有趣的故事可以与读者分享?
研究团队:
当前外泌体的力学调控研究主要集中于宏观尺度(如流体剪切力、基质刚度),而如何在纳米尺度实现单一力学变量的精准调控仍面临两大挑战:一是合成力学性质可控的纳米颗粒,二是对外泌体进行精确定量。针对上述问题,本研究摒弃复杂材料体系设计,创新性地将传统的药物递送载体(氧化硅纳米颗粒)转化为一种纳米力学调控器,利用其可精确调控的弹性模量这一“隐形”物理属性,干预巨噬细胞的外泌体分泌与货物分选。同时,本研究综合采用纳米颗粒追踪分析、外泌体标志物检测及免疫荧光等多重技术,实现了外泌体生成的可靠定量。
CellPress:
团队下一步的研究计划是怎样的?
研究团队:
未来的研究将不仅阐明机制,更致力于明确其功能输出与应用潜力。重点包括:揭示由不同弹性纳米颗粒诱导产生的外泌体,如何差异化调控T细胞、B细胞等免疫细胞的功能,从而精确影响抗肿瘤免疫或免疫耐受等生理病理过程。基于上述“力学编程”的外泌体,评估其作为新型免疫治疗制剂或靶向递送载体的潜力,为实现按需定制的细胞外囊泡疗法提供理论基础。
CellPress:
最后,是否可以与我们分享一下选择Cell Biomaterials来发表这个工作的原因?
研究团队:
Cell Biomaterials的核心宗旨在于探索生物材料与生命系统的前沿界面,并报道由此产生的医学突破。本研究通过赋予传统氧化硅材料以可调的力学性能,并将其作为工具揭示了纳米力学调控外泌体生物发生的新机制,完美契合了期刊所倡导的“材料驱动生物学发现”这一核心理念。

作者介绍

杨孜晨
博士研究生
第一作者:杨孜晨,同济大学医学院基础医学专业博士研究生,目前以第一作者在Cell Biomaterials,ACS Nano,J Control Release等国际权威期刊发表研究型论文5篇。
研究方向:材料力学生物学与免疫治疗

李永勇
研究员
通讯作者:李永勇,同济大学医学院研究员,博士生导师,当前致力于物理免疫调控的机制研究,并探索其变革慢病治疗模式的潜力。在Adv. Mater., Adv.Funct. Mater., Cell Reports, Adv. Sci., ACS Nano, Angew. Chem. Int. Ed.等期刊发表论文60余篇。
李艳
副研究员
通讯作者:李艳,同济大学医学院副研究员,硕/博士生导师,以纳米技术、力学调控及生物递送为核心,聚焦巨噬细胞表型重编程与免疫优化,探索疾病精准治疗新范式。在Advanced Functional Materials、ACS Nano、Advanced Science、Cell Reports、Biomaterials、J Control Release、ACS Applied Materials &Interfaces、Nano Research等国际期刊发表SCI论文30余篇。
▌论文标题:
Piezo1-mediated regulation of macrophage-derived exosome secretion via nanoparticle elasticity for tumor immunomodulation
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S3050562326000437
▌DOI:
https://doi.org/10.1016/j.celbio.2026.100387
原标题:《同济大学李永勇/李艳Cell Biomaterials: 纳米颗粒弹性调控巨噬细胞来源外泌体分泌以实现肿瘤免疫调节 | Cell Press对话科学家》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




