- +1
梦泽邀谈2|逆转生命时钟:iPSC技术二十年——从实验室奇迹到“人体零件工厂”的蜕变
转载需获取授权,请至后台留言
正文5200余字,预计阅读18分钟
【核心看点】
iPSC技术诞生二十年,日本两款疗法率先获批上市,标志着iPSC疗法从“艺术品”迈向“药品”。国家干细胞转化资源库副主任贾文文,以一线亲历者视角,梳理技术演进脉络,解析中日美全球竞速格局,直面致瘤性、免疫排斥、成本三大挑战。化学重编程“中国方案”,正在改变世界格局。
从“艺术”到“工程”,iPSC技术二十年,终于从实验室走向了患者。
【正文】
2007年,山中伸弥团队成功诱导获得人诱导多能干细胞( Human Induced Pluripotent Stem Cell,iPSC),这项突破像一颗种子,在此后二十年间迅速生长、开花、结果。
今年2月的一个下午,手机上弹出一条新闻:日本两款iPSC疗法获批上市。我正在和同事讨论iPSC衍生药物的申报材料,那一刻,我们几乎同时抬起头,对视了一眼。
那一刻,我心里涌起一种复杂的情感——这条路,走了二十年,终于走到了患者面前。
今天,我想和同行们聊聊我眼中iPSC技术的这二十年。
一、2026年春天,我们等来了什么?——从“奢侈品”到“药品”的跨越
今年2月,日本厚生劳动省批准了两款基于诱导多能干细胞(iPSC)的细胞疗法上市——ReHeart用于治疗重症心力衰竭,Amchepri用于治疗帕金森病。这不仅仅是一条新闻,更是一个时代的注脚。
作为从业者,我们更关心的是:这两款产品凭什么能获批?它们背后的技术路线意味着什么?
ReHeart这款产品很有意思。它不是简单地注射细胞悬液,而是将iPSC分化出的心肌细胞制备成细胞膜片,像贴膏药一样直接贴附在患者受损心脏表面。临床数据显示,这种结构能更好地促进血管新生和心肌修复。临床数据显示,8名重症患者在移植一年后症状均有改善,其中4名症状完全消失——对于终末期心衰患者来说,这几乎是“起死回生”级别的疗效。
Amchepri则走的是另一条路。它将iPSC分化成的多巴胺能神经前体细胞精确注射到患者脑内,替代因疾病而死亡的多巴胺神经元。Nature上发表的数据显示,患者在24个月随访中,运动症状评分显著改善了38%。要知道,帕金森病患者最痛苦的就是那种“身体不听使唤”的失控感,38%的改善,意味着他们可能重新获得自己系鞋带、端杯子的能力。
更值得关注的是,这两款产品均采用同种异体(现货型)策略。它们不是为每个患者单独定制,而是利用健康供体建立的iPSC库,实现了规模化生产、冷冻保存和“随取随用”。我在东方医院GMP实验室工作这些年,最深的体会就是:细胞疗法要想真正惠及患者,必须走产业化道路。个体化定制成本太高、周期太长,无法大规模推广。现货型产品的出现,意味着细胞疗法正在从“奢侈品”变成“药品”。
当然,日本的批准是有条件的——企业需在7年内完成有效性确证,否则许可将被撤销。这背后折射出的是一种审慎的乐观:我们相信这条路是对的,但还需要更多数据来证明。
二、回望2006年:一场“细胞返老还童”的冒险——诺奖光环背后的技术隐患
把时间拨回2006年。那一年,日本京都大学的山中伸弥团队在 Cell 杂志上报道了一组神奇的“四因子”——Oct4、Sox2、Klf4和c-Myc。当这些因子被导入到小鼠的皮肤成纤维细胞中时,奇迹发生了:这些已经“定型”的体细胞竟然被逆转回了具有胚胎干细胞特性的多能状态,这就是iPSC的诞生。
为什么说这是“奇迹”?因为在iPSC诞生之前,人类获取多能干细胞的唯一途径主要依赖于胚胎干细胞,这涉及到对早期胚胎的破坏,伦理争议从未停歇。而iPSC的出现,让科学家们看到了一种可能:从患者自身细胞出发,逆转生命时钟,再生出任何需要的组织。
2012年,山中伸弥与约翰·戈登共同获得了诺贝尔生理学或医学奖。评委会的评语是:他们证明了“成熟的、特化的细胞可以被重编程,变成未成熟的、具备发育成各种组织潜能的细胞”。
但作为一线研究者,我们很清楚:诺奖的光环背后,是巨大的技术隐患。早期使用的逆转录病毒载体,其基因有随机插入宿主基因组的风险,可能诱发肿瘤。特别是致癌基因c-Myc的存在,更是让人捏一把汗。
三、技术迭代:从“转基因”到“无痕”的二十年——从“艺术”到“工程”的蜕变
正是因为有这样的顾虑,全球科学家开启了长达近二十年的技术竞赛。这不是效率的比拼,而是对安全的极致追求。
第一波突破:非整合技术。
科学家们开发出了使用仙台病毒、质粒、mRNA甚至蛋白质的直接导入法。这些方法就像“临时工”,在完成细胞改造后便会自行降解,不再留下任何外源基因痕迹。
2018年我在同济大学附属东方医院干细胞基地GMP实验室时,我们就在摸索CTS仙台病毒体系的工艺。记得有一次,连续传代到P8的细胞仍存在残留检测阳性的问题,整个团队几乎崩溃。后来我们发现改变传代方式可以极大地降低残留——这让我深刻体会到:从科研到GMP,每一步都有坑,但每一步都值得。
第二波突破:化学重编程。
2022年,北京大学邓宏魁团队带来了颠覆性突破。他们仅使用化学小分子组合,成功诱导出多能干细胞(CiPSC)。这一技术完全避免了基因操作,让重编程过程变得更加可控、简单且安全。2025年,邓宏魁团队又建立了更快更高效的化学重编程体系,诱导周期由原来的50天缩短到30天以内,最短16天即可完成。我在一次行业会议上听到这个消息时,第一反应是:这是真正意义上的“中国方案”。
当然,这一技术距离大规模产业化应用还有工艺放大的路要走,但方向已经明确。
我个人的判断是:化学重编程正在把iPSC技术从“艺术”变成“工程”。过去,重编程的成功率很大程度上取决于操作者的经验;现在,化学小分子组合让整个过程变得标准化、可重复。这对于产业化至关重要。
四、全球竞速:从实验室到患者的产业化进程——谁在领跑,谁在追赶?
2026年日本的药物审批,是iPSC技术从“研究”走向“产业”的分水岭。但日本并不是唯一的玩家。在这场全球竞速中,美国、中国等多个产品已进入或完成临床试验,覆盖了从神经退行性疾病到心血管疾病、从糖尿病到肿瘤免疫的广泛适应证谱系。
(一)日本:先行者率先获批
凭借山中伸弥等科学家的原创优势,日本在iPSC领域一直扮演着先行者角色。2026年2月,两款产品率先获批上市:
ReHeart(心衰治疗):将iPSC分化心肌细胞制备成细胞层片,贴附于受损心脏表面。临床数据显示,8名重症患者移植一年后症状均有改善,其中4名症状完全消失。
Amchepri(帕金森治疗):将iPSC分化多巴胺能神经前体细胞注射至患者脑内,替代死亡神经元。24个月随访显示运动症状评分改善38%。
这两款产品均采用同种异体(现货型)策略,利用健康供体iPSC库实现规模化生产,标志着细胞疗法正在从“奢侈品”向“药品”转变。
(二)美国:多适应证并行推进
美国在iPSC领域的布局呈现“多点开花”的特点,覆盖神经系统、肿瘤免疫、内分泌代谢等多个疾病领域,详见表1。
表1 美国iPSC疗法神经系统适应证进展
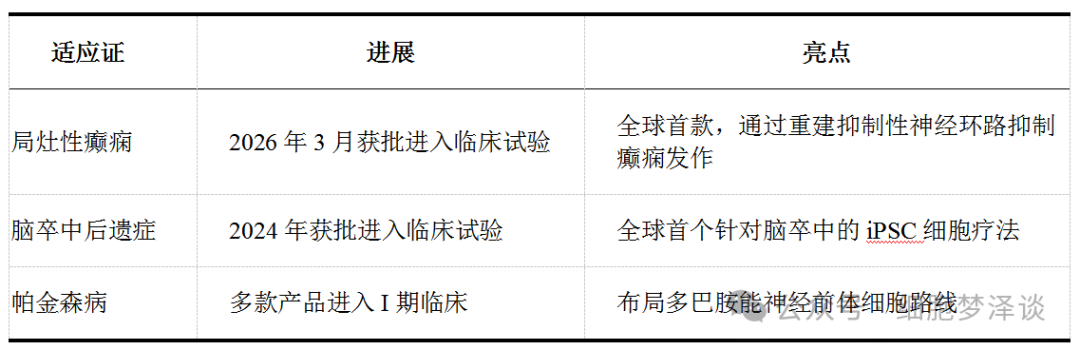
在肿瘤免疫领域,基于iPSC分化的自然杀伤细胞(iNK)疗法正在加速推进。这类产品通过基因编辑增强对肿瘤细胞的靶向杀伤能力,实现“现货型”规模化生产,已进入临床前及早期临床阶段。
在内分泌代谢疾病领域,针对1型糖尿病的iPSC衍生胰岛细胞疗法已完成临床前研究,正在向临床试验阶段迈进。
(三)中国:化学重编程原创突破,多个适应证实现“全球首个”
中国在iPSC领域的崛起,得益于原始创新能力的突破和“中美双报”策略的成熟应用。
1. 原创技术:化学重编程(CiPSC)
北京大学邓宏魁团队开创了完全避免基因操作的化学重编程技术:
2022年:首次报道使用化学小分子组合诱导获得多能干细胞(CiPSC)
2024年:世界首例CiPSC来源胰岛移植成功,该成果发表于Cell,获国际干细胞领域广泛关注。一名1型糖尿病患者从第75天起完全脱离胰岛素注射,随访1年以上疗效稳定
2025年:建立更快更高效的化学重编程体系,诱导周期由原来的50天缩短到30天以内,最短16天完成
这一技术为糖尿病治疗提供了“中国方案”,在安全性和可控性上具有独特优势。
2. 神经系统疾病:多个赛道实现“全球首个”
中国在神经系统疾病领域的进展见表2。
表2 中国iPSC疗法神经系统适应证里程碑进展
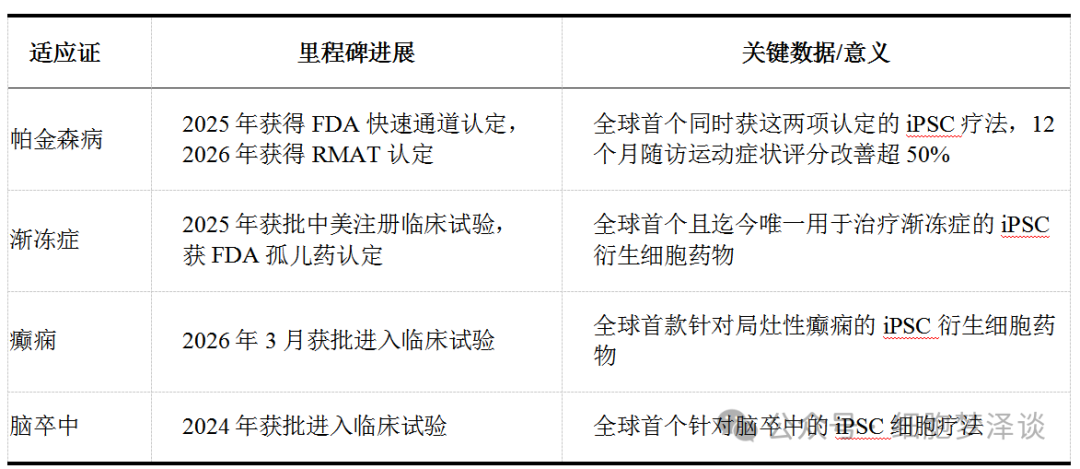
3. 心血管疾病
中国自主研发的人iPSC来源心肌细胞治疗心力衰竭的创新药,是全球首个在中美双获批IND的重度心衰细胞创新药,目前正在中国、美国、新加坡、泰国开展多中心临床试验。
4. 产业进展概览
据公开信息统计,中国企业在帕金森病、渐冻症、癫痫、多系统萎缩等多个适应证上累计获得数十项中美临床试验批件,多个产品进入临床I/II期阶段(详见表3)。
表3 中国企业iPSC疗法临床进展概览
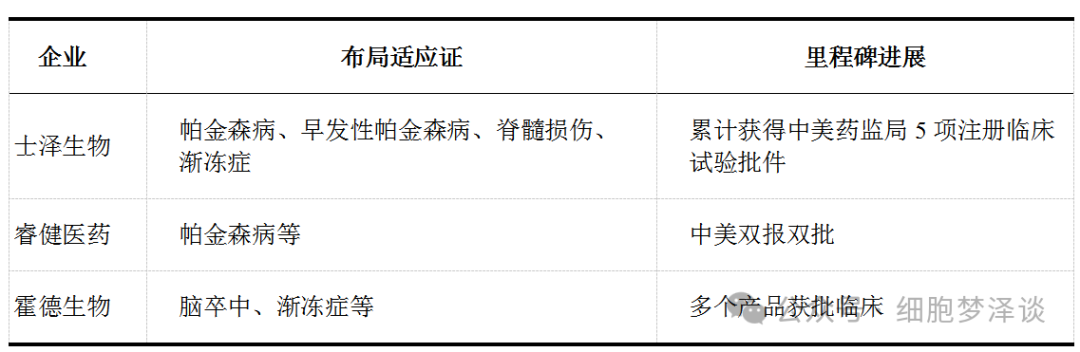
(四)细胞库建设:产业化的重要基石
iPSC疗法的规模化应用,离不开高质量的细胞资源库支撑。目前,中国正积极推进HLA高匹配临床级iPSC库的建设:
日本计划:以75个细胞系覆盖全国80%的人口。
中国进展:国家干细胞转化资源库(依托同济大学生科院和附属东方医院建设)已建立可覆盖60%人群的HLA配型iPSC库(基于现有HLA分型数据的理论覆盖),这是目前已知的亚洲最大规模的HLA高匹配临床级iPSC库。
需要说明的是,这一工作虽然不直接面向临床,却是“现货型”产品能否真正惠及患者的基础——没有标准化的细胞库,就没有可及性的细胞药。
(五)全球格局小结
主要国家/地区iPSC疗法发展格局见表4。
表4 主要国家/地区iPSC疗法发展格局
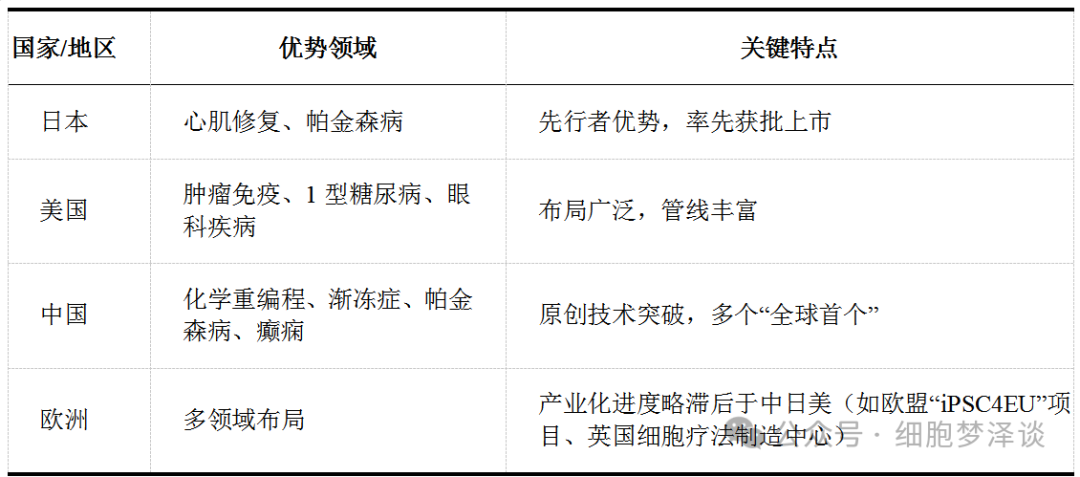
监管机构对iPSC疗法的态度,正在从“谨慎观望”转向“加速认可”。值得注意的是,各国在iPSC领域的竞争是动态的,中国在化学重编程等原创技术上的突破正在改变全球格局。
五、挑战依然存在:光明中的审慎——致瘤性、免疫排斥、成本,三道必答题
尽管里程碑已经树立,但作为一线从业者,我们必须保持冷静。山中伸弥教授本人就曾公开表示:“通过更多的临床案例来验证安全性和有效性是必不可少的过程……我们必须以科学的审慎态度,一步一步向前迈进。”
目前,iPSC疗法仍需克服以下三大核心挑战:
第一,致瘤性。
未分化的iPSC有形成畸胎瘤的风险。如何确保移植的细胞达到安全、有效的纯度比例?如何检测那千万分之一的残留未分化细胞?这是GMP生产中的极高门槛。我所在的实验室,每一批细胞放行前都要经过至少12项质控检测,其中半数以上与安全性相关。有同行问我:“这么多检测,成本怎么降?”我的回答是:安全是不能讨价还价的底线。
第二,免疫排斥。
即使是“现货型”细胞,也需要进行HLA配型。日本正在建立的iPSC库计划以75个细胞系覆盖全国80%的人口,但中国人口基数大、种族多样性更复杂,这个目标实现起来难度更大。我们正在做的HLA高匹配库,虽然只能覆盖60%的人群(基于现有HLA分型数据的理论覆盖),但已经是目前国内覆盖面最广的临床级iPSC库。
第三,成本。
目前的细胞药物制备成本依然高昂。以目前的生产工艺测算,一剂“现货型”iPSC细胞产品的生产成本约为传统小分子药物的数十至上百倍。如何在保证质量的前提下实现工艺的稳定放大,是让这些药物进入医保、惠及大众的关键。我个人的判断是:未来5年,随着自动化、封闭式生产系统的普及,成本有望下降一个数量级。
六、结语:二十年,只是一个开始——与所有同行共勉
从2006年那一个小小的培养皿,到2026年进入临床的救命药,iPSC技术走过了二十年。
作为一名亲历者,我见证了这个领域从“冷板凳”到“风口”的整个过程。我见过凌晨三点的实验室,也经历过细胞污染后从头再来的崩溃时刻。有人问我,为什么还在坚持?我说,因为每一次看到那些临床数据——心衰患者重新站起来,帕金森患者重新拿起筷子——我都觉得,凌晨三点的实验室,值得。
这场关于生命定义的认知革命告诉我们:细胞的分化并非不可逆的单行道,生命的时钟在分子层面是可以被重设的。
这或许只是一个序章。未来的十年,随着基因编辑技术与iPSC技术的深度融合,以及“通用型”细胞库的全球化普及,人类真的有可能迎来一个可以随意更换“人体零件”的医疗新时代。
对于无数心衰、帕金森病、失明甚至糖尿病的患者来说,这场始于二十年前的科学探索,正将科幻中的“再生”,一点一点变成病房里的奇迹。
与所有在干细胞领域奋斗的同行共勉。
【作者简介】
贾文文,国家干细胞转化资源库副主任,同济大学生命科学与技术学院副教授、博士生导师,上海干细胞临床转化研究院特聘研究员。兼任上海同金干细胞科技有限公司副总经理。2018-2025年曾任同济大学附属东方医院干细胞基地GMP实验室主任。
本硕博毕业于西北农林科技大学,美国宾夕法尼亚州立大学联合培养博士。
长期从事临床级干细胞(iPSC、成体干细胞)制备、质检及临床转化研究。主持国家自然科学基金、国家重点研发计划课题等10余项,发表SCI论文50余篇,获授权专利17项,参与制定干细胞相关标准5项。
【关于“梦泽邀谈”专栏】
本专栏由“细胞梦泽谈”公众号主理人梦泽先生发起,特邀生物医药领域、细胞产业链的专家学者、企业创始人、临床研究者、政策观察者,就行业热点问题进行撰文观察、深度分析与理性反思。不为流量,不为喧哗,只为给关注这个领域的同行者,提供一份有价值的参考。
编辑、审校:梦泽
原标题:《梦泽邀谈2 |逆转生命时钟:iPSC技术二十年——从实验室奇迹到“人体零件工厂”的蜕变》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




