- +1
脑声常谈总结|肠治久安?肠道微生物如何远程操控你的“喜怒哀乐”
肠道微生物群-脑轴由免疫、神经、内分泌、代谢系统构成的双向交流网络,是维持胃肠道、中枢神经和微生物系统稳态的关键。人体肠道菌群包含细菌、古菌等,细菌数量与人体细胞相当,菌群基因组约含2.32 亿个基因,代谢能力堪比人类肝脏;其组成和活性受饮食、年龄、基因、药物等因素动态调控。肠神经系统(ENS)作为 “第二大脑”,与中枢神经系统(CNS)通过迷走神经连接,无菌(GF)小鼠存在神经发生、髓鞘形成等发育异常,证明肠道菌群对神经系统发育的关键作用。
在微生物学与神经科学的交叉领域,过去十年间的开创性研究正逐步揭示,动物与其肠道定植菌群之间存在动态相互作用,而这种作用对神经系统的形成与功能发挥着重要作用。二者的 “交流” 过程十分复杂,通过免疫、神经和化学信号传导等多种方式实现,却对人体健康以及我们对神经系统疾病的认知有着至关重要的影响。
长期以来,精神疾病被认为完全由大脑生理过程的缺陷引发;然而,这种以大脑为核心的视角忽略了一个事实,神经系统的发育与功能会受到机体代谢和免疫状态的影响。当代研究正逐渐探明微生物的作用机制:它们能够在肠道中生成并调节多种代谢、免疫和神经化学因子,而这些因子最终会对神经系统产生作用。这一新视角催生出大量相关研究,将微生物群落及其功能与各类神经精神疾病关联起来,包括发育相关疾病(如自闭症谱系障碍、精神分裂症)、情绪障碍(如抑郁症、焦虑症)以及神经退行性疾病(如帕金森病、阿尔茨海默病和多发性硬化症)。
为厘清这些关联开展的研究,在很大程度上依赖于简化的动物模型,但这类模型难以还原人类疾病的复杂全貌。目前,肠道微生物群与神经精神疾病之间关联的潜在机制尚未得到广泛验证,不过相关新技术正不断研发,助力研究走出相关性分析的范畴,进一步发掘并验证具有实际人类疾病治疗潜力的生物学作用机制。
肠道微生物群-脑轴
包括人类在内的所有动物,都是在与微生物群落(含细菌、古菌、真菌和病毒)的密切关联中进化而来的。这些微生物群落被称为微生物群,几乎遍布人体所有与外界接触的体表,而胃肠道内的群落(即肠道微生物群)是人体内微生物密度最高、数量最多的群体。
大量研究表明,肠道微生物群绝非人体中的 “被动乘客”,而是对免疫系统功能、新陈代谢乃至多个器官的发育都起着至关重要的作用。肠道细菌群落是动态变化的实体,其组成和活性会在人的一生中不断改变,既受宿主年龄、遗传等因素影响,也会响应饮食、药物等外界环境变化(其中饮食和药物的影响最为显著)。尽管肠道微生物群研究涵盖真菌、古菌和病毒等多个类群,但目前最丰富的研究数据来自细菌相关研究。
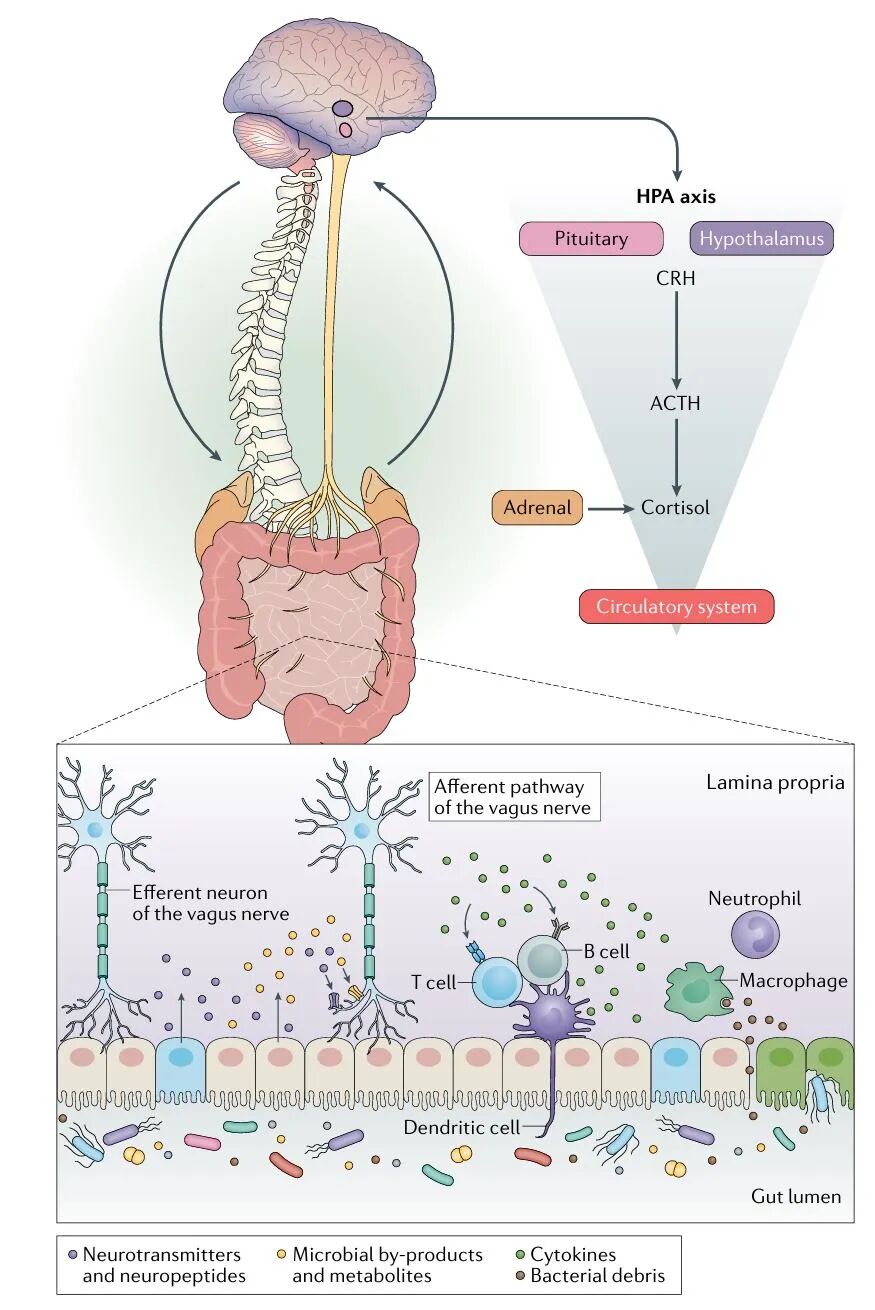
图1 肠道微生物群-脑轴
肠道微生物群与中枢神经系统通过肠-脑轴双向交流,主要经由自主神经(如迷走神经)、HPA轴、免疫系统和微生物代谢物(如GABA、5-HT、短链脂肪酸等)等途径实现。微生物产物可作用于肠神经系统、免疫细胞或经门静脉影响大脑;同时,应激激活HPA轴释放皮质醇,破坏肠道屏障、改变肠道环境,进而重塑菌群组成。这种双向互作在焦虑、抑郁、自闭症等神经精神疾病中尤为显著,而现有机制证据多源于可控的动物模型研究。
肠道与大脑之间的化学信号传导
肠道微生物群可通过与神经系统的化学交流(包括 “直接” 和 “间接” 信号传导,帮助调节宿主动物的稳态和行为。
肠道微生物群通过直接和间接化学信号影响中枢神经系统。
直接途径的典型代表是短链脂肪酸(SCFAs):由菌群发酵膳食纤维产生,可调节神经可塑性、表观遗传、基因表达及免疫;例如,丁酸钠能上调脑内BDNF表达并缓解小鼠抑郁样行为。
间接途径包括调控神经内分泌系统:微生物代谢物(如吲哚、SCFAs)刺激肠内分泌细胞分泌GLP-1和血清素(5-HT),影响食欲、迷走神经活动及情绪。无菌或抗生素处理小鼠的GLP-1和5-HT合成减少,而定植产芽孢菌可恢复色氨酸代谢和5-HT水平,提示这是哺乳动物保守的调控机制。
尽管肠道产生的5-HT不能穿过血脑屏障,但无菌小鼠海马中色氨酸和5-HT仍降低,暗示菌群可能通过间接机制(如前体供应或神经/免疫通路)影响脑内血清素系统。
然而,由于多数微生物代谢物入脑速率不明,其对CNS的直接作用常难以与免疫或神经通路区分。未来需整合宏基因组学、代谢组学与行为学数据以厘清化学信号在肠-脑轴中的确切角色。
肠道-大脑相互作用的神经通路
神经通路是肠道与大脑之间的物理连接,其中最主要的是迷走神经,该神经从脑干延伸至肠道,支配肠道和肠神经系统(ENS)。肠神经系统的发育和功能部分由肠道微生物群介导,但这一领域的研究仍相对匮乏。无菌小鼠结肠上皮的神经支配减少,而微生物定植可恢复这一表型;此外,肠道微生物群还能调节小鼠肠神经胶质细胞的发育,这类细胞对维持肠道稳态和神经元网络至关重要。
肠道微生物群通过化学信号(如短链脂肪酸、细菌细胞壁成分)调节肠神经系统功能,影响肠道蠕动,并经神经通路将信号传递至大脑。无菌小鼠的肠-脑交感通路过度激活,而补充产短链脂肪酸菌可抑制该通路,表明菌群对肠-脑神经活动具有调控作用。
迷走神经是肠-脑交流的核心通路:其末梢通过机械或化学感受器(如响应肠内分泌细胞释放的激素和微生物代谢物)感知肠道信号。研究显示,短链脂肪酸可激活肠内分泌细胞,进而触发迷走神经传入信号;而益生菌(如鼠李糖乳杆菌JB-1、罗伊氏乳杆菌)改善焦虑或自闭症样行为的作用,在迷走神经切断后完全消失,证明其效应依赖迷走神经传导。
鉴于迷走神经刺激术已用于治疗癫痫和抑郁症,靶向微生物-迷走神经轴可能为非侵入性干预神经精神疾病提供新策略。
肠道微生物群-大脑的免疫信号传导
中枢神经系统和肠道微生物群均直接影响免疫系统,且均受免疫系统的调控。肠道微生物群是调节外周免疫系统发育和功能的关键因素,同时也是大脑固有免疫细胞:小胶质细胞健康发育、成熟和激活的必要条件。与常规小鼠相比,无菌小鼠多个脑区的未成熟小胶质细胞数量增加(通过小胶质细胞形态分析和成熟转录标志物检测证实),经抗生素处理的小鼠也呈现类似结果。小胶质细胞介导的免疫编程似乎依赖于微生物代谢信号:给予无菌小鼠细菌来源的短链脂肪酸可恢复小胶质细胞的形态和功能。此外,复杂的微生物群或特定细菌类群可能是小胶质细胞正常功能和发育的必要条件。将复杂微生物群(而非有限的共生微生物子集)移植到无菌小鼠体内可修复其小胶质细胞缺陷。
肠道细菌对小胶质细胞的影响具有性别特异性和时间特异性:雄性无菌小鼠在胚胎期、雌性无菌小鼠在成年期,小胶质细胞基因表达和形态的变化更为显著。因此,未来旨在研究微生物群对脑细胞影响的研究,应将性别视为重要的生物学变量。关键的是,小胶质细胞功能异常已被证实与应激、行为障碍和神经退行性疾病相关,这表明肠道微生物群可能通过小胶质细胞介导的作用影响人类神经系统疾病。
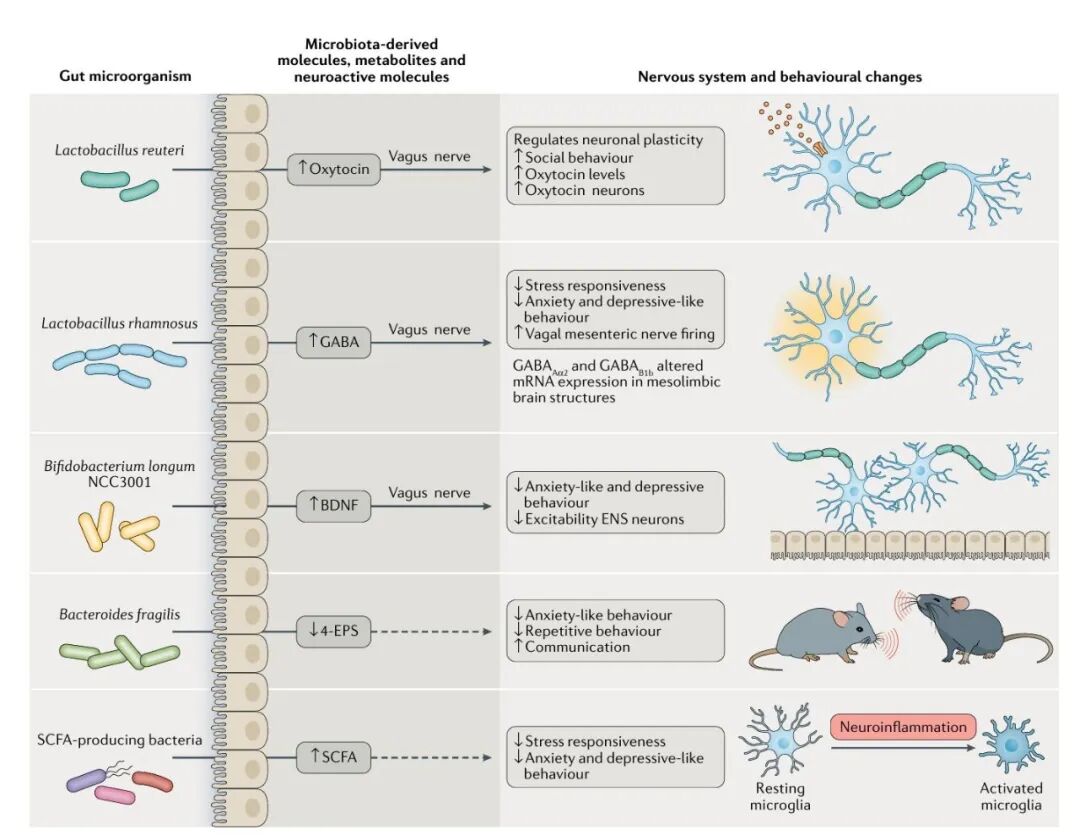
图2 微生物群及微生物源分子对宿主行为与神经系统功能的调控作用
肠道微生物不仅能诱导宿主产生神经递质和代谢物,还能自身合成多种神经活性分子,主要通过迷走神经信号和免疫调节两条路径影响大脑功能。
疾病中的肠道微生物群-脑轴
大量横断面研究表明,各类神经系统疾病患者的肠道微生物群组成与健康人群存在差异。此外,神经系统疾病的临床前模型不仅能重现肠道微生物群组成的改变,还证实人类肠道细菌可能会影响小鼠的行为和脑部病理状态;不过,这些表型背后的机制仍需进一步研究来明确。相关研究已鉴定出可改善疾病症状的潜在益生菌,同时也发现了会影响小鼠疾病进展的细菌及细菌因子,为后续开展人类相关研究提供了参考模板。
原标题:《脑声常谈总结|肠治久安?肠道微生物如何远程操控你的“喜怒哀乐”》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




