- +1
梦泽邀谈1|315曝光“三无”外泌体后,一位企业创始人的深度反思
转载需获取授权,请至后台留言
文章近5200字,预计阅读17分钟
梦泽邀谈|开栏语
在干细胞领域走了十余年,“细胞梦泽谈”自开设以来,有幸邀请了几位专家朋友分享他们的思考。从2025年10月第一篇发出至今,每一次对话都让我确信:一个人的视野终究有限,而行家的智慧值得被更多同行看见。
于是有了“梦泽邀谈”。
这个专栏的定位很简单:特邀生物医药领域、细胞产业链的专家学者、企业创始人、临床研究者、政策观察者,就行业热点问题进行撰文观察、深度分析与理性反思。不为流量,不为喧哗,只为给关注这个领域的同行者,提供一份有价值的参考。
首期邀请的是高博博士。315之后,外泌体被推上风口浪尖,我问他:能不能以一个业内人的身份,写写行业到底该往哪儿走?他答应了,于是有了这篇《315曝光的“三无”外泌体,到底冤枉了谁?一位企业创始人的深度反思》。
未来,还将不定期邀请更多业内专家,聊聊他们的观察与思考。
这,就是“梦泽邀谈”想做的事——把问题摊开,把路看清。
梦泽先生
2026年3月
【核心看点】
315曝光之夜,一位外泌体企业创始人的微信“炸”了。委屈过后,是清醒的反思:我们被误读了,但也确实被“捧杀”。从认知、监管到技术,三大维度拆解行业真问题;对标全球首款获批进展,追问“国内企业还有机会吗?”黎明前夜,与所有同行共勉。
315曝光,对外泌体行业而言,不是“寒冬”,而是一场迟到的“大考”。
【正文】
3月15日那晚,我的微信“炸”了。
同行发来央视315曝光“外泌体是三无产品”的链接,投资人在问“这个赛道还能不能看”,甚至家里的亲戚也转来视频,忧心忡忡地问:“你们搞的那个东西,是不是骗人的?”
那一夜,五味杂陈。作为在这个领域从科研到产业深耕了十年、从复旦神经生物学实验室走到创业一线的企业创始人,委屈吗?有一点。
但冷静下来后,我更清醒地意识到:这场曝光,对外泌体行业而言,不是“寒冬”,而是一场迟到的“大考”。
今天,我想以一个企业创始人和一线研发者的身份,和各位同行、关注外泌体的朋友们,聊聊315之后,我们这个行业到底该往哪儿走。
一、认知与市场:行业发展的第一道坎
——我们被误读了,但也确实被“捧杀”了
315晚会的曝光,让“外泌体是‘三无’产品”的印象刻在了大众心中。这是行业当下最直接的挑战。
但作为从业者,我们需要冷静解读:央视的结论并非否定外泌体技术本身的科学价值,而是剑指目前市场上无合规批准、无质量标准、无正规来源的“三无”流通产品。
一个必须正视的现实是:截至目前,全球范围内尚未有一款外泌体药品完成完整审批并正式上市。这就意味着,所有先行流入消费市场的外泌体相关产品,都缺乏官方的安全性和有效性背书。
而大众对健康与美的迫切需求,反被不法商家利用,将外泌体异化为“抗衰神针”“疾病调理剂”等营销噱头。这种过度包装,不仅扰乱了市场秩序,更让消费者对这项严肃的技术产生了误解与抵触。
与此同时,资本的快速涌入虽助推了行业热度,却也带来了一定的浮躁之气。部分企业并未沉下心做技术研发,反而急于推出概念产品抢占市场,进一步加剧了市场的混乱,让真正潜心研究的企业陷入“劣币驱逐良币”的尴尬。
但换个角度看,乱象丛生恰恰印证了市场对优质外泌体产品的真实渴求。我们在研发一线深耕这些年,最深的体会是:医美、慢病修复等领域的需求是真实存在的,甚至呈现出百倍溢价。
315的曝光,恰恰成为行业“祛魅归真”的契机——它清退虚假炒作,也为正规技术和产品让出了市场空间。
对那些被误导的消费者,我想说:外泌体技术本身值得期待,但请给正规产品一点时间,也给合规企业一点耐心。
二、监管与标准:行业规范化的核心缺失
——有“政策”无“细则”,企业不知路在何方
如果说市场认知偏差是外部阻碍,那么权威的国家标准与可操作的监管细则双重缺失则是制约外泌体行业发展的内在痛点。当然,我们也要看到,监管的逐步完善,正是行业走向成熟的核心标志。
近年来,国家层面已逐步明晰外泌体的行业定位:
2024年国家药监局明确外泌体不作为普通的医疗器械或化妆品原料管理;
2025年6月CDE发布《先进治疗药品的范围、归类和释义(征求意见稿)》,首次以官方文件形式将其明确归入“先进治疗药品”的药品属性进行管理;
国务院第818号、828号文件也为生物医学新技术的临床转化和支付保障指明了方向。
但政策框架的搭建,并不意味着监管细则的完善。
目前,行业仍缺乏统一的国家标准和规范:从细胞来源筛选、制备工艺确定,到质量属性研究、质检方法建立,再到非临床研究和临床试验注册路径,均无细致、明确的要求。
这直接导致研发企业陷入“有法可依、无细则可循”的困境——即便拥有核心技术,也常常在如何满足审评要求、推进产品注册的路径上感到迷茫。
以我们一线研发的亲身经历为例,在外泌体分离纯化、药物装载工艺上,行业里不少团队都积累了一定经验,但在合规申报时,依然要花大量精力去“猜”监管的尺度。
值得期待的是,行业标准建设正在加速推进。目前已有近30项外泌体相关团体标准发布(详见表1),涵盖提取、制备、质检等多个环节,国家标准《纳米技术 外泌体形貌和尺寸测量 原子力显微术》也即将实施。
表1 全国外泌体团体标准(数据来源:全国团体标准信息平台)
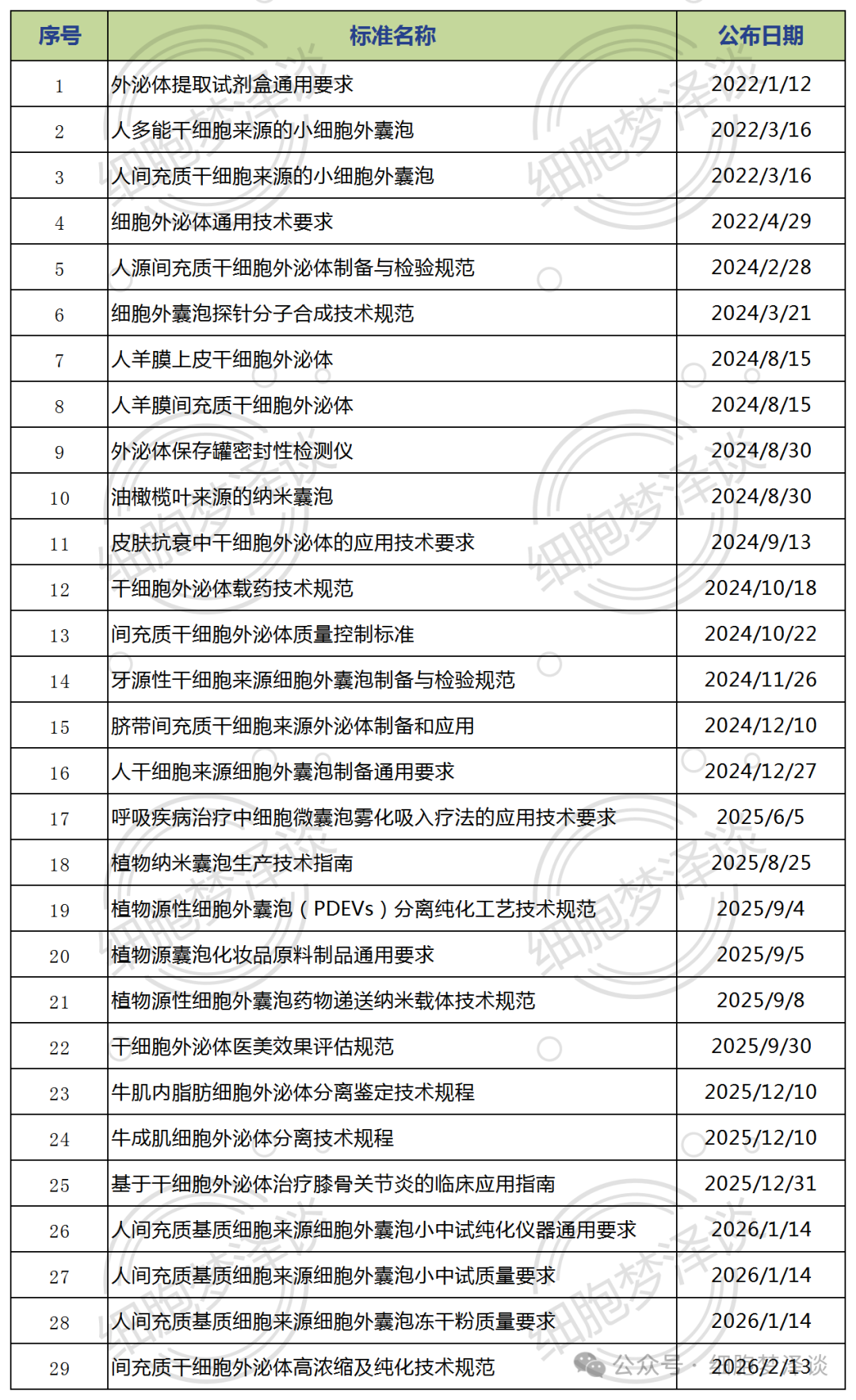
注:本表数据截至2026年3月
315曝光后,监管进一步收紧,严禁违规宣传。可以说,行业正从“野蛮生长”向“规范发展”艰难但坚定地转型。
三、技术与研发:行业进阶的核心壁垒
——从“能做出来”到“稳定量产”,中间隔着无数个“坑”
作为一项前沿生物科技,技术难题是外泌体从实验室走向产业化的最大壁垒。这一点,作为常年泡在实验室和GMP车间的一线研发人员,我感触尤深。
从种子细胞的选择到最终产品的制剂,外泌体的研发生产全流程,都充满了亟待攻克的技术“硬骨头”。
机制之谜:我们知道的,还远远不够
首先必须承认,外泌体的作用机制尚未完全阐明,其在体内的分布、靶向、摄取、代谢及潜在长期风险仍有诸多未知,这为临床转化带来了不确定性。
但全球科研力量正持续深耕,从新型分离纯化设备、多维度质控方法的开发,到工程化外泌体、靶向载药技术的探索,每一项技术突破,都可能为行业打开新的发展空间。
制备之难:从“实验室手工”到“工厂化生产”
在制备与纯化环节,如何实现大规模、低成本、高纯度的分离纯化,是产业化的首要拦路虎。
我们早期也用过传统的超速离心法,虽然被视为“金标准”,但根本无法放大。后来转向切向流过滤与层析联用的工艺路线,光是摸索膜材、压力、流速这些参数,就耗掉了团队整整两年时间。那两年,我和团队几乎每天都在“推倒重来”中度过,但每次看到纯度数据提升0.5%,都觉得值了。
同时,外泌体的细胞来源多样,干细胞、免疫细胞、植物细胞等不同来源的外泌体,其功能与安全性特征差异显著。如何筛选出安全、稳定、高活性的工程化细胞株,并建立标准化的培养工艺,是企业必须攻克的根基性问题。
质检之困:测出来的数据,自己都不敢信
质检与质控同样是技术痛点。我曾和几位同行交流,大家苦笑:同一批外泌体,送到三家检测机构,拿回三份截然不同的报告。到底信谁的?这不是夸张,是很多同行私下交流时的真实感慨。
这不是技术问题,而是行业没有“度量衡”的缩影。外泌体是纳米尺度的复杂生物实体,其表征需要从形态、粒径、标志蛋白、核酸内容物及生物活性等多维度进行。
从粒径分布、颗粒浓度到宿主蛋白残留、内毒素,从特定生物学功能评价到病毒安全性筛查,建立覆盖全流程的质量控制体系,是确保产品安全有效、质量可控的基石。
载药之惑:效率与完整性,能否两全?
在药物装载与剂型开发上,外泌体虽被认为是理想的药物载体——能穿过血脑屏障、免疫原性低、可装载多种药物,但目前的载药技术仍普遍存在效率低、易损伤外泌体完整性的问题。
我们在做药物装载工艺开发时,共孵育、电穿孔、超声法都试过,每一种都有“按下葫芦浮起瓢”的尴尬:载药率上去了,外泌体破了;外泌体保住了,载药率下来了。
此外,外泌体产品的制剂稳定性也是一大挑战,目前多为需-80℃超低温储存的液体制剂,如何开发出便于运输、储存且能长期保持活性的冻干或其他剂型,是决定其能否成为“药品”走进千家万户的关键。
四、前景可期:数据印证黄金发展期
——全球首款获批在即,国内企业还有机会吗?
尽管挑战重重,但从市场规模、临床进展、政策走向等多维度数据来看,一个千亿级的生物医药新赛道正加速成型,我们或许正迎来政策加码、临床突破、产业规范的黄金发展期。
国际上的好消息,给行业打了一剂强心针。
美国Capricor Therapeutics的外泌体疗法Deramiocel迎来关键节点,其III期临床数据显示能显著延缓杜氏肌营养不良症患者的心功能和肢体功能衰退,FDA已恢复其上市审评,2026年8月或将成为全球首款获批的外泌体细胞疗法。
这个消息对我们行业是极大的提振——它证明:这条路虽然难,但走得通。
INTENT公司的PEP生物制剂也获得FDA快速通道认定,用于治疗糖尿病足溃疡。
国内政策环境,正在从“模糊”走向“清晰”。
回到国内,国家对生物经济的大力支持为行业发展提供了坚实的政策保障。从外泌体技术被纳入《“十四五”生物经济发展规划》的国家级战略布局,到CDE将其明确归入“先进治疗药品”范畴,监管路径日益清晰。
315曝光后,监管并未“一刀切”式打压,而是精准打击非法产品,这恰恰为正规科研和临床转化扫清了市场干扰,是“良币驱逐劣币”的开端。
技术突破,正在把“不可能”变成“可能”。
在制备纯化上,工业界正推动切向流过滤与层析联用的组合工艺成为GMP主流方法;在质检质控上,纳米流式检测仪等新型设备的普及,正推动质控从定性走向定量、从混乱走向精准;在载药技术上,通过基因编辑改造供体细胞,直接产生携带目标分子或靶向肽的工程化外泌体,正成为突破载药效率瓶颈的主流方向。
这些方向,也正是国内很多同行正在全力投入的领域。
所以,国内企业还有机会吗?
我的回答是:有,但窗口期正在收窄。谁能率先跑通合规路径,用扎实的临床数据证明产品的安全有效,谁就更有可能拿到下一阶段的入场券。
五、破局之路:多方携手,共筑行业未来
——给学界、业界、监管的三点建议
看到前景,更要看清前路。外泌体行业的发展,绝非单一主体能够完成,需要学术界、产业界、监管方三方携手,各司其职,形成合力,共同在挑战中开新局。
接下来,我想从三个角度谈谈,这条路具体该怎么走。
给学术界的建议:坐稳冷板凳,把机制搞清楚
核心是持续深耕基础研究,阐明外泌体的生成、摄取、体内命运等基本机制,攻克细胞工程改造、大规模制备、精准质控等关键技术,同时加强基础研究与临床需求的对接,加速成果转化。
给产业界的建议:坚持长期主义,用数据说话
作为企业负责人,我常和同行们交流一个观点:我们做的不是快消品,是可能进入人体的药品,每一批产品、每一个数据,都要对得起“合规”二字。
企业应以“安全、有效、可及”为核心,投入资源打造标准化的生产工艺和全链条的质量体系,积极参与行业标准讨论与制定,找准赛道,聚焦细分领域,以扎实的临床数据说话,而非沉迷于概念炒作。
给监管部门的建议:细则先行,让企业有路可走
作为一线从业者,我们由衷期待监管部门能紧跟科技发展步伐,加快完善从药学研究、非临床评价到临床试验的监管细则和技术指导原则,搭建清晰、可预期的产品注册路径。
同时,持续加强市场监管,严厉打击“三无”产品,为合规企业营造良性有序的市场环境。
六、结语:曙光在前,与所有同行共勉
——外泌体的黎明,或许会迟到,但绝不会缺席
315晚会的曝光,绝非外泌体行业的“寒冬”,而是行业规范化、高质量发展的起点。
它让行业清醒地认识到自身的问题,也让大众对这项技术有了更理性的认知。
外泌体作为生物医药领域的下一代核心技术,其发展在我看来,是一场需要耐心和定力的持久战。
这个曾被乱象遮蔽的赛道,终将走出“李鬼”的阴影。而我们这群还在坚守的创业者,需要的不仅是耐心,更是 “明知山有虎,偏向虎山行”的勇气,和“板凳要坐十年冷”的定力。
外泌体的黎明,或许会迟到,但绝不会缺席。
与所有同行共勉。
【作者简介】
苏州志恒生物董事长&创始人。
本科毕业于西安交通大学生物工程专业,硕士毕业于武汉大学微生物专业,博士毕业于复旦大学神经生物学专业。
2016至今担任志恒生物生物技术有限公司(前身上海宇玫博生物科技有限公司)首席运营官,负责外泌体产品的开发和工艺研发,包括分离纯化、检测鉴定、载体标记、药物装载等工艺开发。
编辑、审校:梦泽
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




