- +1
厦门大学袁晶课题组Current Biology:疟原虫极简基体如何在极端机械应力下保持完整性?

生命科学
Life science
纤毛(Cilia)与鞭毛(Flagella)的剧烈摆动会产生物理撕扯力。为了抵抗机械应力,经典模式生物的基体(Basal body)演化出由微管三联体和中央车轮结构(Cartwheel)交织而成的坚固内部骨架。疟原虫(Plasmodium)是引发疟疾传染病的病原体,其有性生殖中产生有鞭毛能摆动的精子——雄配子。然而,较之模式生物,疟原虫鞭毛轴丝相关过程非常独特:急速组装+快速摆动+基体朝外。其在演化中几乎丢失了所有经典基体结构,趋向极简。结构极简的基体如何能在疟原虫鞭毛剧烈摆动时避免解体?近日,厦门大学袁晶教授团队在Cell Press细胞出版社旗下期刊Current Biology上发表题为“Mechanoregulation of basal body integrity during Plasmodium exflagellation”的研究成果。该研究揭示了疟原虫在雄配子发生时,如何依赖新鉴定的蛋白Calcifer维持极简基体在极端机械应力下的完整性。
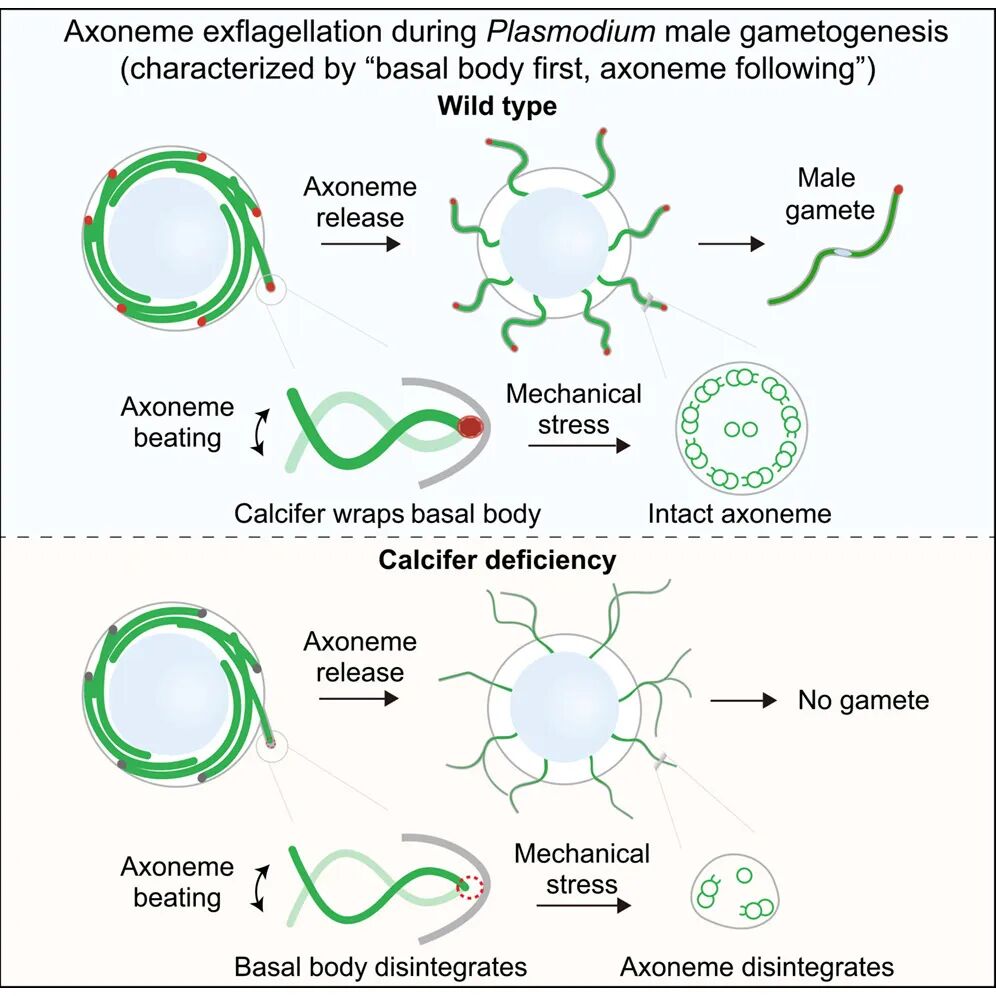
图1: 本研究的视觉摘要,涵盖Calcifer保护极简基体抵抗机械应力的机制模型和核心结论
论文概述
1. 疟原虫基体面临的散架危机:极简架构与极速释放
疟原虫的传播需经历由脊椎动物宿主向按蚊媒介的转换。当疟原虫随血液被吸食进按蚊中肠后,雄配子体(Male gametocyte)被激活,开启雄配子发生。面对按蚊消化系统与免疫机制的双重生存压力,雄配子体启动名为出丝(Exflagellation)的极速逃逸机制——12-15分钟内,在核膜上从头组装出8条轴丝(Axoneme),然后直接顶起母体细胞质膜向外推挤突出,最终分离形成8个雄配子。游离的雄配子以最短的时间与雌配子完成受精,形成能穿透消化道上皮细胞的动合子(Ookinete),实现跨组织屏障的物理逃逸。
出丝过程不仅时间紧迫,更对基体提出了极端的物理挑战:首先是极端的机械应力。在经典模式生物的纤毛或鞭毛发生过程中,基体(轴丝负末端)通常锚定在细胞膜下方,轴丝正末端向外突出。而疟原虫的轴丝在组装阶段,基体锚定在核膜上,以此为模板向细胞质延伸出轴丝;一旦轴丝完成组装,基体与核膜解偶联并邻近细胞边缘,向外推挤质膜以驱动轴丝的最终突出释放,其突进速度高达294-1254 μm/h(远超衣藻轴丝向胞外生长的速度9-24 μm/h及哺乳动物纤毛的0.1-2.6 μm/h)。这种罕见的“基体在前,轴丝在后”的向外伸出方式使得基体不仅要承受轴丝高速摆动产生的机械力,还要正面对抗细胞质膜的阻力。
其次是自身结构的极简性。在演化过程中,疟原虫基体丢失了经典九重对称三联体微管和车轮结构,基因组缺少多个保守基体相关基因,依靠脆弱的单微管支撑。面对极速释放和剧烈摆动产生的机械力,这个缺乏内部支架的极简基体如何避免分崩离析?
2. 特殊基体蛋白Calcifer的鉴定及其滞后定位
研究团队发现一个未被表征但在疟原虫中保守的蛋白——Calcifer。基因敲除实验表明,缺失该蛋白的疟原虫不能形成出丝点(Exflagellation center),即无法产生有受精能力的雄配子,彻底阻断了其按蚊传播。
利用超微结构膨胀显微成像(U-ExM)与活细胞成像,Calcifer展现出独特的“滞后”定位模式:传统基体蛋白(如Centrin1、SAS4和GCP3)在基体组装时即被招募。而Calcifer在轴丝组装初期(雄配子发生前4分钟)依然弥散在细胞质,直到轴丝组装基本完成(第4-6分钟)才富集于基体,并在轴丝即将释放时完全定位于基体。
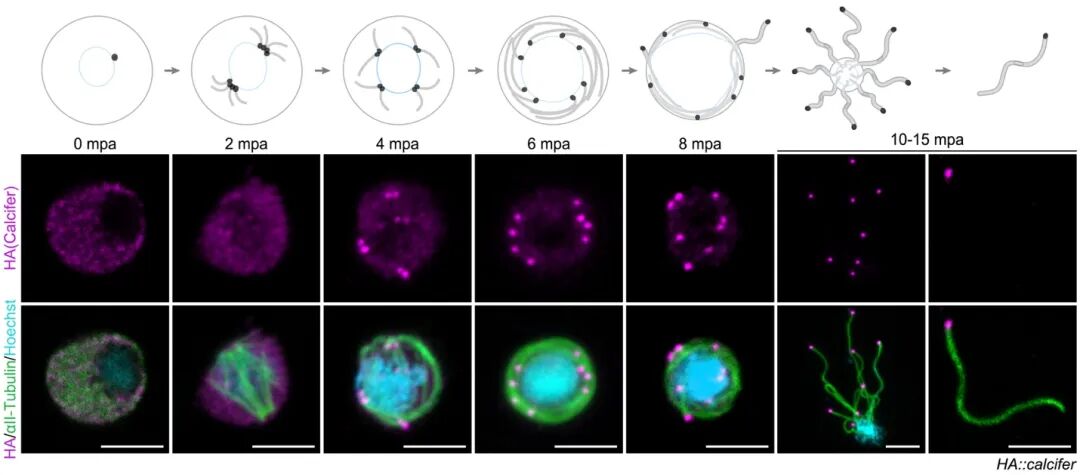
图2: 免疫荧光揭示Calcifer在雄配子发生时从胞质均匀分布变为轴丝负末端聚集。
3. 轴丝解体与分支鞭毛表型
作为基体蛋白的Calcifer是否调控鞭毛轴丝的组装?超微结构膨胀显微成像和透射电镜结果证实,Calcifer缺失的雄配子体在激活后依然能组装出与野生型无明显差别的“9+2”微管结构轴丝,表明Calcifer不参与鞭毛轴丝的组装。
然而,一旦轴丝释放出母体细胞,基体和轴丝结构瞬间解体。透射电镜结果显示缺失Calcifer后,原本应紧密排列的9组二联体微管出现结构性解离;对基体的标志蛋白进行免疫荧光成像,显示此时预期定位于轴丝负末端的基体蛋白也发生结构性崩塌。
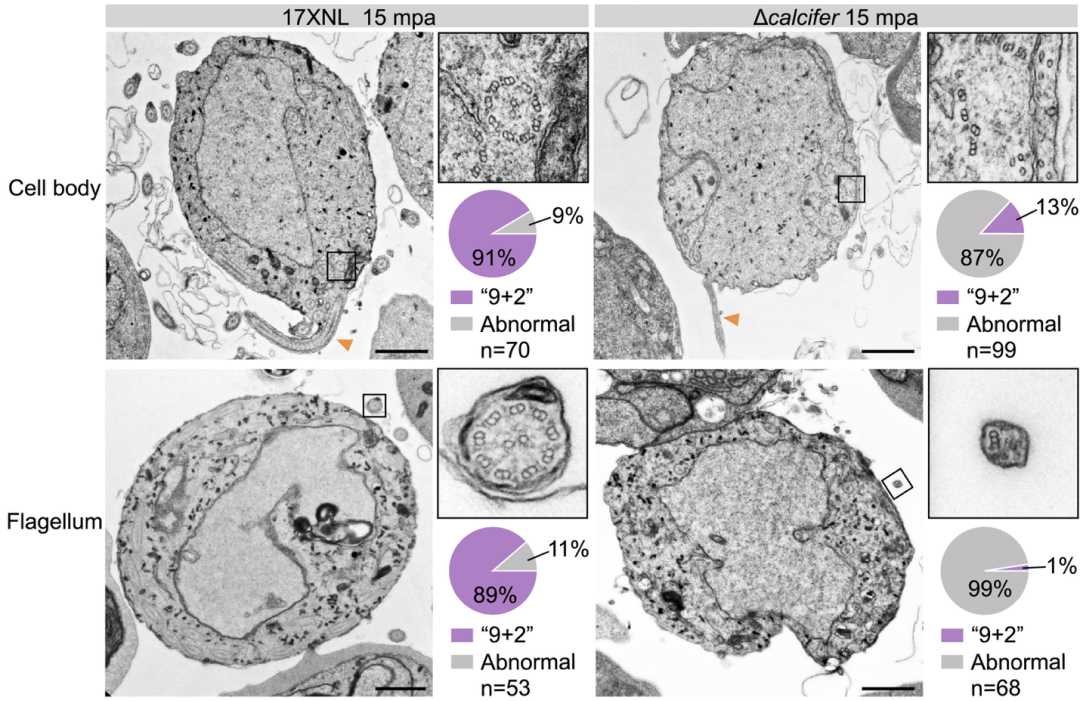
图3: Calcifer缺失的雄配子体在出丝时轴丝“9+2”微管结构散架
这种结构瓦解不仅让轴丝丧失了“9+2”微管结构,还让鞭毛出现“分支”表型。活细胞成像进一步观察到Calcifer缺失后,解体的轴丝摆动能力明显减弱。
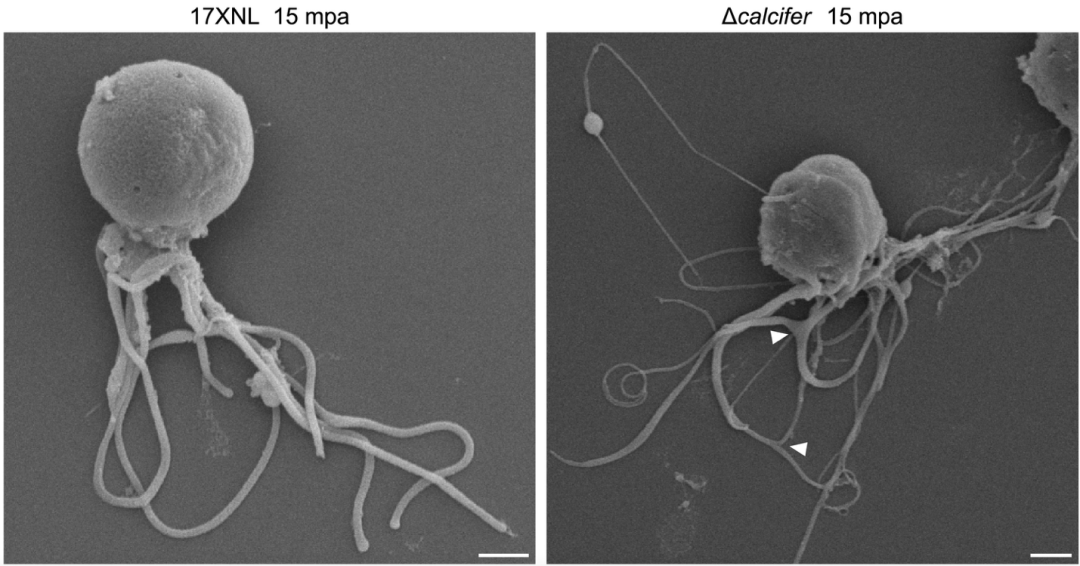
图4: Calcifer缺失后鞭毛出现分叉(白箭头),远离胞体侧的鞭毛变得纤细
4. 体内外力学验证与鞘状包裹加固机制
为证明结构解体源于纯物理机械力,团队进行了双重验证:
体外剪切力模拟:使用去垢剂脱氧胆酸钠(SDC)将完成组装但未释放的轴丝从激活后的雄配子体分离出来,使用涡旋振荡器对其施加流体剪切力。结果显示,野生型的基体和轴丝负末端在震荡后结构保持完好;而缺乏Calcifer的基体则解体,且轴丝负末端出现分叉。
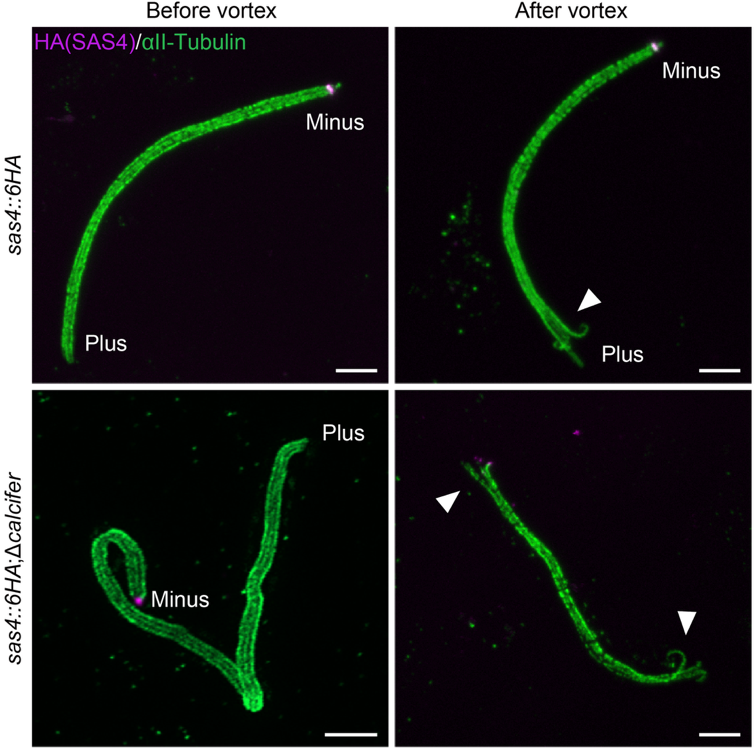
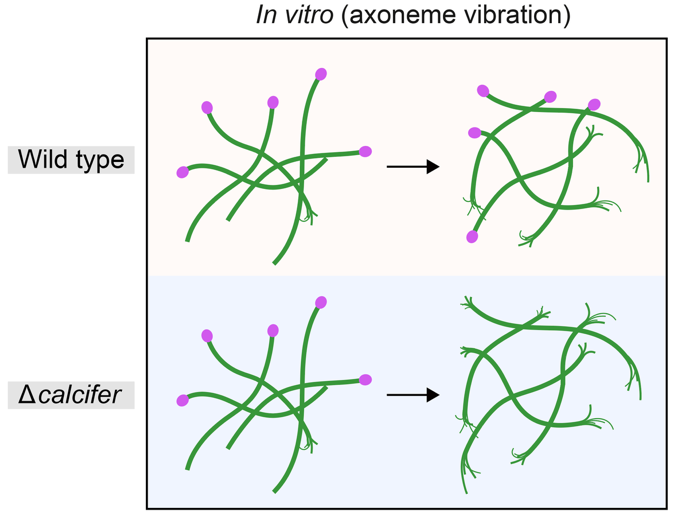
图5: 体外涡旋振荡后,Calcifer缺失的轴丝的两末端均极易分叉
体内动力马达敲除:敲除驱动轴丝摆动的动力蛋白基因dhc1后,轴丝彻底失去摆动能力且只能缓缓地从母体细胞释放。通过超微结构膨胀显微成像和透射电镜观察到,在轴丝无法摆动的情况下即使缺乏Calcifer,轴丝仍保持“9+2”微管结构,成功挽救了解体表型。
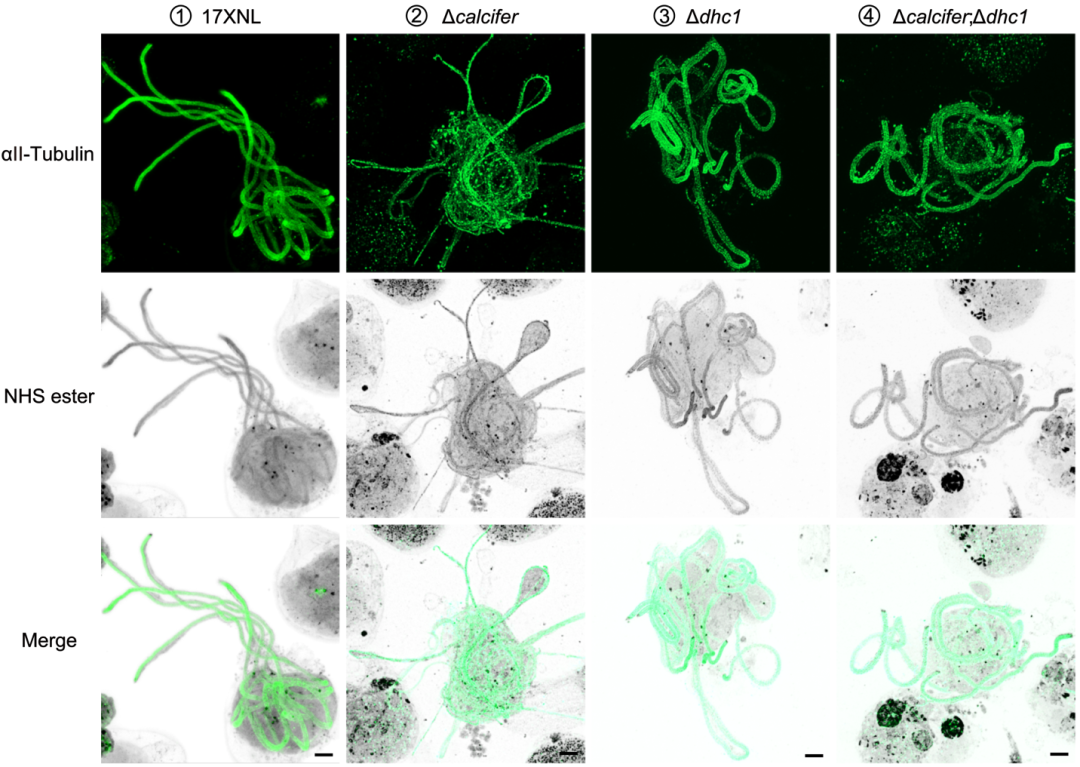
图6: 超微结构膨胀显微成像结果说明敲除dhc1(消除轴丝摆动)能挽救轴丝解体表型
最终,团队通过荧光信号3D拓扑重建,揭示了Calcifer在基体上形成一个体积大于内部核心蛋白的鞘状包裹结构,牢固锁定基体的核心组件与轴丝负末端微管。研究者推测通过这种物理包裹加固,Calcifer弥补了极简基体因缺乏内部三联体微管和车轮结构而导致的先天脆弱性,赋予了极简基体抵抗高强度机械应力的能力。
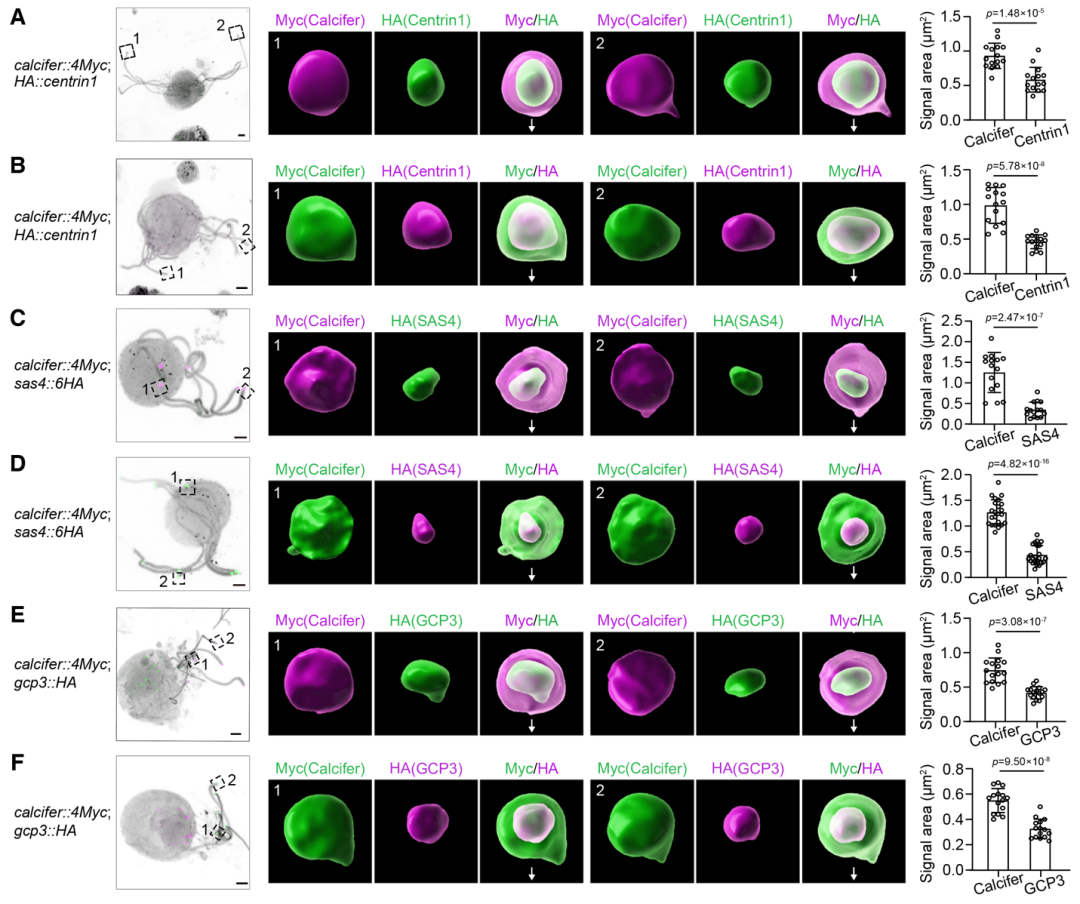
图7: 3D拓扑重建显示Calcifer在物理空间上包裹住基体经典蛋白(Centrin1、SAS4和GCP3)
作者专访
Cell Press细胞出版社特别邀请袁晶教授、关杰鹏博士进行了专访,为大家进一步详细解读。
CellPress:
这项研究的创新性和意义是什么?
袁晶教授:
创新性在于打破基体蛋白主要参与成核与组装的传统认知。Calcifer是极少数仅发挥结构稳定而不参与基体复制和轴丝组装的基体蛋白。在研究意义上,该发现不仅为阻断疟疾传播提供了全新的干预靶点,更拓展了对基体功能多样性的理解,为真核细胞应对极端物理挑战提供了进化适应的新范例。
CellPress:
为什么疟原虫雄配子发生时,要采用“基体在前,轴丝在后”的释放模式?
关杰鹏博士:
本质上是生命在极端环境下追求绝对速度的演化折中。疟原虫进入按蚊消化道后,面临宿主消化和免疫系统的攻击。如果像常规鞭毛发生那样,依靠鞭毛内运输缓慢向胞外组装出轴丝,疟原虫可能会被宿主消灭。在极短生存窗口期下,疟原虫采取了特殊策略:在细胞内部先行完成轴丝的预组装,并以带有Calcifer保护、物理强度更高的基体作为物理前导,直接顶起母体细胞膜向外突出。体外涡旋实验也表明了轴丝正末端比携带有基体的负末端脆弱,因此“基体在前”是保护轴丝免受极端机械力损伤的较优方案。
CellPress:
Calcifer表现出的这种“滞后定位”有什么生物学意义?
袁晶教授:
本质是为了维持基体的结构灵活性。实验证明Calcifer不参与轴丝组装,其唯一功能是后期的物理加固。若这种提供机械保护的蛋白过早入场,可能带来空间位阻,干扰基体的复制与轴丝的初始组装。
CellPress:
缺失Calcifer导致的“分支鞭毛”现象,其背后的物理力学逻辑是什么?
袁晶教授:
轴丝的摆动依赖于马达蛋白在微管间的相对滑动。要将这种微观滑动转化为宏观弯曲,所有微管的根部必须在基体端被牢固锚定。在缺乏Calcifer这个包裹鞘时,马达蛋白一旦启动,未受物理束缚的微管在剧烈的相对滑动中会直接破坏脆弱的基体。原本紧密锚定的微管阵列就像失去物理束缚的钢缆一样发生结构性破裂,各自向外随机挤压细胞质膜,从而形成了宏观的鞭毛分支。
CellPress:
疟原虫这种“极简基体”与“打补丁”式的加固机制,在演化视角上有何启示?
关杰鹏博士:
该机制诠释了极简主义与补偿性适应的生存策略。在极致时效的自然选择压力下,疟原虫演化出的极速传代模式,伴随着经典基体骨架的物理性退化。然而物理法则不可逾越,结构精简容易导致力学脆弱。面对生存红线,疟原虫演化出了功能专一、时空定位精准的Calcifer来代偿这种先天缺陷。这启示我们,生命的适应并不总是意味着系统复杂性的叠加,通过局部的极简换取整体效率,再辅以精准的补偿性保护,同样是自然选择淬炼出的高效生存之道。

作者介绍

袁晶
教授
通讯作者:袁晶,厦门大学生命科学学院教授,国家自然科学基金优秀青年科学基金获得者。2002年及2007年分别获得中国农业大学学士与博士学位;2007年至2012年于美国国立卫生研究院(NIH)进行博士后研究。长期深耕疟原虫双宿主适应性机制及前沿基因修饰工具开发,研究成果多次以通讯作者发表于Science, Nature Communications, PNAS, Science Advances, Current Biology, EMBO Journal等学术期刊。



共同第一作者及重要贡献作者:厦门大学博士生关杰鹏和龚玉姣为本论文的共同第一作者,硕士生梁文琪为重要贡献作者。三位同学在基因编辑、超微成像、体内外力学机制的独立验证等实验中做出了关键贡献。
相关论文信息
论文原文刊载于Cell Press细胞出版社
旗下期刊Current Biology
▌论文标题:
Mechanoregulation of basal body integrity during Plasmodium exflagellation
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S0960982226003878
▌DOI:
https://doi.org/10.1016/j.cub.2026.03.068
原标题:《厦门大学袁晶课题组Current Biology:疟原虫极简基体如何在极端机械应力下保持完整性? | Cell Press对话科学家》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




