- +1
同病不同命:两位患者的不同结局
冯媛、雷云霞 医学界心血管频道

系统性红斑狼疮(SLE)相关PAH(SLE-PAH)已经成为风湿科医师必须面临的挑战,且是继神经精神性狼疮、狼疮性肾炎之后,基础病脏器损伤导致SLE患者死亡的重要原因之一。SLE同时又是一种异质性很强的疾病,甚至相同的并发症也会有不同的表现和预后,下面的两个病例会带给我们一些思考和启示。
病例一:
患者,女,29岁。因“气促8月,加重伴水肿2月”于2017年3月入住我科。
(上滑查看更多信息)
2016年7月(孕7月)患者出现乏力、活动后气促,体力逐渐下降,间中有干咳,不能平卧,未经特殊处理,约10天后自行缓解;
2016年10月再次出现乏力伴活动后气促,上4层楼梯可出现气促,但症状较轻,未予重视。症状逐渐加重,12月活动后气促明显加重,步行300米或上2层楼后可出现,伴头晕、腹胀及双下肢水肿,遂至当地医院检查提示多浆膜腔积液,ANA(+)、抗SSA(+)、抗SSB(+);低补体血症;血尿及蛋白尿;肾穿刺活检提示II期膜性肾病(IgG2+、IgM+、C3++、C1q+),UCG提示中度肺动脉高压(63mmHg),诊断:SLE、LN、PAH。
予足量激素+LEF 10 mg/qd辅以营养心肌、利尿消肿等治疗,症状有所好转出院。但出院后觉头晕再次加重,为进一步诊治入我院,病人近来脱发增多,夜间出汗较多,精神、胃纳尚可、大便干、小便量少,可见少量泡沫。体重无明显变化。
既往史:2014年夏有发作双膝关节疼痛,无红肿,未处理数月后自行缓解,后未再发作;2017年2月有产后抑郁症病史,予“帕罗西汀片”治疗后精神症状消失。
查体:T:36℃,P:120次/分,R:22次/分,Bp:88/52 mmHg,Wt:43Kg。双肺呼吸音粗、右下肺呼吸音明显减弱、左下肺可及少量湿性啰音、未闻及胸膜摩擦音、三尖瓣听诊区闻及收缩期3/6级吹风样杂音、P2亢进、心率120次/分、律齐、未闻及心包摩擦音。双手雷诺现象+、双下肢可见网状青斑、双手及双足可见血管炎样皮疹。
辅助检查:
BUA 601 μmol/L;TBIL 34.1 μmol/L,AST 51 U/L;尿蛋白5.0 g/L;RBC 10.10/μL;ERY 4+;ESR 7 mm/h;D-DI 4930 μg/L;
血气分析:PH 7.436、PCO2 22.8mmHg、PO2 91.5 mmHg;SpO2 96.3%;C3 770 mg/L、C4 125 mg/L;IgG 23.70 g/L;ANA+1:3200,颗粒型;抗SSA+、抗SSB+、抗ds-DNA 34.4 IU/mL;24小时尿蛋白定量1332 mg;NT-ProBNP(E)15697.0 pg/mL;ANCA、ACA阴性。
ECG:窦性心动过速、不完全性右束支传导阻滞,疑右心室肥厚。
6MWT:134米,因心悸无法耐受停止;
Borg呼吸困难指数:7分;WHO心功能分级:Ⅲ级;
UCG:三尖瓣返流、彩束面积19.9 cm2、肺动脉收缩压:75 mmHg;肺动脉瓣返流、彩束面积4.1 cm2、肺动脉平均压:41 mmHg;右房右室明显扩大、右室壁增厚达5.1 mm;少量心包积液;
右心导管:右心房压力(RAP)13 mmHg、肺动脉压力(PAP)收缩压59mmHg、平均压41 mmHg、混合静脉血氧饱和度(SvO2)49、肺动脉楔压(PAWP)7 mmHg、心输出量(CO)1.64升/分、肺血管阻力(PVR)18 wood。吸入万他维5分钟后肺动脉收缩压54 mmHg
病情变化:2017年3月30日开始出现认知障碍,不认识自己的母亲,焦虑,烦躁,自己拍打脸部,并出现咬人、打人暴力行为,言语含糊,情绪难以自控,并有咬伤自己、声称要跳楼等自虐、自杀倾向。
腰穿提示颅内压升高310 mmH2O脑脊液病原学检查阴性;脑电图提示中度异常未见异常癫痫波;头颅MR+MRA未见异常。
这个患者的诊断?下一步应该怎么做?
SLE诊断明确,并逐渐出现狼疮性肾炎、狼疮相关性的肺动脉高压及神经精神性狼疮,SLEDAI(狼疮活动度)评分24(精神症状8分+血管炎8分+蛋白尿4分+补体下降2分+抗ds-DNA升高2分)。

UCG的变化:心包积液逐渐消失、右心室/右心房大小由扩大逐渐恢复正常、sPAP由75mmHg逐渐降至正常(75→70→42→32→33)、mPAP由41mmHg降至15mmHg、TAPSE由13增加至20、右室FAC由23%增加至40%。
患者预后良好:精神症状完全消失;维持心功能Ⅱ级;尿蛋白转阴;血管炎皮疹消失;雷诺现象明显改善,未见发作;
病例二:
患者,女,35岁;因“确诊SLE 9年,纳差、视物模糊、胸闷1月”于2017年8月入住我科。
(上滑查看更多信息)
9年前患者因“发热、胸闷、气短10天”查ANA+1:10000,均质型、抗U1RNP(+)、抗SSA(+)、抗HIS(+),另伴发面部红斑,多浆膜腔积液,关节痛,脱发,贫血,诊断SLE;给予足量激素+HCQ+CTX 1.0 g/QM (累积量为22 g)治疗,多次自行停药,2013年7月激素减至Pred 5 mg/qd,之后患者未再返院复诊,自行调整用药。
目前治疗方案为Pred 10 mg/qd+HCQ 0.2/qd;近半年出现记忆力及计算力下降;1月前患者出现胃纳差、视物模糊、胸闷;患者神志尚清,精神可,有脱发,面部间断出现皮疹,大小便正常,体重无明显变化。
查体:T:36.2℃、P:72次/分、R:20次/分、Bp:145/85 mmHg。
神清、反应差、对答不切题、计算力下降、四肢肌力正常、病理征阴性;慢性病面容、双眼睑水肿、浅表淋巴结未及肿大。双肺呼吸音清、未闻及干湿啰音。心率72次/分、心律齐、P2>A2、未闻及杂音。面部可见大小不一红斑丘疹、雷诺现象+。
辅助检查:
血象、生化及肝功能正常,BUA 313 μmol/L;尿蛋白-;ESR 31 mm/h;D-DI 980 μg/L;
血气分析:PH 7.464、PCO2 37.0 mmHg、PO2 130 mmHg;SpO2 98.5%;C3 645 mg/L、C4 112 mg/L;IgG 27.60 g/L;CRP 9.30 mg/L;ANA+1:1000,颗粒型;抗SM+,抗U1RNP+、抗HIS+、抗ds-DNA 26.3 IU/mL;NT-ProBNP(E)1729 pg/mL;ANCA,ACA阴性。
脑脊液检查未见异常,脑压正常;胸片:心影增大、肺动脉膨隆、考虑肺动脉高压;心电图:不完全性右束支传导阻滞、ST-T改变、疑右心室肥厚;6MWT:365米;Borg呼吸困难指数:3分;WHO心功能分级:Ⅱ级;
UCG:三尖瓣返流、彩束面积3.1 cm2、肺动脉收缩压:89 mmHg;右房右室稍扩大、无心包积液;头颅MR+MRA示:双侧额、顶、枕叶、丘脑、小脑半球、脑室旁白质区见多发弥漫性异常信号,考虑狼疮性脑病,头颅MRA未见异常;头颅ECT:双侧大脑皮质、双侧丘脑,左侧纹状体后部多发局限性血流灌注减低,结合CT所示多发大脑白质及双侧小脑半球低密度、蛛网膜下腔出血,考虑多发脑损伤改变;眼科检查提示视野缺损。
这个患者的诊断?下一步应该怎么做?
此患者诊断SLE也是比较明确的,并逐渐出现血液系统损害、相关性的肺动脉高压及神经精神性狼疮,SLEDAI评分30分:(器质性脑病8分+视觉受损8分+血管炎8分+新出现皮疹2分+补体下降2分+抗ds-DNA升高2分)
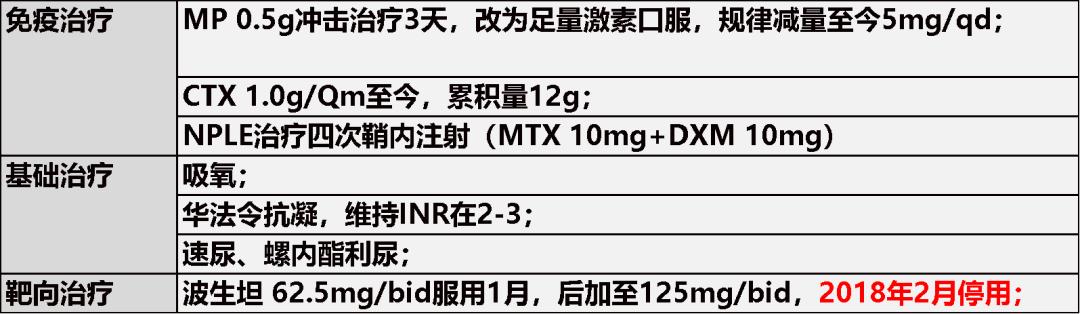
UCG的变化:sPAP由89mmHg逐渐降至正常(89→53→33→正常),后再次升高至76mmHg;右心室/右心房大小由扩大(57、57)逐渐恢复正常(45、55),后再次扩大(60、65);TAPSE由17增加至23,后又减至16;右室FAC由13%增加至26%,后又降至22%。
患者预后:记忆力及计算力稍有恢复、仍较前差、无法胜任数学老师的工作、调离岗位;仍有视野缺损、无法恢复;雷诺现象未见明显改善;2018年2月停用波生坦,2018年6月底出现乏力、间中心悸发作、心功能维持Ⅱ级,但复查UCG提示PAH复发,现再次加用;
两个病例给我们的启示:
相同的疾病为什么会有不同的结局?
相同之中又有什么不同?
停靶向药后为什么有稳定和复发两种结局?
PAH靶向药物治疗的减药和停药指征?真的能停药吗?
下表的对比可能会对我们有一些启示:
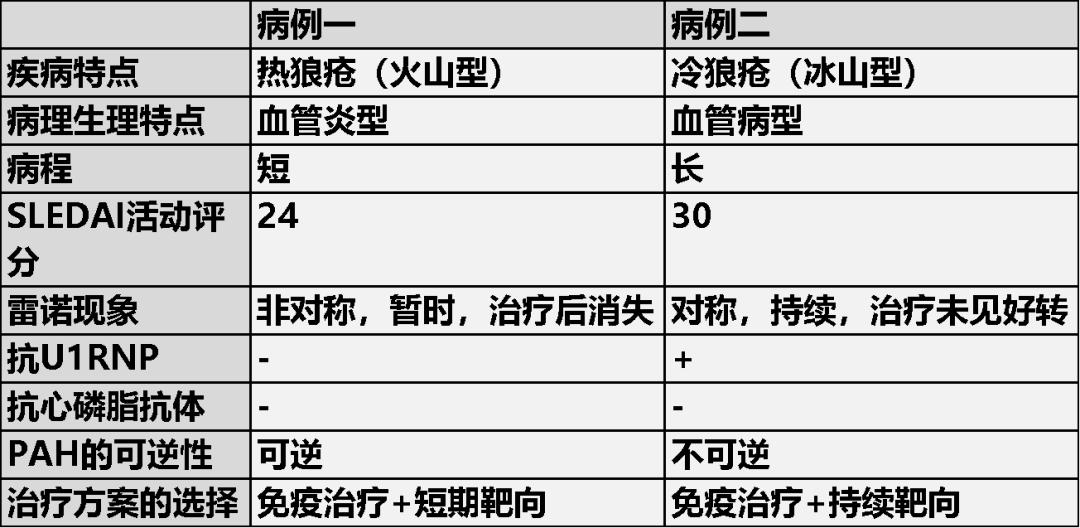
而重度PAH、疾病活动度不高、治疗不可逆、PAH出现病程长的、抗U1RNP阳性的患者则更偏向于血管病机制,此类型对激素及免疫抑制剂效果不明显或不持久,PAH往往不可逆,所以我们不仅要根据SLE病情是否活动来确定治疗方案及减药停药,还要评估PAH的治疗是否达标。
如病例一和病例二在SLE的治疗上均达到了缓解,不同之处在于病例一PAH的治疗也已达标,所以可以停用靶向治疗后没有复发,而病例二SLE虽达到了缓解,但PAH并未达标,虽然sPAP降至正常,但右房右室的大小仍大,这时停用靶向治疗药物PAH复发的风险很大。
所以说SLE缓解而PAH未达标是临床最为困难的选择,通常在SLE维持缓解治疗的基础上加强PAH的靶向治疗,根据危险分层评估随访达到低危标准即临床方面没有右室功能衰竭的表现、无晕厥发作,功能方面WHO心功能稳定在Ⅰ~Ⅱ级、6MWD>380~440m、CPET测定的VO2max>15 mL/min/kg,血清学方面BNP<50 pg/mL或NT-proBNP<300 pg/mL(正常或接近正常),RHC方面RAP<8 mmHg和CI≥2.5 L/min.m2维持半年左右才考虑减停靶向治疗药物。
参考文献
[1]Sun F,Lei Y,Wu W,et al. Two distinct clinical phenotypes of pulmonary arterial hypertension secondary to syetemic lupus erythematosus [J]. Ann Rheum Dis, 2019,78(1): 148-150.
[2] Zhang, N., et al. (2019). "Pulmonary arterial hypertension in systemic lupus erythematosus based on a CSTAR-PAH study: Baseline characteristics and risk factors." Int J Rheum Dis 22(5): 921-928.
本文首发:医学界心血管频道
本文作者:广东省人民医院风湿科 冯媛 、雷云霞
责任编辑:董小雯
版权申明
本文原创 如需转载请联系授权
- End -
看过,请点这里
↓↓↓
原标题:《同病不同命:两位患者的不同结局》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




