- +1
【科技前沿】周鸣/颜宁课题组合作揭示人源二酰甘油酰基转移酶DGAT1 三维结构及催化机制
三酰甘油酯(triacylglycerol, TAG)是生命体中主要的能量储存物质,其合成过程主要有两种路径:3-磷酸甘油路径以及单酰基甘油路径【1】。两种合成路径的最终一步都是二酰甘油酯(diacylglycerol,DAG)的酰基化从而产生TAG,而这一过程是由二酰甘油酰基转移酶(Diacylglycerol-O-Acyltransferase, DGAT)催化完成【2】。人体中有两种序列不同源的DGAT,分别为DGAT1和DGAT2。DGAT1 主要负责脂肪吸收及储存过程中TAG的合成,DGAT2则负责各组织及皮肤基本脂肪的平衡。前期研究表明,DGAT1敲除的小鼠能保持正常的代谢,并且可以抵抗高脂肪饮食引起的肥胖,而DGAT2敲除的小鼠则由于皮肤脂肪的缺失在出生数小时内死亡【3】。因此,DGAT1被认为是重要的治疗肥胖及糖尿病的药物靶点,各药物公司都有针对DGAT1抑制剂开发【4】。
根据序列同源性,DGAT1属于跨膜O-酰基转移酶超家族(Membrane-bound O-acyltransferase superfamily, MBOATs)。MBOATs 超家族是一类广泛存在于不同物种中的多次跨膜酰基转移酶,其成员包括:催化TAG合成的DGAT1【5】,催化胆固醇酯化的酯酰辅酶A:胆固醇酰基转移酶(Acyl-CoA: cholesterol Acyltransferase,ACAT )(注:今日Nature同步在线的另一篇来自颜宁教授课题组的工作解析了ACAT1的结构,详见文末报道。)【6】,以及催化蛋白质脂修饰的PORCN(Porcupine)【7】等。前期华盛顿大学许文清教授组解析了细菌来源的MBOATs超家族蛋白DltB8(),然而DGAT1和DltB有着级低的序列同源性以及截然不同的功能,因此难以通过DltB的结构来预测和研究DGAT1的结构以及底物识别反应机理。前期虽然有很多DGAT1功能相关的研究,但针对其多聚物分子结构、底物识别方式以及反应机理依旧没有明确的结论。
2020年5月13日,贝勒医学院周鸣授课题组和普林斯顿大学颜宁教授课题组合作在Nature上发表文章Structure and mechanism of human diacylglycerol-O-acyltransferase 1 (本文第一作者为贝勒医学院博士生王列,普林斯顿大学钱洪武博士、贝勒医学院的年寅博士,普林斯顿大学韩亦沫博士以及为共同一作。韩亦沫博士现为莱斯大学助理教授,年寅博士现为昆明动物所研究人员)。该工作利用单颗粒冷冻电镜技术,首次解析了分辨率为3.1Å人源DGAT1的同源二聚体结构,并通过结合酶活性实验,确定了酰基辅酶A(acyl-CoA)在DGAT1上的结合位点。

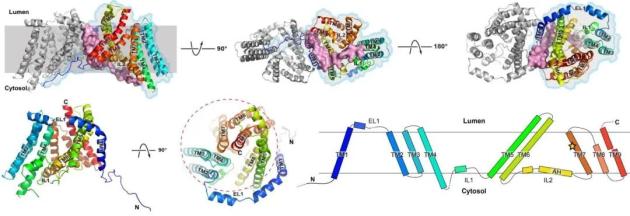
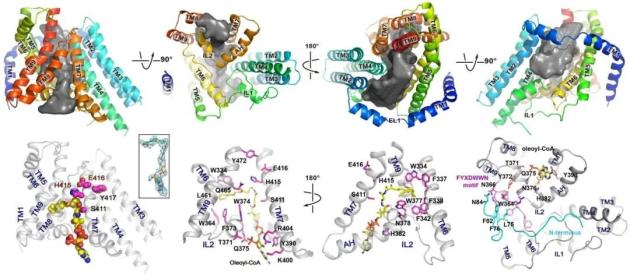
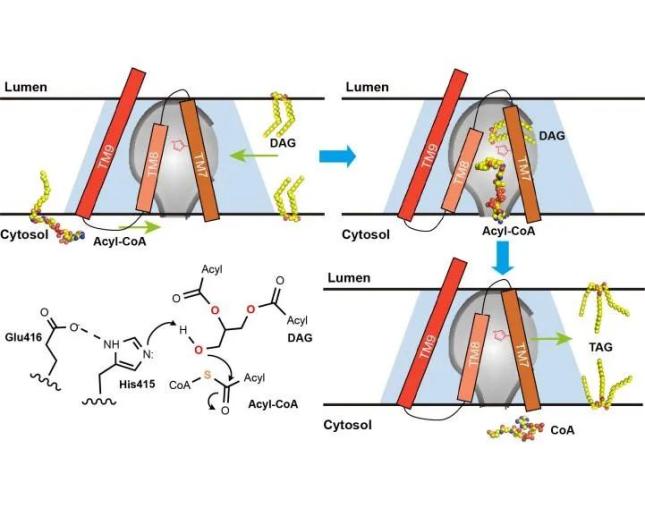
值得一提的是,Nature同步上线了另一篇背靠背的工作,解析了分子量为55 kDa的人类甘油三酯合成与代谢的关键酶——DGAT1的蛋白结构,并系统地阐明了DGAT1识别底物及催化甘油三酯合成的分子机制。该工作由哈佛大学公共卫生学院Robert Farese, Jr. (费波)教授& Tobias Walther(华涛北)教授联合课题组以及哈佛大学医学院廖茂富教授课题组合作完成,详细报道详见今日BioArt的单独报道。


中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
微信号:BSC-1979
原标题:《【科技前沿】周鸣/颜宁课题组合作揭示人源二酰甘油酰基转移酶DGAT1 三维结构及催化机制》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




