- +1
【学术前沿】”双剑合璧”——李大力组开发新型双碱基基因编辑器
以下文章来源于BioArt ,作者BioArt

高屋建瓴,提供专家点评,引导学术争论,展现学术批评;诚心实意,关注科研生态,推广科研经验,倡导师生交流。

获取更多CSCB2020相关资讯

据 ClinVar 数据显示,人类约58%的遗传疾病是由于碱基突变引起的【1】。CRISPR/Cas9技术可实现精确的碱基修复,但其效率低下(0.1%-5%),且存在非靶向切割,高度精确修复能力的极大地限制了广泛的的应用。碱基编辑系统(base editing)依据nickase Cas9(D10A)融合了不同的碱基修饰酶分为胞嘧啶碱基编辑器(cytosine base editors, CBE)和腺嘌呤碱基编辑器(adenine base editors, ABE)。这两种碱基编辑器能在不产生DNA双链断裂的情况下,在4-8(距离PAM远端起)窗口内分别实现精准的C•G到T•A或A•T到G•C 的替换,高效、精准和低脱靶的特性使其逐渐成为基因编辑领域的新宠【2,3】。在疾病模型制作、精准基因治疗、动植物遗传育种,耐药性筛选等领域展现出光明的发展前景【4,5】。
然而,现有的碱基编辑器只能催化单一类型碱基的转换,这限制了其广泛应用。因此,开发新的碱基编辑器能高效地同时产生两种不同碱基的突变,这既是概念上的创新,也将极大地丰富碱基编辑工具,在基因治疗,物种改良和分子进化等方面都有重要意义。
2020年6月1日,华东师范大学李大力课题组在Nature Biotechnology杂志发表了题为“Dual base editor catalyzes both cytosine and adenine base conversions in human cells”的研究论文。该研究将人类胞嘧啶脱氨酶hAID-腺嘌呤脱氨酶-Cas9n(SpCas9 D10A突变体)融合在一起,开发了一种新型双功能高活性碱基编辑器-A&C-BEmax,它可以在同一等位基因的靶序列上实现C>T和A>G的高效转换。与CBE和ABE相比,A&C-BEmax拓宽了C>T的编辑窗口,提高了编辑效率;A>G的窗口保持不变,效率略有下降,RNA脱靶水平大幅降低。

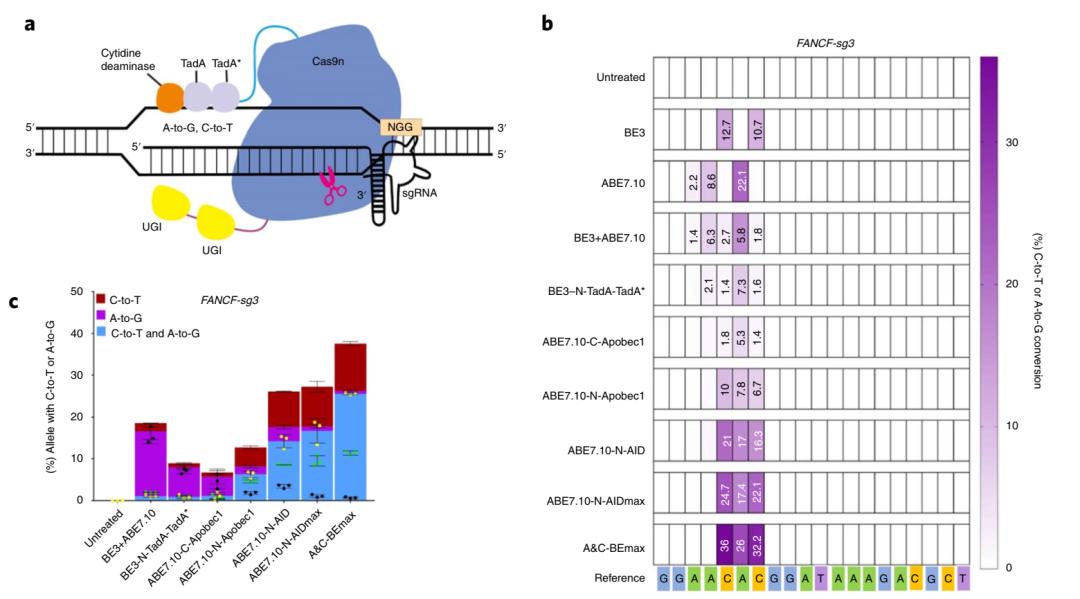
为了进一步提高效率,课题组通过密码子、核定位信号、linker序列以及UGI串联等多轮优化获得了一种高效的A/C同时转换的编辑器,并命名为:A&C-BEmax(图1)。经过上述系列优化,与原始构建体相比,A&C-BEmax的碱基转化效率,产物纯度和A/C同时转换活性显著提高,C(胞嘧啶)的编辑窗口大幅拓宽,且更安全,RNA脱靶率更低。
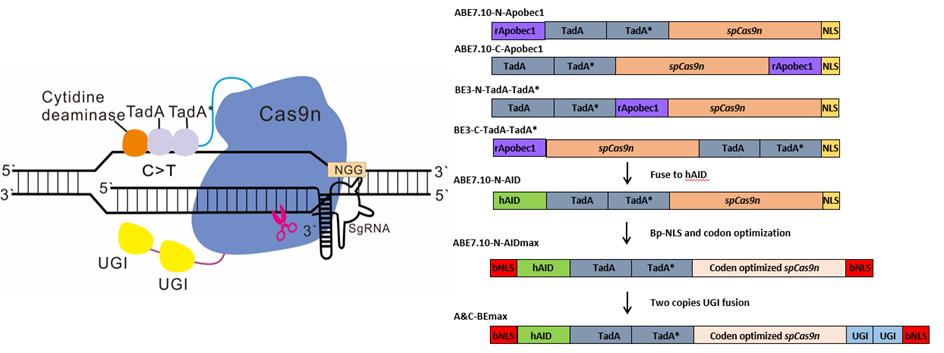
为了公正地评价A&C-BEmax的性能,科研人员在HEK293T细胞中测试了28个内源性靶点(其中4个靶点仅包含Cs或As)同时和与ABEmax和AID-BE4max进行对比。测试显示, A&C-BEmax的编辑窗口从C3-C10位扩展到了C2-C17位,在C7-C17位的编辑活性相对于AID-BE4max提高了1.9-14倍,而A>G的编辑效率与ABEmax相似或略有降低,但比ABEmax在RNA上的脱靶率更低,同一等位基因的A和C同时突变效率最高达到30%。(图2)
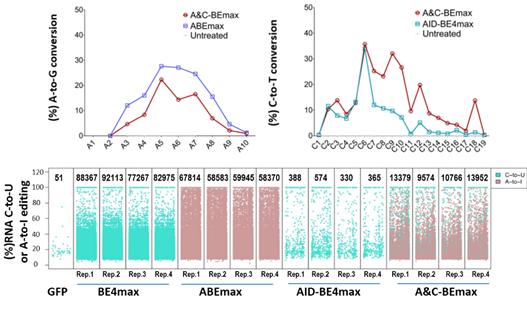
那么这么好的工具有什么独特的用途呢?论文进一步验证了A&C-BEmax在基因治疗中的应用(图2),将A&C-BEmax递送到红细胞前体细胞中(HUDEP-2)。结果表明,A&C-BEmax能高效地破坏胎儿期血红蛋白基因HBG1/2启动子区域转录抑制因子BCL11A结合位点(-114C>T或-115C>T)并同时创建新的转录激活因子GATA1的结合位点(-113A>G),与周围单独产生C的编辑细胞相比,分化的HUDEP-2细胞中更高的HBG表达水平。(图3)该工作展示了A&C-BEmax这一新型双碱基编辑系统对于精准治疗β-血红蛋白病的巨大潜力。
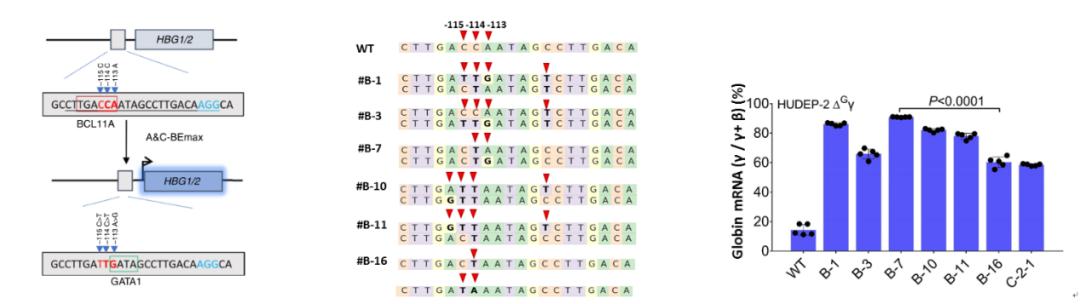
最后,与杨力课题组合作,通过大数据挖掘,在ClinVar【6】和dbSNP【7】 (SNPs)临床数据库中发现了临床中A&C-BEmax可同时靶向AC纠正203个临床报道的致病突变;进一步拓展PAM为NG时, Cas9-靶向范围增加了2.8倍(〜573个)。研究团队还统计到,A&C-BEmax与ABE或CBE相比,能实现60个额外的密码子更改(18个氨基酸替换),这些更改无法使用现有的单碱基编辑器做到。与单脱氨酶碱基编辑器相比,A&C-BEmax能高效地同时引入A>G和C>T编辑,因此产生的突变组合多样性更大,且更安全。因此,这种扩展的编辑器将广泛用于许多不同的研究和应用。A&C-BEmax是成为分子记录系统(例如谱系追踪)以及饱和诱变筛选、定向进化强而有力的工具。
非常有趣的是,同一天Nature Biotechnology还在线发表了另外两个在哺乳动物细胞中开发双碱基编辑器的工作,分别来自日本东京大学Nozomu Yachie实验室以及美国麻省总医院Keith Joung实验室。
Nozomu Yachie实验室将来源于七鳃鳗的胞嘧啶脱氨酶PmCDA1和鼠源的胞嘧啶脱氨酶rAPOBEC1分别和腺苷脱氨酶(TadA)融合到nCas9(D10A)的C端和N端,开发了3种新的双碱基碱基编辑器—Target-ACE/Target-ACEmax/ACBEmax。他们通过该系统成功在哺乳动物细胞中实现了A/C的同时突变,平均编辑效率最高分别达C为50%和A为40%。大量实验数据统计显示,他们发现双碱基编辑器的特性和单个碱基编辑工具的编辑效率,突变窗口和突变谱等特性相当, DNA和RNA脱靶,都在单种碱基编辑器的范围内。Target-ACE与ABE+CBE共同作用相比,能更有效地在目标位点的序列窗口中同步高效地实现C>T和A>G点突变,且Target-ACE比单独的CBE或ABE能诱导更多种类型的氨基酸转换。最后他们使用深度测序数据对编辑模式进行建模,模拟了Target-ACE和其他单种碱基编辑工具在整个人类基因组中的编辑谱,展现了Target-ACE能产生更多氨基酸突变种类,对于分子进化有重要意义。


上述四个团队以2种不同的构建策略,开发了类似功能的新型双碱基编辑器,都实现只有一个靶点的引导下就可以诱导靶位点C>T和A>G的同时突变。李大力和高彩霞课题组经过不同的位置测试分别将胞嘧啶脱氨酶hAID与APOBEC3A和腺嘌呤脱氨酶ecTadA-ecTadA7.10同时融合在nCas9(D10A)的N端,分别证明了双碱基编辑器可有望应用于基因治疗和作物改造。两个工作也几乎同时投稿。同期发表的这两个组的研究,虽然也具有AC同时突变的功能,但是李大力课题组开发的A&C-BEmax在动物细胞中表现出更高的CBE活性、更广的编辑窗口以及更高的AC同时突变的效率,将更有潜力成为治疗学和谱系追踪、饱和突变筛选等生物技术强有力的工具。值得注意的是,同样是哺乳动物细胞,李大力课题组的工作展现了更高CBE活性和突变窗口以及A/C同时突变的效率,证明A&C-BEmax相比SPACE和Target-ACE具有更好的表现。
据悉,华东师大生命科学学院2016级博士研究生张晓辉,2017级博士研究生朱碧云和2018级硕士研究生陈亮为该论文的共同第一作者,李大力教授为本文通讯作者,中国科学院上海生命科学研究院计算生物学研究所杨力研究员参与了部分研究工作。
相关阅读:
;
;
;
专家点评
左二伟(中国农科院农业基因组研究所)、杨辉(中科院神经所)
双剑合璧——双碱基基因编辑工具的开发与应用
单碱基突变是人类的遗传疾病主要致病原因之一。通过CRISPR/Cas9结合NHEJ或者HDR方式修复碱基突变的方法,已经在动物模型上实现了治疗人类遗传疾病的目的。但在CRISPR/Cas9介导的修复方法中,同时在大量细胞诱导产生的DNA双链断裂有可能导致基因组的异位、倒位、激活原癌基因(如p53)异常表达等潜在问题,并对基因组存在难以预测的损伤【8】。为了消除这些不利因素,基因编辑大牛David liu与同事将失去催化活性的Cas9与脱氨酶融合,在sgRNA指导下,在不产生双链断裂的情况下实现单核苷酸的定向突变,建立了单碱基基因编辑系统【9】。较高安全性和高效性促使单碱基编辑系统迅速应用于多种动物、植物以及人类基因组的编辑研究,并且逐渐与动物模型结合进行遗传疾病研究与治疗的探索,为多种遗传性疾病的治疗带来了希望。
目前较为成熟的单碱基基因编辑技术包括CBEs (C→T)与ABEs (A→G)两种,都源自哈佛大学David R. Liu实验室,在相关领域科学家的努力下,这两种工具的碱基编辑效率与精确性等也逐步得到了提高与改善【9】。尽管这两种单碱基基因编辑技术具有广泛的应用性,但想要同时对相邻位置的两个碱基位点进行编辑的时候,这两种单碱基基因编辑技术的限制性便有所体现——同时或分步使用两种单碱基编辑工具进行基因编辑不但效率低,还可能带来更多的脱靶效应,在可行性与安全性上都不理想。
近日,Nature Biotechnology (NBT) 杂志连续推出4篇双碱基基因编辑技术的相关研究论文,其中两篇分别由中科院遗传发育所的高彩霞课题组与华东师范大学李大力课题组完成。这4篇论文中开发的双碱基基因编辑工具具有相似的结构,能对临近的CA碱基同时进行CA→TG的碱基替换,实现双碱基基因编辑,且该工具有较好的安全性,对人类遗传疾病的治疗及动植物基因编辑、遗传育种等都具有较高的应用价值。这四篇论文的连续发表充分表明了碱基基因编辑技术是目前基因编辑领域的热点,也说明了碱基编辑工具在未来将得到更进一步发展与完善,并更好地为科研与临床应用服务。接下来我们对这四篇文章分别进行梳理与解读,以供读者探讨。
在同时上线的4篇文章中,哈佛医学院J. Keith Joung课题组的设计较为简单也易理解。他们将传统的CBEs工具与ABE工具相结合,在nCas9的N端保留AID(A→G的主要功能元件),并将rAPO1(C→T的主要功能元件)与UGI整合到nCas9的C端,设计出名为SPACE(synchronous programmable adenine and cytosine editor (SPACE))的双碱基基因编辑工具,并成功在HEK293T细胞上实现了双碱基基因编辑,且在其后对这一工具DNA与RNA的脱靶性(off-target)进行了相关检测。

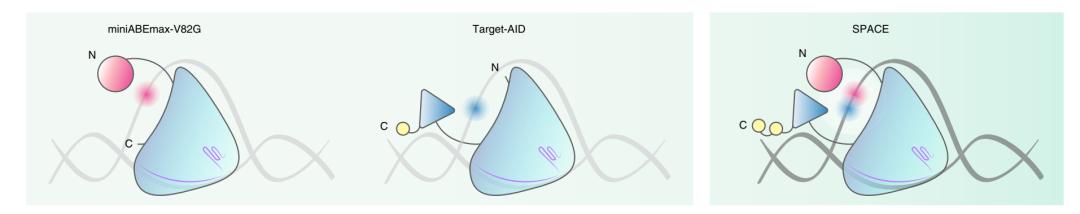



然而,在这些研究中仍然存在需要继续优化与完善的地方。经典的CBEs与ABEs工具在单独使用时具有5-6nt左右较窄的碱基编辑窗口(window)【9,10】,而整合形成的双碱基基因编辑工具的碱基编辑窗口在李大力等的报道中则C→T与A→G的窗口分别扩增到了16与13个核苷酸,在其他几篇文章中也有类似的现象。虽然这些特性在扩展双碱基基因编辑能力时具有一定的意义,但从另一方面而言,编辑窗口的扩张代表着碱基基因编辑工具在进行单碱基基因编辑时精确性与特异性的降低,也暗示着在打靶位点约20bp的片段内容易出现不符合预期的突变情况。然而有意思的是,编辑窗口以及可编辑碱基类型的增加,或许更适合用作为高通量筛选工具【12,13】。
同时,在这四篇报道中,双碱基基因编辑工具的安全性仍需要进一步地验证与评估。虽然双碱基基因编辑工具CBEs工具相比具有较低的脱靶效应,但这些脱靶效应不可忽视,它们仍然是限制双碱基基因编辑工具在生命科学研究与临床应用中的重要因素。因此,利用具备更低脱靶效果的APOBEC/TAD变体重新整合双碱基基因编辑工具可能是提高该工具安全性的有效方法之一。
尽管双碱基基因编辑工具仍需要进一步的研究与完善,但它的出现仍然为人们提供了更为方便有效的基因编辑策略,增进了我们对碱基基因编辑工具的认识与理解。同时,在这四篇报道中对双碱基基因编辑工具的相关应用暗示了我们这一工具在动物、植物多物种中的可用性,并说明了该工具在基础研究与医学研究中广阔的应用前景。例如双碱基基因编辑工具在红细胞细胞系HUDEP-2中的应用说明了这一工具在临床治疗中的潜力,而双碱基基因编辑工具在水稻中的应用则说明了这一工具在植物抗病育种中的重要价值。这些研究为基因编辑工具的发展方向及其在各领域中的广泛应用提供了很好的参考,并为我们更进一步地开发与利用碱基基因编辑工具提供了新的思路。
原文链接:
https://doi.org/10.1038/s41587-020-0527-y
https://doi.org/10.1038/s41587-020-0509-0
https://doi.org/10.1038/s41587-020-0535-y
参考文献
1.Landrum, M.J. et al. ClinVar: public archive of interpretations of clinically relevant variants. Nucleic Acids Res .44, D862-D868 (2016).
2.Komor, A.C., Kim, Y.B., Packer, M.S., Zuris, J.A. & Liu, D.R.J.N. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature 533, 420-424 (2016).
3.Gaudelli, N.M. et al. Programmable base editing of A• T to G• C in genomic DNA without DNA cleavage. Nature 551, 464-471 (2017).
4.Yang, B., Yang, L. & Chen, J.J.T.C.j. Development and application of base editors. CRISPR J 2, 91-104 (2019).
5.Hess, G.T., Tycko, J., Yao, D. & Bassik, M.C.J.M.c. Methods and applications of CRISPR-mediated base editing in eukaryotic genomes. Mol Cell 68, 26-43 (2017).
6.Yang, L. et al. Increasing targeting scope of adenosine base editors in mouse and rat embryos through fusion of TadA deaminase with Cas9 variants. Protein & Cell 9, 814-819 (2018).
7.Sherry, S.T. et al. dbSNP: the NCBI database of genetic variation. Nucleic Acids Res. 29, 308-311 (2001).
8.Cox, D. B. T., Platt, R. J., & Zhang, F. (2015). Therapeutic genome editing: prospects and challenges. Nature medicine, 21(2), 121.
9.Komor, A. C., Kim, Y. B., Packer, M. S., Zuris, J. A., & Liu, D. R. (2016). Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature, 533(7603), 420-424.
10 .Rees, H. A., & Liu, D. R. (2018). Base editing: precision chemistry on the genome and transcriptome of living cells. Nat Rev Genet, 19(12), 770-788. doi: 10.1038/s41576-018-0059-1
11 Gaudelli, N. M., Komor, A. C., Rees, H. A., Packer, M. S., Badran, A. H., Bryson, D. I., & Liu, D. R. (2017). Programmable base editing of A*T to G*C in genomic DNA without DNA cleavage. Nature, 551(7681), 464-471. doi: 10.1038/nature24644
12.Li, Q., Li, Y., Yang, S., Huang, S., Yan, M., Ding, Y., . . . Sun, Z. (2018). CRISPR–Cas9-mediated base-editing screening in mice identifies DND1 amino acids that are critical for primordial germ cell development. Nature cell biology, 20(11), 1315-1325.
13.Liu, Y., Cao, Z., Wang, Y., Guo, Y., Xu, P., Yuan, P., . . . Wei, W. (2018). Genome-wide screening for functional long noncoding RNAs in human cells by Cas9 targeting of splice sites. Nature Biotechnology, 36(12), 1203.
来源:BioArt


原标题:《【学术前沿】”双剑合璧”——李大力组开发新型双碱基基因编辑器》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




